

组蛋白修饰是指在组蛋白的氨基酸残基上发生的翻译后修饰(PTM),这些修饰能够改变染色质的结构和功能,进而影响基因的表达。常见的组蛋白修饰包括甲基化、乙酰化和磷酸化等。这些修饰通过招募或排斥特定的蛋白质复合物,调节基因的转录活性。其中,组蛋白单胺化修饰是一种新型的组蛋白修饰,涉及单胺类神经递质(如血清素、多巴胺)与组蛋白上的谷氨酰胺残基(如H3Q5)的共价结合。这种修饰在大脑中尤为重要,因为它不仅影响局部染色质状态,还能调节全局的基因表达。
2025年1月8日清华大学基础医学院、美国纪念斯隆凯特琳癌症中心和美国弗里德曼脑研究所联合在Nature杂志(IF:50.5)上发表了题为“Bidirectional histone monoaminylation dynamics regulate neural rhythmicity”的研究文章,该研究发现了组蛋白H3Q5位点的单胺化修饰,且该修饰由转谷氨酰胺酶2(TG2)催化,并受到昼夜节律的调控。H3Q5的单胺化修饰包括血清素化、多巴胺化和组胺化,它们在细胞中可以相互转换。组胺化修饰与昼夜节律基因的表达和行为有关,并能够抑制WDR5蛋白的结合,从而拮抗组蛋白H3赖氨酸4位点的甲基化。这些发现揭示了H3单胺化修饰的动态调控机制,以及其在神经元节律性调节中的重要作用。

组蛋白单胺化修饰
组蛋白单胺化修饰的发现源于对神经递质与表观遗传调控之间联系的探索。早期研究表明,血清素和多巴胺等单胺神经递质不仅参与神经传导,还可以被转氨化到组蛋白H3的谷氨酰胺残基上,形成新的PTM(称为血清素化和多巴胺化)。H3Q5是主要的修饰位点,这些单胺化修饰在神经转录编程中发挥重要作用。这一发现不仅揭示了神经递质在表观遗传调控中的新功能,也为研究神经-表观遗传相互作用提供了新的视角。然而,H3单胺化修饰的调控机制尚不清楚。
TG2是组蛋白单胺化修饰的“writer”与“eraser”
为了深入理解H3单胺化修饰的调控机制,研究聚焦于转谷氨酰胺酶2(TG2)。利用5-PT化学探针,成功追踪了H3的胺基化反应,揭示了TG2在其中的关键作用。通过构建TGM2敲除细胞和过表达实验,进一步证实了TG2是H3胺基化的主要“writer”。此外,脉冲追踪实验的结果表明,TG2不仅能够催化H3胺基化修饰,还能够去除这些修饰。研究表明TG2在调节H3单胺化修饰动态平衡中扮演了双重角色。
TG2是H3胺基化的交换剂
为了更全面地了解TG2在H3单胺化修饰中的功能,科研人员进行了LC-MS分析,并利用NCPs进行体外竞争实验。结果表明,TG2不仅能够去除H3Q5上的胺基化修饰,还能够将这些修饰交换为新的胺基化修饰(H3Q5ser或H3Q5dop)。这一发现为我们理解H3单胺化修饰的多样性和复杂性提供了新的视角。在研究中,还发现H3Q5组胺化(H3Q5his)是TG2介导的另一种重要的胺基化修饰,并且具有昼夜节律性表达。这一发现进一步支持了H3单胺化修饰在神经节律性调控中的潜在作用。
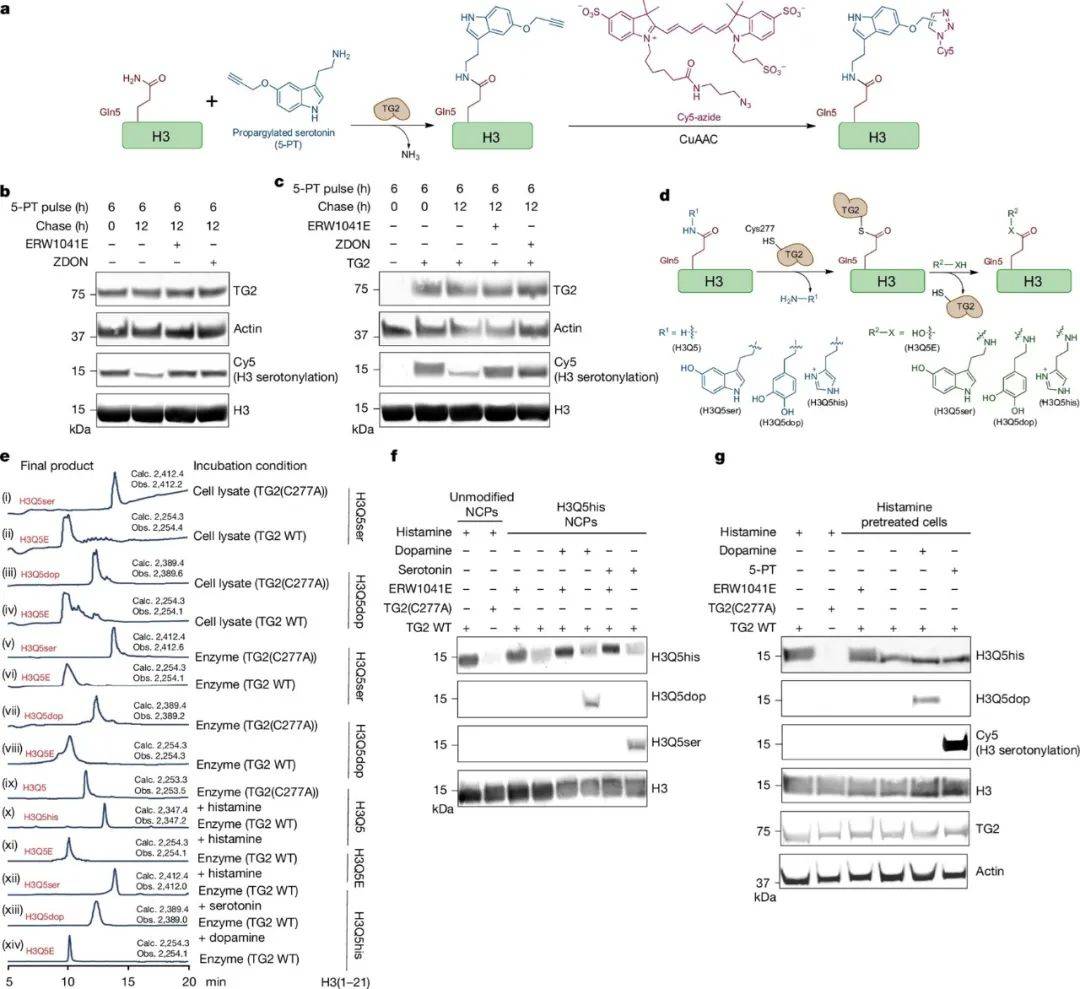 图1 TG2是H3单胺化的writer、eraser和交换剂。
图1 TG2是H3单胺化的writer、eraser和交换剂。
(图源:Zheng, et al., Nature, 2025)
H3Q5his的生物学功能
为了揭示H3Q5his在细胞中的生物学功能,进行了一系列实验。体外竞争实验的结果表明,H3Q5his可以抑制WDR5与H3的结合。进一步地,LC-MS/MS分析揭示了H3Q5his能够抑制MLL-SETD1复合物的H3K4甲基化活性。这些发现为理解H3Q5his如何影响基因表达提供了重要线索。此外,CUT&RUN-seq和qPCR分析的结果表明,H3Q5his在脑中的表达具有昼夜节律性,并与昼夜节律基因表达密切相关。这进一步强调了H3Q5his在神经节律性调控中的核心地位。
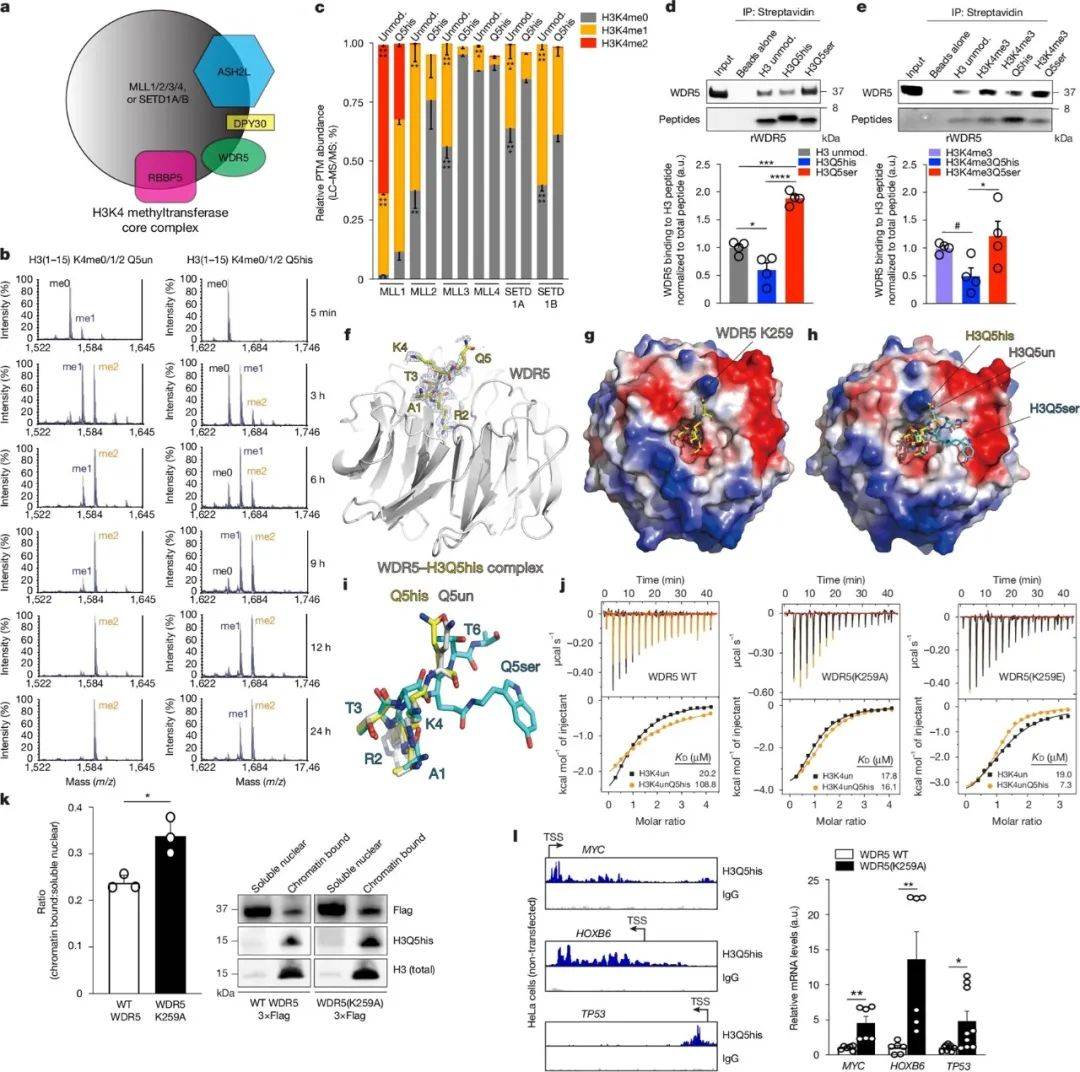 图2 H3Q5his拮抗H3K4甲基转移酶活性和WDR5结合
图2 H3Q5his拮抗H3K4甲基转移酶活性和WDR5结合
(图源:Zheng, et al., Nature, 2025)
H3Q5his对神经节律性的影响
为了探究H3Q5his对神经节律性的具体影响,采用了AAV转导技术降低脑干下丘脑中H3Q5his的表达水平。通过RNA-seq和qPCR分析,发现H3Q5his的缺失会导致昼夜节律基因表达紊乱。这一发现为理解H3Q5his在维持昼夜节律性中的重要性提供了直接证据。进一步地,行为学实验的结果表明,H3Q5his的缺失会导致小鼠的昼夜节律性活动发生变化。不仅揭示了H3Q5his在调节神经节律性中的关键作用,还为针对神经功能紊乱等疾病的治疗提供了新的潜在靶点。
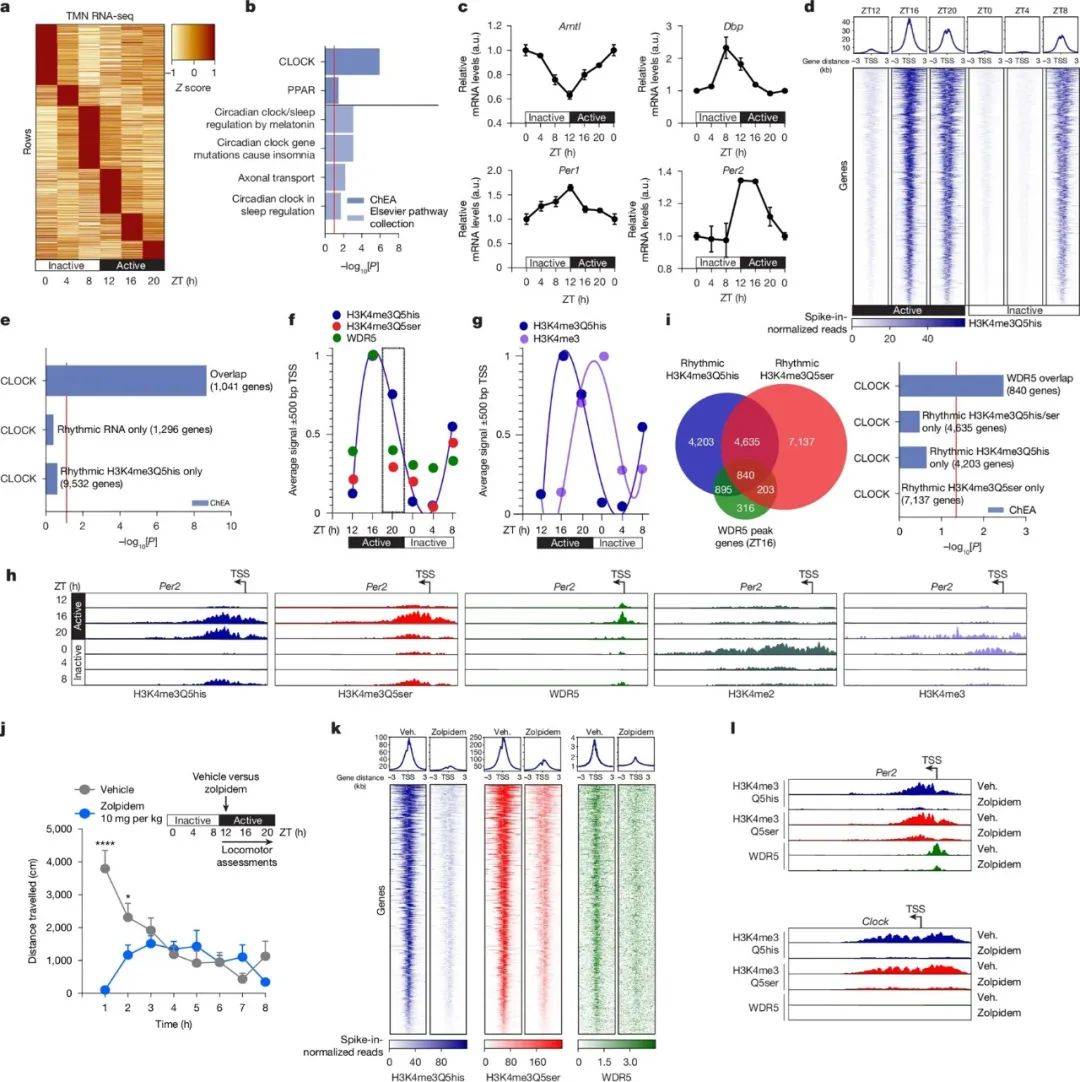 图3 神经H3Q5单胺化有昼夜节律性的
图3 神经H3Q5单胺化有昼夜节律性的
(图源:Zheng, et al., Nature, 2025)
H3Q5his调节神经节律性的机制模型
基于以上实验结果,科研人员提出了一个H3Q5his调节神经节律性的机制模型。在这一模型中,H3Q5his通过抑制WDR5与H3的结合,从而抑制MLL-SETD1复合物的H3K4甲基化活性。由于H3Q5his的表达水平具有昼夜节律性,因此它可以调节WDR5在CLOCK-BMAL1靶基因上的富集,进而影响昼夜节律基因的表达。这一模型为理解H3单胺化修饰如何参与神经节律性调控提供了重要的理论框架。
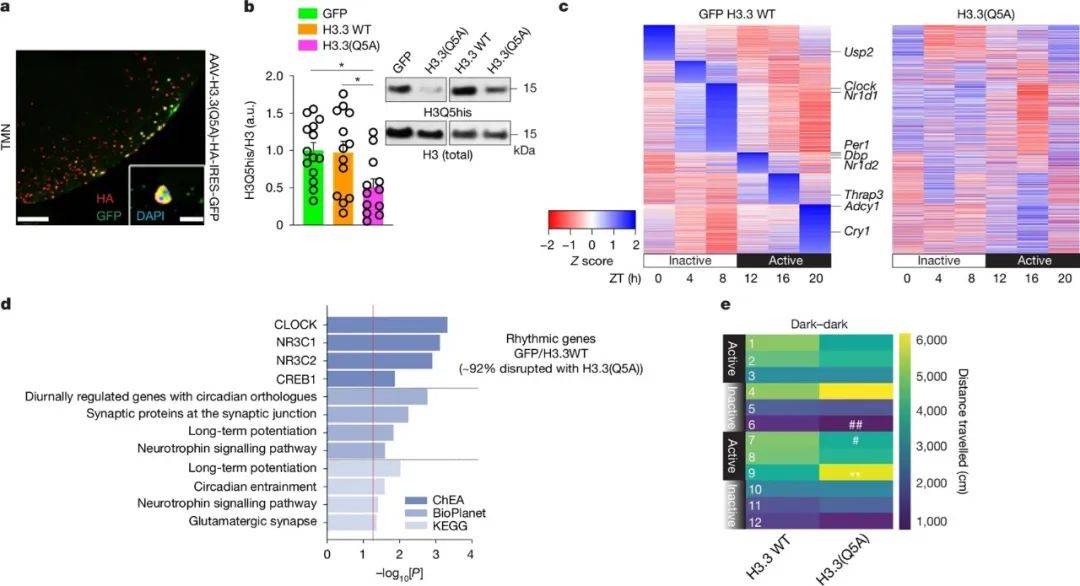 图4 H3Q5单胺化因果关系导致转录和行为节律
图4 H3Q5单胺化因果关系导致转录和行为节律
(图源:Zheng, et al., Nature, 2025)
文章小结
综上所述,本研究不仅显著提升了我们对组蛋白单胺化修饰,尤其是H3Q5位点的胺基化,在细胞生物学中复杂作用的认知,而且为神经节律性调控这一关键生物学领域的机制研究开辟了新路径。通过揭示H3Q5his的昼夜节律特性及其对基因表达的精细调控,本研究为理解生物体内时间生物学的基本规律提供了重要依据。此外,H3Q5his缺失导致昼夜节律基因表达异常及小鼠行为节律改变的发现,不仅强调了这一修饰在维持正常神经节律性中的核心作用,也为探索神经功能紊乱、睡眠障碍等相关疾病的发病机制及潜在治疗策略提供了全新视角。
拜谱小结
拜谱生物作为一家国内领先的多组学服务公司,可提供完善成熟的蛋白质组学、修饰蛋白质组学、代谢组学、转录组学等多组学产品技术服务体系,整合多组学数据进行深入挖掘分析,全面解析机制机理等,助力高分文章发表。围绕神经递质单胺化修饰,拜谱生物可提供血清素化、多巴胺化、组胺化等单胺化修饰产品,构建了产品全面、技术体系成熟的单胺化系列修饰组学产品,通过使用不同的探针进行检测,能够实现组学层面的蛋白检测,帮助科研人员更深入地研究组蛋白单胺化修饰的机制和功能。
值得一提的是,我们的血清素化项目也取得了显著成果。上海交通大学医学院附属仁济医院上海市肿瘤研究所张志刚课题组和江苏大学附属医院肿瘤研究院王旭课题组,在Molecular Cell(IF:16)上发表了一篇题为“A GAPDH serotonylation system couples CD8+T cell glycolytic metabolism to antitumor immunity”的文章(Mol Cell(IF=16)|化学蛋白质组学助力解析5-羟色胺化翻译后修饰促进CD8+T细胞抗癌机制),拜谱生物为其提供血清素化修饰检测服务。该研究展示了血清素化修饰在免疫代谢中的关键作用,揭示了血清素化修饰在CD8+ T细胞糖酵解代谢中的调控机制,并为抗肿瘤免疫提供了新的靶点。这一成果不仅证明了血清素化修饰在生物学中的广泛应用,也展示了拜谱生物在单胺化修饰研究中的强大支持能力。欢迎大家咨询!
参考文献:
Zheng Q, Weekley BH, Vinson DA, Zhao S, Bastle RM, Thompson RE, Stransky S, Ramakrishnan A, Cunningham AM, Dutta S, Chan JC, Di Salvo G, Chen M, Zhang N, Wu J, Fulton SL, Kong L, Wang H, Zhang B, Vostal L, Upad A, Dierdorff L, Shen L, Molina H, Sidoli S, Muir TW, Li H, David Y, Maze I. Bidirectional histone monoaminylation dynamics regulate neural rhythmicity. Nature. 2025 Jan 8. doi: 10.1038/s41586-024-08371-3