

在生命科学领域,蛋白质糖基化的动态异质性长期被视为“分子暗物质”——其复杂程度远超磷酸化或乙酰化等翻译后修饰,却又因技术瓶颈难以窥见全貌。传统糖蛋白质组学受限于三大桎梏:凝集素富集偏好特定糖型、质谱检测灵敏度不足、动态定量通量有限,导致重要科学问题悬而未决:糖基化如何精细调控神经信号传导?肠道菌群能否通过“分子剪刀”重塑宿主糖型?这些谜题因缺乏全局视角始终无解。
2025年2月10日欧洲分子生物学实验室Mikhail M. Savitski教授团队在Nature Structural & Molecular Biology杂志上发表了题为“Uncovering protein glycosylation dynamics and heterogeneity using deep quantitative glycoprofiling (DQGlyco)”的研究文章,该研究通过开发“深度定量糖基化分析(DQGlyco)”,首次实现单次实验捕获17.7万种N-糖肽,并揭示肠道微生物组通过编辑脑蛋白糖基化影响神经功能的全新机制。这项技术不仅将糖蛋白质组鉴定深度提升25倍,更搭建起连接分子细节与生理表型的桥梁,为疾病精准干预提供全新范式。

方法革新:绘制糖基化“全息地图”
要解析糖基化的“微宇宙”,首先需突破技术天花板。研究团队设计了一套革命性流程:通过苯硼酸(PBA)磁珠的pH敏感共价捕获,结合高盐裂解液去除核酸干扰(图1a),糖肽富集特异性跃升至90%以上。这一设计如同为糖分子量身定制的“分子捕手”,克服了传统凝集素法对高甘露糖型的偏好。为进一步区分复杂糖型,团队引入多孔石墨碳(PGC)色谱作为一级分离,其独特的平面吸附机制可将糖链长度差异仅1个糖单元的糖肽精准区分(图1d)。在小鼠脑组织中,该技术鉴定到177,198种N-糖肽,覆盖3,741个N-糖蛋白上的N-糖基位点,其中65%的位点属首次发现(图1e)。这些数据不仅刷新了糖基化复杂度认知,更为后续机制研究奠定基础。
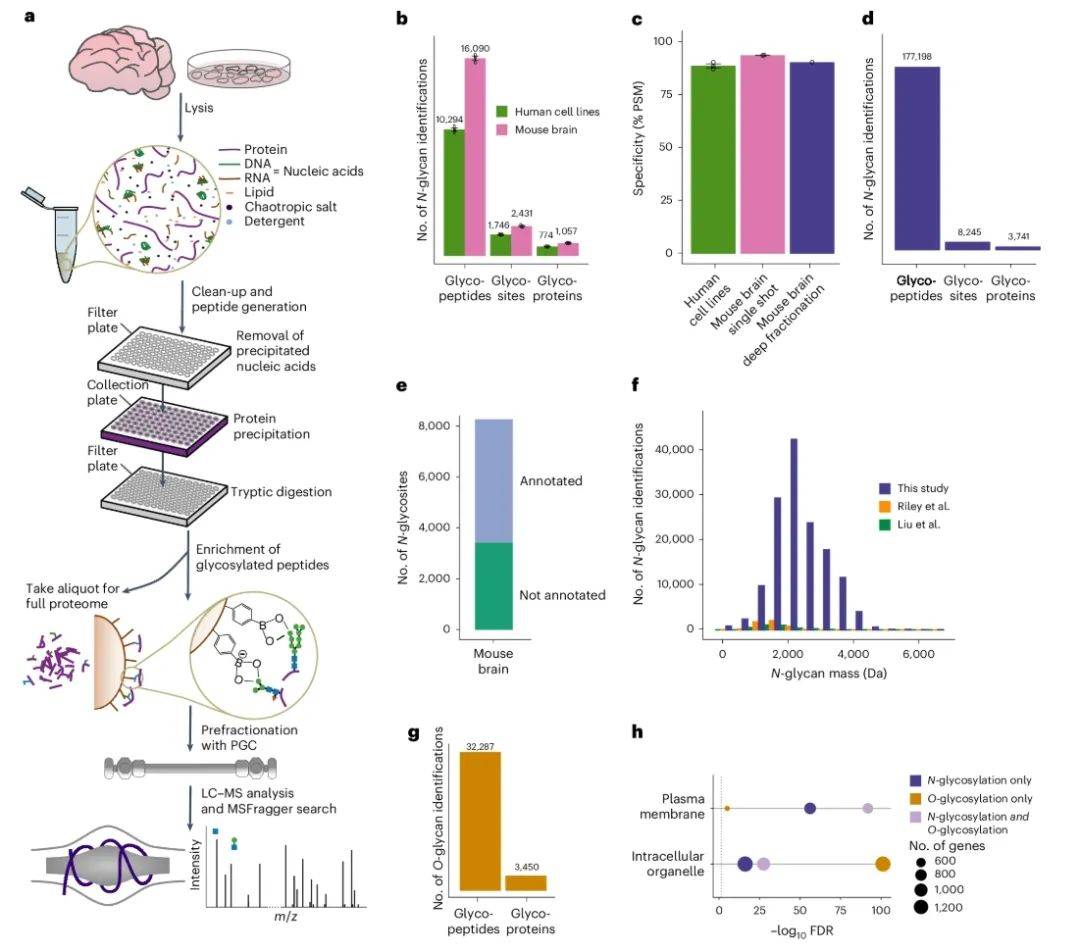 图1 人类细胞系和小鼠大脑中蛋白质糖基化的深度分析
图1 人类细胞系和小鼠大脑中蛋白质糖基化的深度分析
(图源:Potel, et al., Nat Struct Mol Biol, 2025)
异质性密码:糖链如何成为“分子调色盘”
传统观点认为糖基化位点仅携带单一糖型,但DQGlyco揭示的微异质性颠覆了这一认知(图2a)。更惊人的是,每个位点平均检测到17种糖型,兴奋性氨基酸转运蛋白Eaat2的N205位点携带667种糖型,而相邻N215位点仅检测到4种显著变化(图8m)。这种位点特异性调控提示糖基化可能通过局部微环境感知动态调整功能。进一步分析显示,高异质性位点富集于细胞膜受体与黏附分子(图2f),其唾液酸化与岩藻糖基化糖型可能通过空间位阻效应调控配体结合,为药物靶点设计提供新思路。
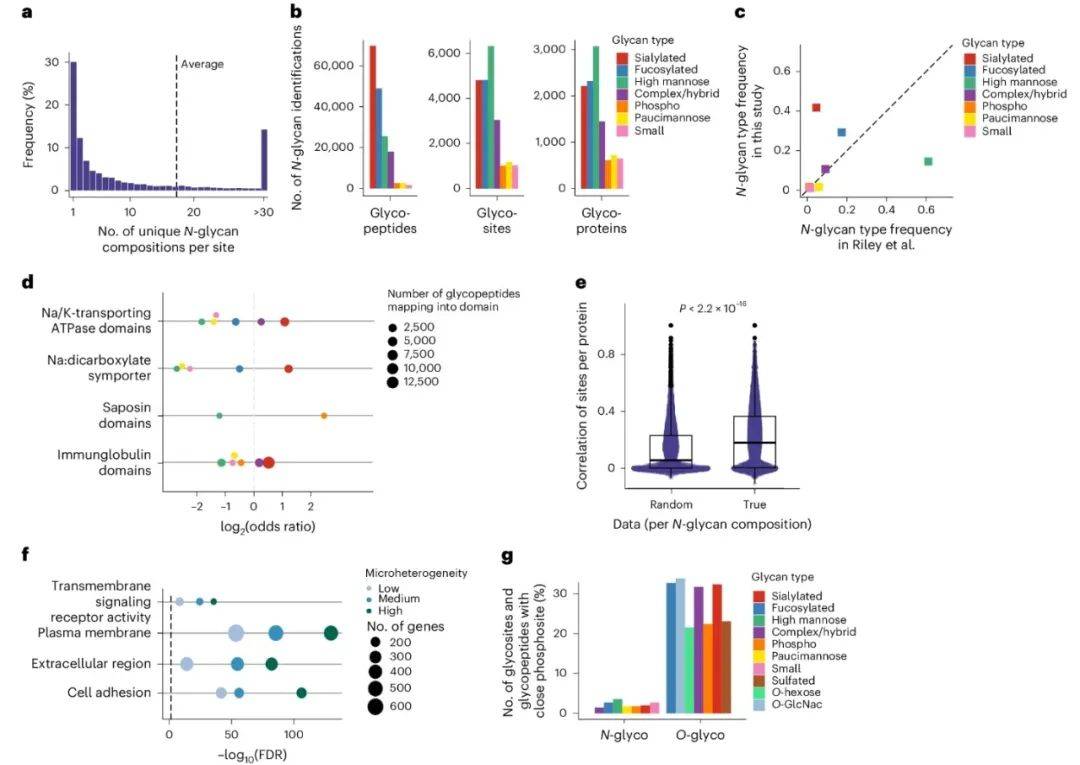 图2 小鼠大脑中的蛋白质糖基化组成和微异质性
图2 小鼠大脑中的蛋白质糖基化组成和微异质性
(图源:Potel, et al., Nat Struct Mol Biol, 2025)
结构决定命运:AlphaFold解码糖型空间密码
当技术突破打开数据洪流,更深层的科学问题浮出水面:为何某些位点会演化出数百种糖型?这种异质性是否遵循某种空间规律?研究团队将AlphaFold预测的蛋白结构引入分析,发现高异质性位点多位于蛋白表面结构化区域(如β转角),其局部溶剂可及性(pPSE)显著高于低异质性位点(图3e)。这种空间暴露特性使糖链加工酶更易接触并进行多步骤修饰。机器学习模型进一步验证,结构特征可预测位点异质性(AUROC=0.707,图3c)。这一发现揭示了糖链加工的“空间法则”:暴露位点更易被糖基转移酶修饰,而隐蔽位点则保留初始高甘露糖型。这种规律为理性设计糖基化修饰提供了理论框架。
 图3 结构背景下的N-糖基化
图3 结构背景下的N-糖基化
(图源:Potel, et al., Nat Struct Mol Biol, 2025)
动态追踪:岩藻糖基化的时空调控网络
为解析糖型动态调控机制,团队利用2-氟岩藻糖(2FF)抑制岩藻糖基化,并通过TMT标记实现时间分辨定量(图4a)。结果显示,岩藻糖基化下降速率存在显著位点差异(图4e):膜受体蛋白NRCAM的N223位点糖型在8小时内快速下调,而N1019位点需72小时才完全响应(图4g)。这种异质性提示糖基转移酶的局部活性差异,或糖链合成路径的分支特异性调控。
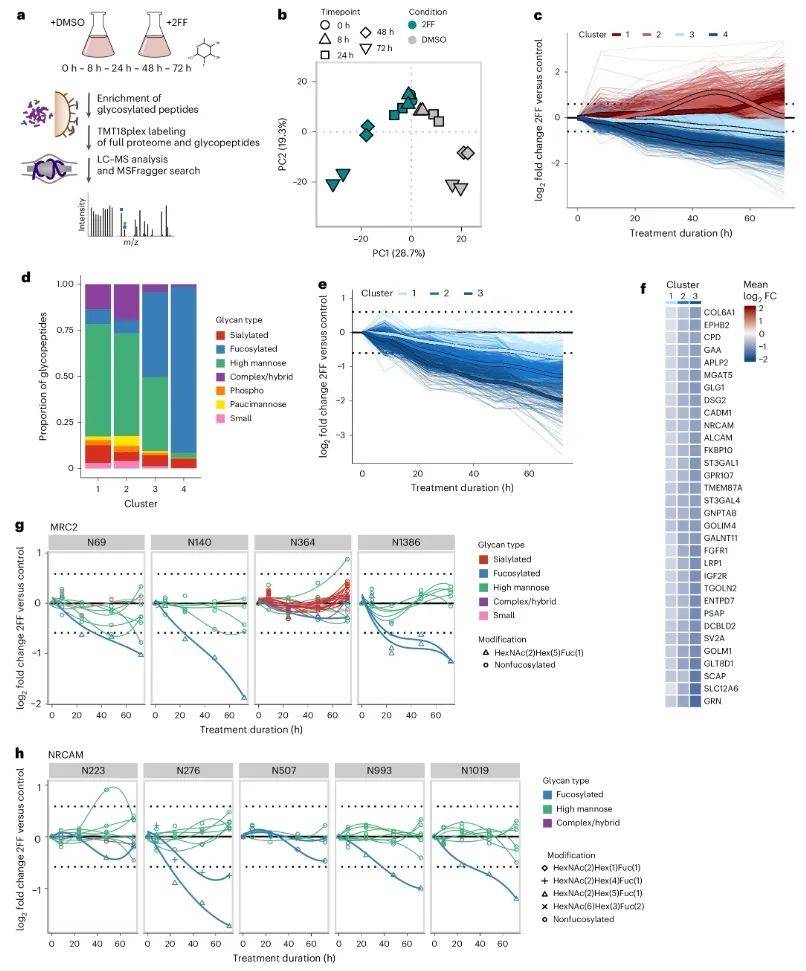 图4 岩藻糖基化抑制的时间过程
图4 岩藻糖基化抑制的时间过程
(图源:Potel, et al., Nat Struct Mol Biol, 2025)
表面糖型标记:区分成熟与未加工糖链
团队猜测糖链加工酶更易接触暴露位点,从而进行多步骤修饰。为了验证这一假设,他们用蛋白酶K与PNGase F处理活细胞(图5a),首次实现表面成熟糖型的原位标记。结果显示,膜表面糖型以唾液酸化/岩藻糖基化为主,而胞内未成熟糖型则富含高甘露糖链(图5e),这与高尔基体加工路径完全吻合。而溶酶体蛋白特异地携带磷酸化糖型(图5g),直接印证甘露糖-6-磷酸的靶向功能。这一技术为研究糖型功能提供了空间分辨工具。
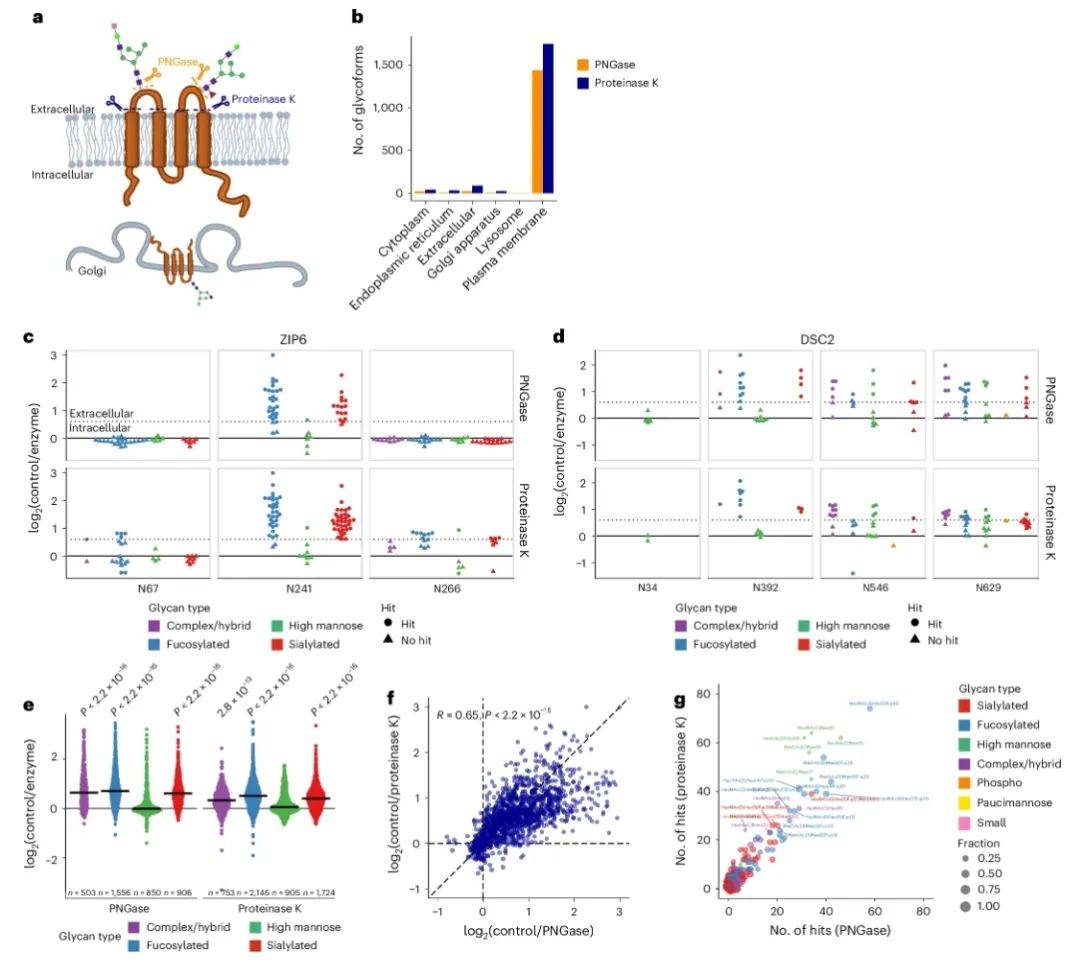 图5 表面暴露的糖型的系统表征
图5 表面暴露的糖型的系统表征
(图源:Potel, et al., Nat Struct Mol Biol, 2025)
组织特异性:从“共性修饰”到“个性签名”
不同组织如何通过糖基化实现功能分化?通过对比小鼠脑、肝、肾组织(图6a),团队发现约30%的糖基化位点具有组织特异性(图6d)。例如,胰岛素受体N445位点在脑中富集唾液酸化糖型,而在肝中则以岩藻糖基化为主(图6h)。这种差异与组织特异性糖基转移酶表达相关,并可能影响受体激活阈值,为器官特异性药物设计提供新思路。
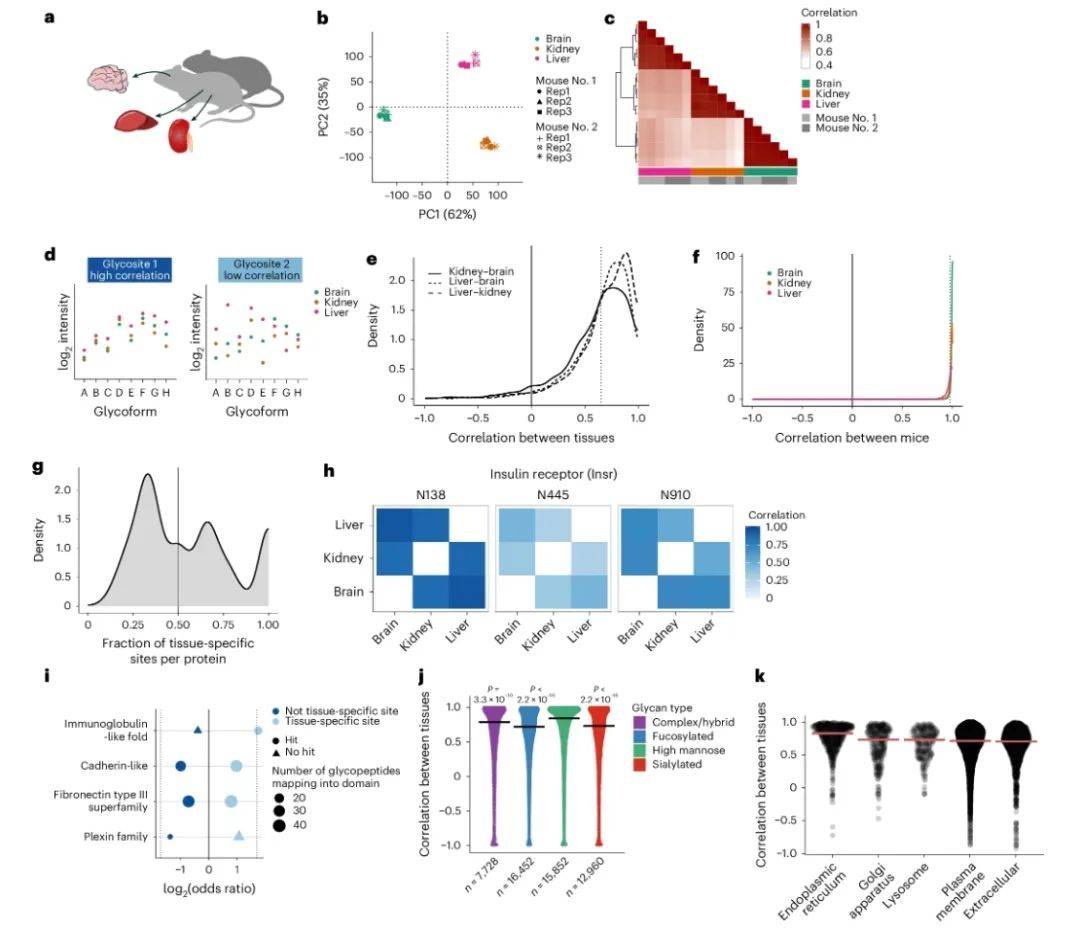 图6 跨组织糖蛋白质组的定量分析
图6 跨组织糖蛋白质组的定量分析
(图源:Potel, et al., Nat Struct Mol Biol, 2025)
生物物理效应:糖型调控蛋白状态
糖基化如何影响蛋白功能?通过溶解度分析(图7a),团队发现高甘露糖型倾向于增加蛋白溶解性,而唾液酸化糖型则促进膜定位(图7b)。例如,钙黏蛋白Cdh13的N86位点(前肽区域)糖型高度可溶,而成熟区域的N489位点糖型则与膜紧密结合(图7c)。这种差异提示糖基化可通过调控蛋白相变影响其功能状态。
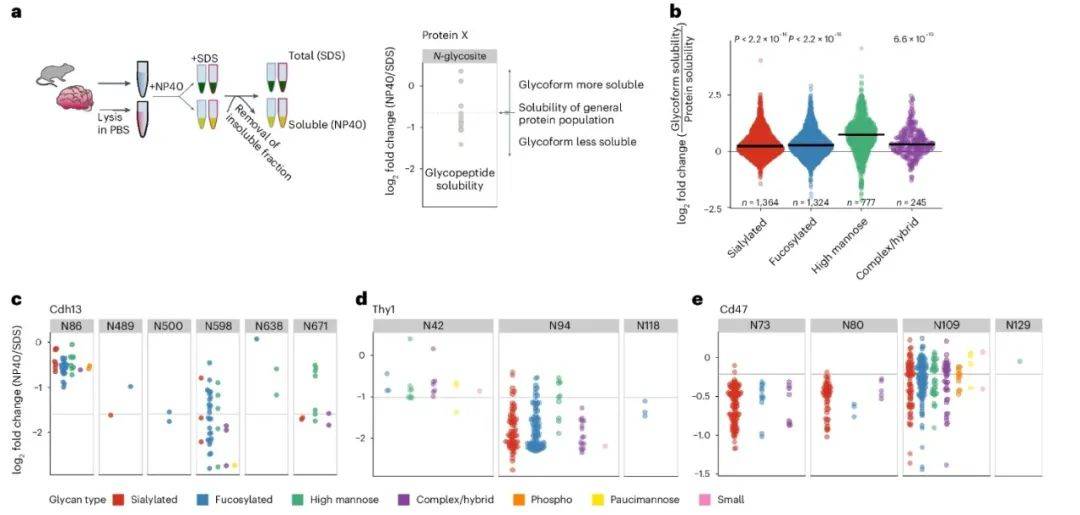 图7 糖型生物物理特性的系统表征
图7 糖型生物物理特性的系统表征
(图源:Potel, et al., Nat Struct Mol Biol, 2025)
肠脑轴新视角:微生物组重塑脑糖蛋白组的分子证据
技术的终极价值在于揭示未知生物学现象。研究团队将DQGlyco推向更复杂的生理场景——肠道菌群如何通过肠脑轴影响宿主?通过对无菌小鼠定植人源菌群,他们发现脑内谷氨酸受体Grin2a的N380位点糖型显著变化,而相邻N443位点却保持稳定(图8k)。这种位点特异性调控提示,菌群可能通过代谢产物(如短链脂肪酸)局部修饰特定糖基转移酶活性。热蛋白质组分析(TPP)提供了更动态的证据。定植菌群后,轴突导向蛋白Cntnap1的热稳定性下降(图8j),提示其糖基化改变导致构象松弛。与此呼应,突触间隙谷氨酸转运体Eaat2的唾液酸化糖型上调(图8n),可能通过增强蛋白溶解度提升神经递质清除效率。这些发现首次将肠道菌群与脑蛋白糖型动态关联,为“菌群-脑”互作提供了分子锚点。
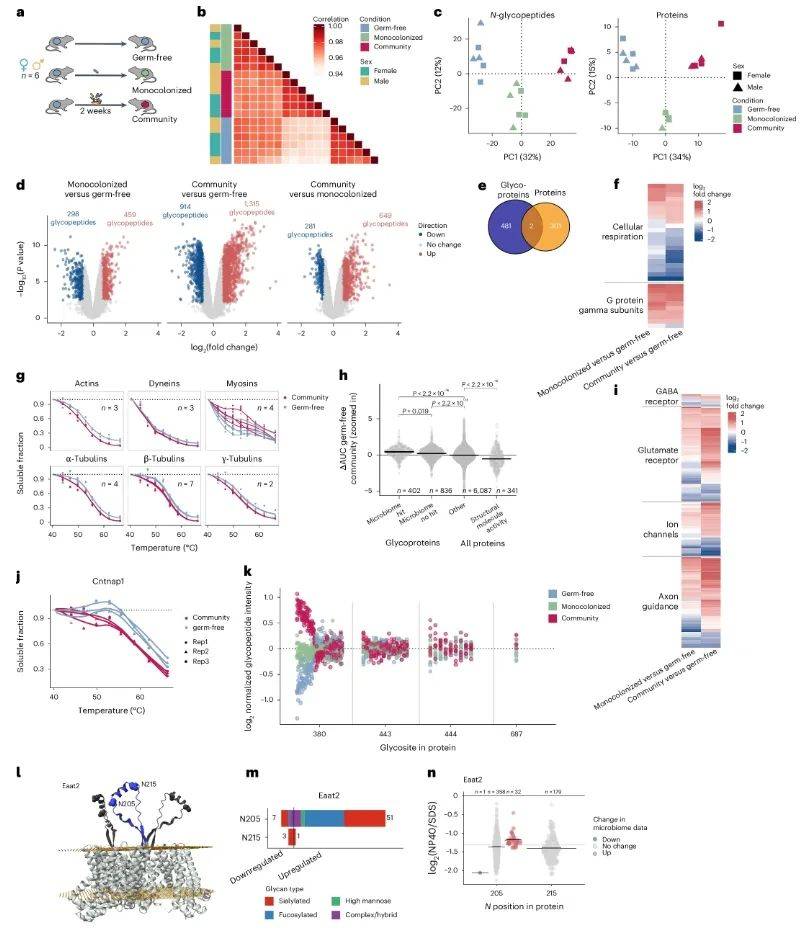 图8 肠道微生物组对小鼠脑糖蛋白组的影响
图8 肠道微生物组对小鼠脑糖蛋白组的影响
(图源:Potel, et al., Nat Struct Mol Biol, 2025)
小结
DQGlyco的诞生标志着糖基化研究从“管中窥豹”迈入“全景扫描”时代。其技术突破不仅在于25倍的鉴定深度提升,更在于首次实现糖型异质性、亚细胞定位与生理功能的跨尺度关联。从理论层面,它揭示了糖基化作为“分子界面”的核心作用——通过微环境感知动态调整蛋白互作网络;从应用层面,该技术为神经退行性疾病、癌症免疫治疗提供了全新的生物标志物筛选平台。
拜谱小结
拜谱作为国内领先的多组学服务公司,可提供蛋白组、修饰组、代谢组、转录组等多组学技术服务。拜谱生物建立了N-糖基化修饰组、O-糖基化修饰组、完整糖肽蛋白质组、唾液酸化修饰组的全体系糖蛋白组学服务,其中完整糖肽产品可以同时进行N-糖和O-糖的定量分析,实现糖基化位点、糖型、糖肽和糖蛋白的完整解析,助力深入挖掘糖基化在疾病发生与发展中的应用。欢迎咨询!
参考文献:
Potel CM, Burtscher ML, Garrido-Rodriguez M, Brauer-Nikonow A, Becher I, Le Sueur C, Typas A, Zimmermann M, Savitski MM. Uncovering protein glycosylation dynamics and heterogeneity using deep quantitative glycoprofiling (DQGlyco). Nat Struct Mol Biol. 2025 Feb 10. doi: 10.1038/s41594-025-01485-w