

间充质干细胞(MSCs)的功能衍生物小细胞外囊泡(sEV)在再生医学中受到了极大的关注和应用。然而,sEV大规模分离的技术限制及其异构性质增加了其应用的复杂性。目前尚不清楚异质性sEVs是否代表MSCs功能的不同方面。
2024年12月,南京医科大学李晶等团队在Journal of Extracellular Vesicles(IF=15.5)上发表了“Distinct molecular properties and functions of small EV subpopulations isolated from human umbilical cord MSCs using tangential flow filtration combined with size exclusion chromatography”的研究论文。该论文提供了一种切向流过滤(TFF)结合尺寸排阻色谱(SEC)的方法来大规模分离和纯化源自人脐带间充质干细胞(HucMSCs)的sEVs亚群。S1-sEVs和S2-sEVs在大小、膜标记蛋白和携带物方面表现出稳定的变化,通过体外实验和动物疾病模型,研究人员验证了S1-sEVs和S2-sEVs的不同功能。S1-sEVs表现出更强的免疫调节作用,而S2-sEVs则在促进细胞增殖和血管生成方面表现出更强的能力。这种方法为针对不同MSCs适应症的靶向治疗干预提供了可能。拜谱生物为该研究提供了蛋白组学检测服务。

英文标题:Distinct molecular properties and functions of small EV subpopulations isolated from human umbilical cord MSCs using tangential flow filtration combined with size exclusion chromatography
发表期刊:Journal of Extracellular Vesicles
影响因子:15.5
发表时间:2024.12.7
作者单位:南京医科大学
组学技术:miRNA测序、蛋白组学(拜谱生物提供)
研究材料:外泌体
研究路线:
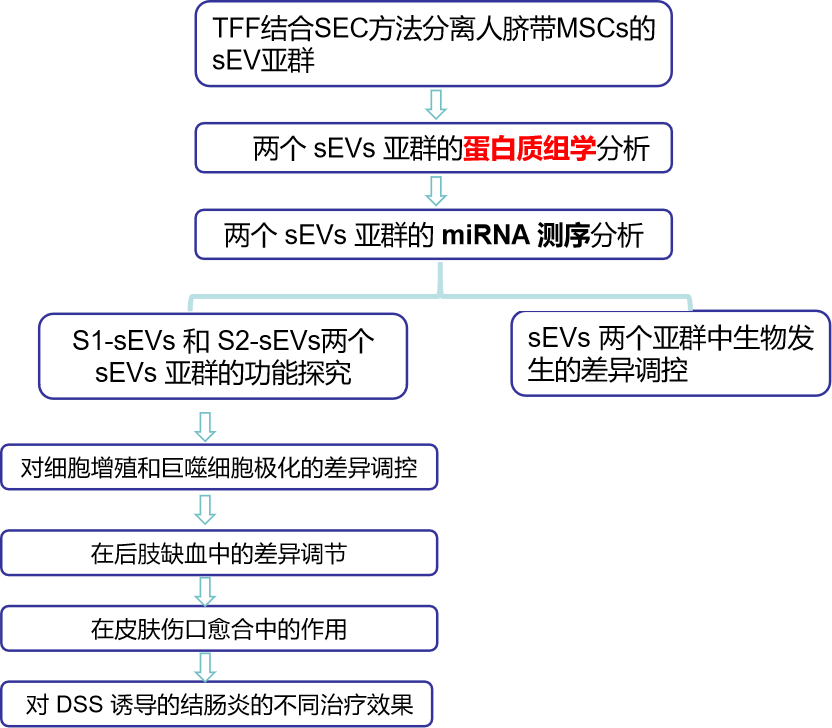
一、研究结果
01、通过将TFF与SEC系统相结合来分离sEVs亚群和HucMSCs
为了实现适合临床应用的MSC-sEVs的大规模生产,作者采用了一种将TFF与SEC相结合的方法,从HucMSCs的条件培养基中分离和纯化sEVs。通过蛋白质印迹、NTA分析、纳流细胞术的结果表明分离的两个峰可能代表了sEVs的两个不同亚群。作者将对应于这两个峰值的sEVs亚群分别命名为S1-sEVs和S2-sEVs(图1)。
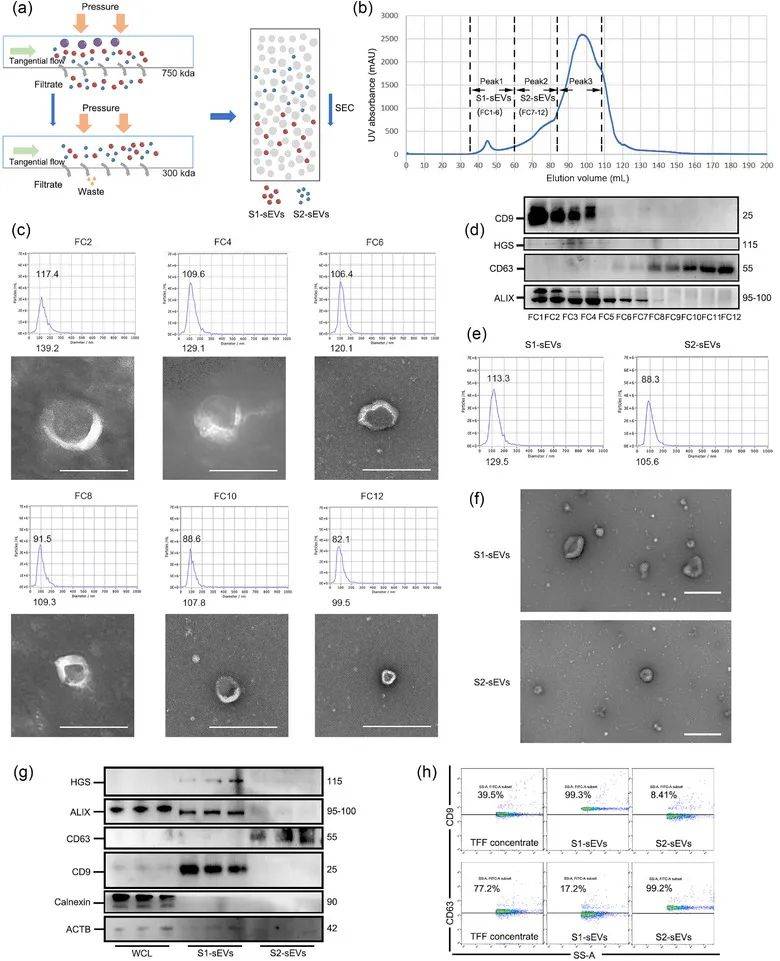 图1:TFF结合SEC系统从HucMSCs中分离和表征sEVs亚群
图1:TFF结合SEC系统从HucMSCs中分离和表征sEVs亚群
(图源:Li J., et al., Journal of Extracellular Vesicles, 2024)
02、MSC-sEVs亚群的表征
sEVs标志物的差异表达意味着它们可能具有不同的内容或功能。为了表征MSC-sEVs亚群的异质性,首先使用蛋白组学分析。总共在S1和S2-sEVs亚群中分别鉴定出1326和1246个蛋白质,其中447个蛋白质在S1-sEVs中高度表达,127个蛋白质在S2-sEVs中富集(图2a)。KEGG分析表明,蛋白酶体途径是S1-sEVs富集蛋白中最富集的通路,而代谢途径在S2-sEVs中显示出最高水平的富集(图2b)。除此之外,还发现S1-sEVs中生长因子受体的富集,例如表皮生长因子受体(EGFR)、肝细胞生长因子受体(HGFR)、成纤维细胞生长因子受体1(FGFR1)等。然而,在S2-sEVs中,枢纽蛋白与代谢、糖酵解和缺氧诱导因子1(HIF-1)信号通路密切相关(图2c-h)。这说明了S1-sEVs和S2-sEVs在靶细胞活动的调节中可能具有不同的作用。
 图2:两个sEVs亚群的蛋白质组学分析
图2:两个sEVs亚群的蛋白质组学分析
(图源:Li J., et al., Journal of Extracellular Vesicles, 2024)
为了探索sEVs亚群中的其他分子,作者进行了miRNA测序,并在S1-sEVs和S2-sEVs中分别鉴定了173和79个miRNA两个sEVs亚群之间的差异表达miRNA,其中在S1-sEVs中发现了113个独特的miRNA,而在S2-sEVs中仅发现了19个miRNA(图3a-b)。通过qRT-PCR验证了在S1-sEVs或S2-sEVs中富集的代表性miRNA,包括let-7b-5p、miR-155-5p、let-7c-5p、miR-9-5p和miR-30d-5p(图3c-g)。在S1-sEVs中,核心节点靶基因包括酪氨酸3-单加氧酶/色氨酸5-单加氧酶激活蛋白zeta(YWHAZ)、BTB结构域和CNC同源物1(BACH1)、丛蛋白D1(PLXND1)、高迁移率组AT-hook1(HMGA1)、SMAD家族成员2(SMAD2)、IL6、IL6R 和转化生长因子β受体1(TGFBR1).在S2-sEVs中,核心节点靶基因被鉴定为PR/SET结构域1(PRDM1)、细胞周期蛋白依赖性激酶抑制剂1A(CDKN1A)、原纤维蛋白2(FBN2)、Notch受体1(NOTCH1)、KLF转录因子6(KLF6)和贝克蛋白1(BECN1)。GO分析显示S1-sEVs组靶基因中与细胞内蛋白质转运、染色质或组蛋白修饰相关的丰富生物过程,而S2-sEVs组靶基因中富含细胞增殖或代谢相关生物过程的负调控(图3h-j)。KEGG通路分析,发现S1-sEVs的miRNAs靶基因在与RNA转运或贴壁连接等相关的信号通路中更富集,而S2-sEVs中的miRNAs靶基因在丝裂原活化蛋白激酶(MAPK)和Wingless/Integrated(WNT)信号通路中更富集(图3k)。
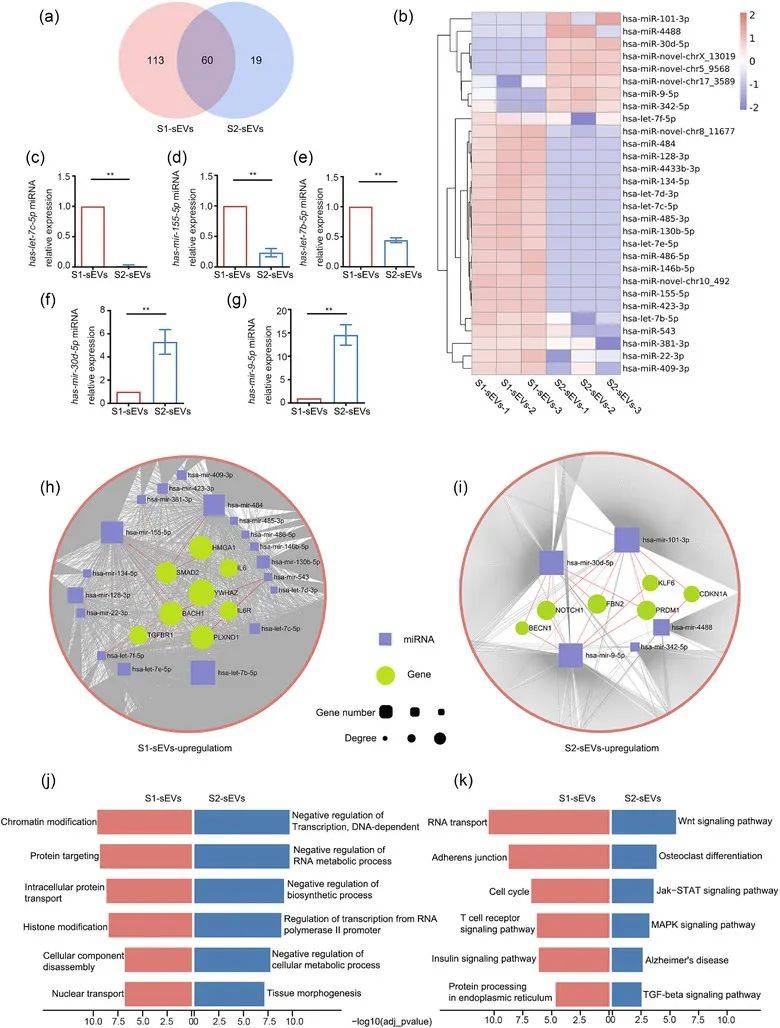 图3:两个sEVs亚群的miRNA谱
图3:两个sEVs亚群的miRNA谱
(图源:Li J., et al., Journal of Extracellular Vesicles, 2024)
03、S1-sEVs和S2-sEVs对细胞增殖和巨噬细胞极化的差异调控
基于两个sEVs亚群的不同携带物组成,研究进一步分用三种不同剂量的S1-sEVs或S2-sEVs培养3T3细胞以及用脂多糖(LPS)处理小鼠骨髓来源的巨噬细胞(BMDMs)。结果发现S1-sEVs和S2-sEVs对细胞生长和分裂速率表现出不同的影响,并且对巨噬细胞极化的能力存在差异(图4a-p)。
 图4:S1-sEVs和S2-sEVs对细胞增殖和巨噬细胞极化的差异调控
图4:S1-sEVs和S2-sEVs对细胞增殖和巨噬细胞极化的差异调控
(图源:Li J., et al., Journal of Extracellular Vesicles,2024)
04、S1-sEVs和S2-sEVs在后肢缺血中的差异调节
MSC及其衍生的sEVs通过促进新血管的形成在后肢缺血治疗中被广泛报道,为了观察S1-sEVs和S2-sEVs对血管生成和缺血组织再生的影响,通过单侧股动脉结扎建立了小鼠后肢缺血模型。结果表明与S1-sEVs相比,S2-sEVs表现出卓越的促血管生成特性,导致缺血诱导损伤后后肢快速完全修复和再生(图5a-o)。
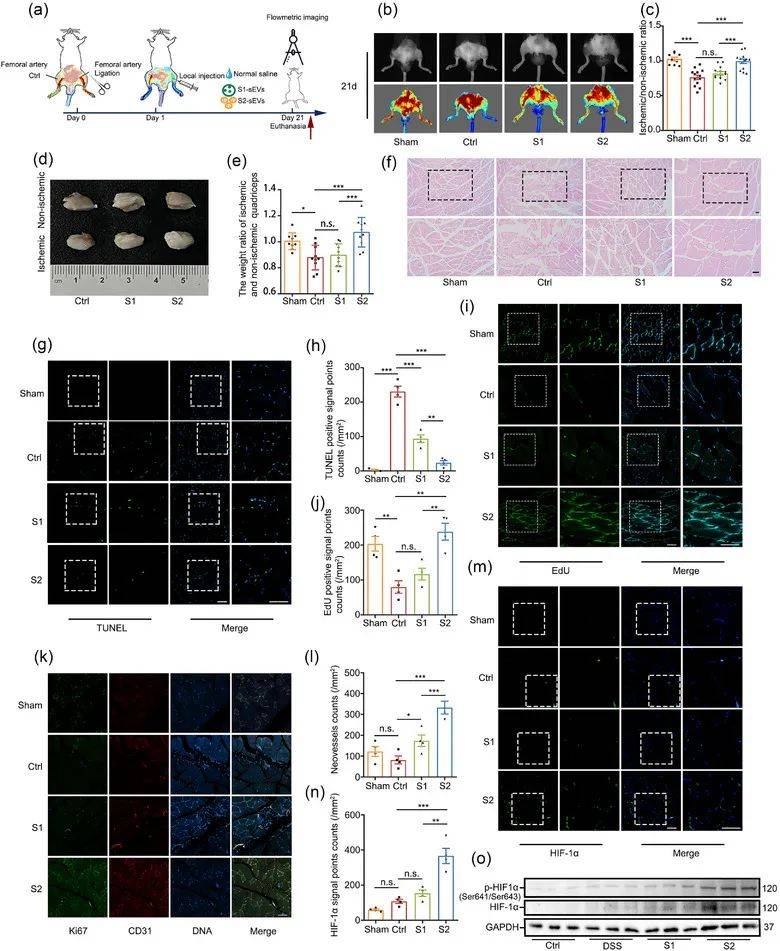 图5:S1-sEVs和S2-sEVs对后肢缺血的不同治疗效果
图5:S1-sEVs和S2-sEVs对后肢缺血的不同治疗效果
(图源:Li J., et al., Journal of Extracellular Vesicles, 2024)
05、S1-sEVs和S2-sEVs在皮肤伤口愈合中的作用
MSC及其衍生的sEV因其在手术、创伤、烧伤或糖尿病疾病引起的皮肤伤口愈合中的作用而被广泛研究。为了观察分离的sEVs亚群对皮肤伤口愈合的影响,本研究建立了一个具有深部2度烧伤的大鼠模型。结果表明S2-sEVs通过对糖酵解的积极影响对皮肤伤口愈合表现出非常有益的影响(图6a-p)。
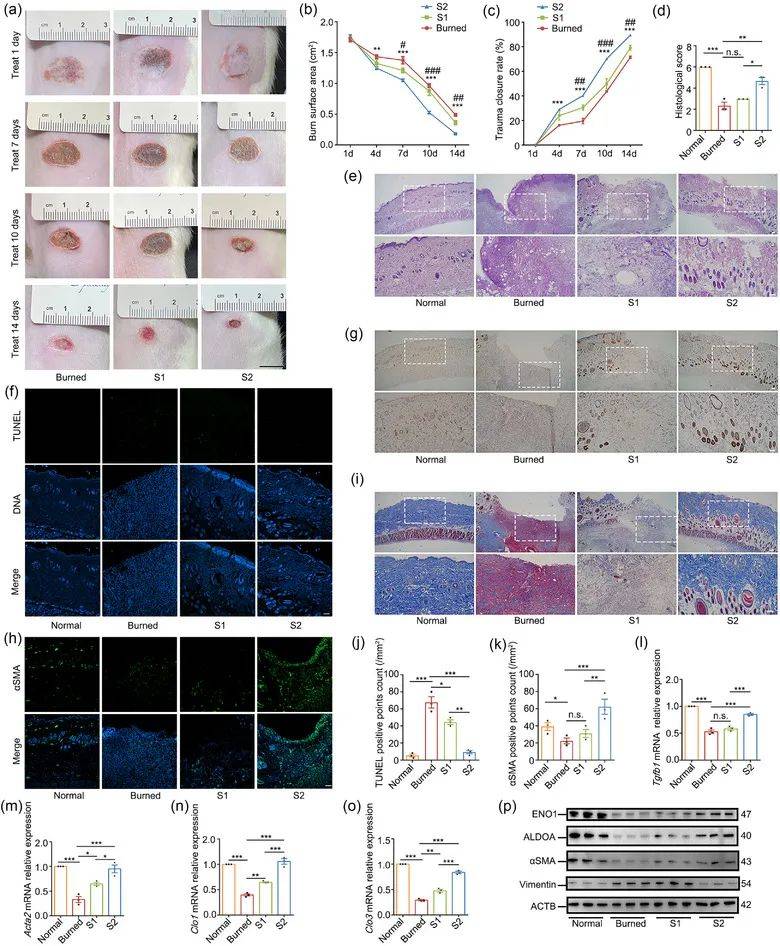 图6:S1-sEVs和S2-sEVs对皮肤伤口愈合的不同影响
图6:S1-sEVs和S2-sEVs对皮肤伤口愈合的不同影响
(图源:Li J., et al., Journal of Extracellular Vesicles, 2024)
06、S1-sEVs和S2-sEVs对DSS诱导的结肠炎的不同治疗效果
作者发现S1-sEVs和S2-sEVs对巨噬细胞极性的差异调节之后,继续在小鼠结肠炎模型中评估它们的免疫调节功能。结果揭示了S1-sEVs治疗DSS诱导的结肠炎的特异性(图7a-s)。
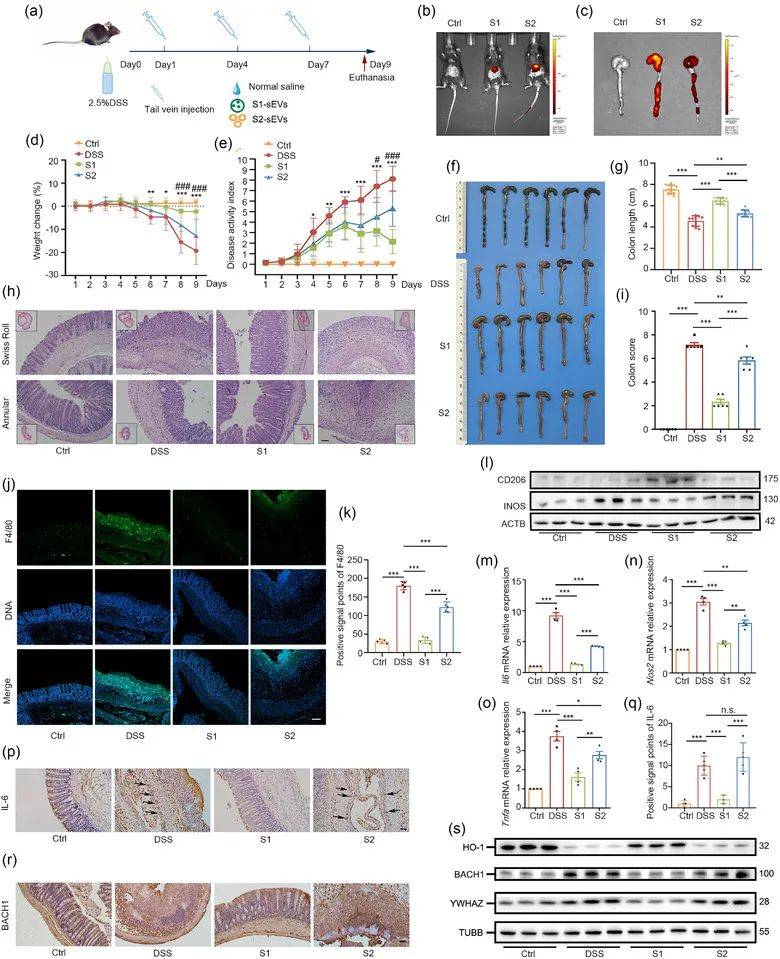 图7:S1-sEVs和S2-sEVs对皮肤伤口愈合的不同影响
图7:S1-sEVs和S2-sEVs对皮肤伤口愈合的不同影响
(图源:Li J., et al., Journal of Extracellular Vesicles, 2024)
07、sEVs两个亚群中生物发生的差异调控
ESCRT依赖性途径和非ESCRT性途径都指导sEV的生物发生。在这项研究中,作者发现了sEVs标志物在S1-sEVs和S2-sEVs中的差异表达。EGFR是经典内吞途径中已建立的HGS底物,尽管在S1-sEVs和S2-sEVs中都可以观察到EGF蛋白,但在S1-sEVs中EGFR泛素化水平要高得多,HGS在将泛素化货物引导到S1-sEVs中起关键作用,通过构建HGS敲除细胞系发现HGS的缺失诱导S1-sEVs的生物发生显着减少,但对S2-sEVs的产生几乎没有影响,表明S1-sEVs和S2-sEVs通过不同的调节机制分泌,分别称为ESCRT依赖性和ESCRT非依赖性途径(图8a-t)。
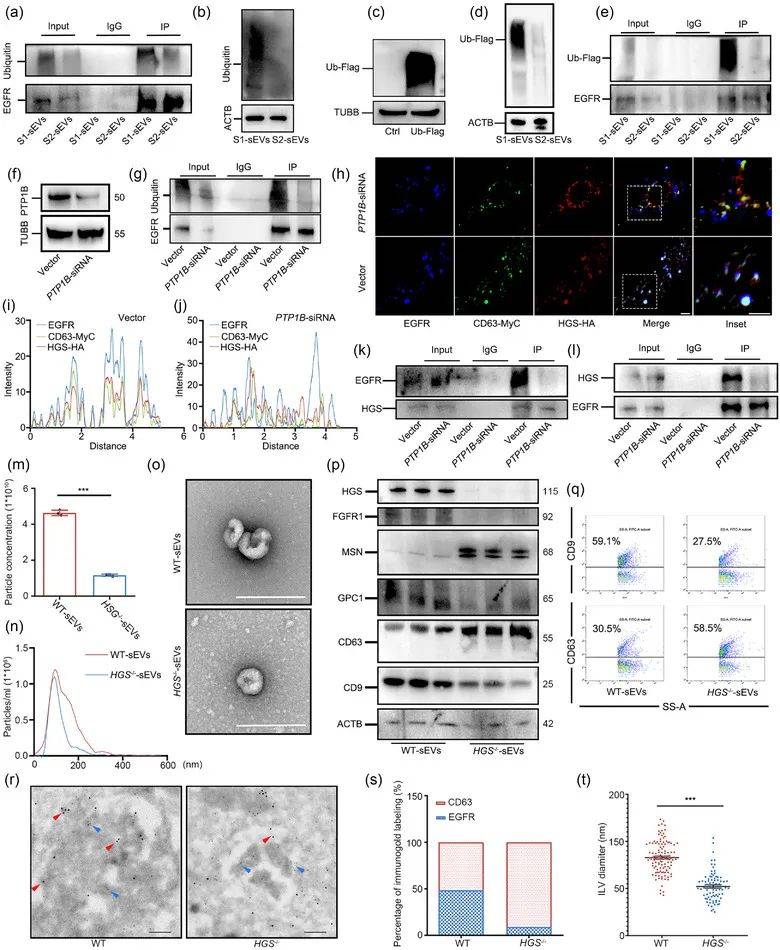 图8:sEVs的两个亚群之间生物发生的差异调节
图8:sEVs的两个亚群之间生物发生的差异调节
(图源:Li J., et al., Journal of Extracellular Vesicles, 2024)
二、文章小结
本研究使用TFF和SEC从人MSC中分离的两个sEV亚群在大小、膜标志物或携带物上表现出差异,并探究不同的sEVs亚群代表了MSCs的不同生物学功能。利用蛋白组学,miRNA测序及基因敲除,模型构建等分子生物学实验表明了高度表达CD9、HRS和GPC1的S1-sEVs表现出更大的免疫调节作用,而富含CD63和FLOT1/2表达的S2-sEVs在促进细胞增殖和血管生成方面具有增强的能力。这些差异归因于它们包含的特定蛋白质和miRNA。进一步研究显示,两个不同的sEVs亚群对应于不同的生物过程:ESCRT通路(S1-sEVs)和以脂质筏(S2-sEVs)为代表的ESCRT非依赖性通路(图9)。这种方法可能为各种MSC适应症的靶向治疗干预提供优势。
 图9:sEVs亚群的生物合成依赖于不同的细胞内途径
图9:sEVs亚群的生物合成依赖于不同的细胞内途径
(图源:Li J., et al., Journal of Extracellular Vesicles, 2024)
三、拜谱小结
该研究使用TFF-SEC系统从人脐带间充质干细胞中规模化生产不同的sEVs亚群,并且鉴定和表征了两种不同的sEVs亚群,S1-sEVs和S2-sEVs,它们在生物发生、特征和携带物含量方面有所不同。这些差异导致了它们生物学功能的变化。虽然MSC衍生的SEV因其临床潜力而备受关注,但该研究引入了一个新概念,即利用这些不同的MSC sEVs亚群对特定疾病进行靶向治疗。拜谱生物为该研究提供了蛋白组学检测分析服务,拜谱生物可提供完善成熟的转录组学、蛋白组学、代谢组学以及多组学联合产品技术服务体系,助力发表高分文献,欢迎致电咨询!
参考文献:
LiuW, Wang X, Chen Y, Yuan J, Zhang H, Jin X, Jiang Y, Cao J, Wang Z, Yang S, Wang B, Wu T, Li J. Distinct molecular properties and functions of small EV subpopulations isolated from human umbilical cord MSCs using tangential flow filtration combined with size exclusion chromatography. J Extracell Vesicles. 2025 Jan;14(1):e70029. doi: 10.1002/jev2.70029. PMID: 39783889; PMCID: PMC11714183