

传统的微生物组研究通常依赖于DNA测序,这种方法的局限性在于缺乏对活性微生物功能的认识。由于许多生物功能发生在蛋白质水平,因此蛋白质组学分析可以更准确地描述活性微生物群落及其与宿主的相互作用。过往的宏蛋白质组通常只关注微生物菌群的蛋白表达特征,而且在物种水平上的蛋白功能分析存在局限性。在整个胃肠道中,膳食成分和长期的膳食模式是宿主肠道黏膜和微生物群功能的核心调节因素。但目前缺少可以同步评估膳食-宿主-微生物组交互作用的研究方法。
2025年1月20日,以色列魏茨曼科学研究所Eran Elinav团队在Cell上发表题目为“Metagenome-informed metaproteomics of the human gut microbiome, host, and dietary exposome uncovers signatures of health and inflammatory bowel disease”的文章,作者建立了以菌群宏基因组、宿主(人或大小鼠)蛋白组、近300种食源物种蛋白组为数据库的宏蛋白质组分析新方法,以此探究了肠道共生菌和致病菌定植、膳食改变以及抗生素扰动过程中的微生物组-宿主相互作用,并精确表征了多种临床和饮食条件下的营养暴露景观图。膳食-肠道菌群-宿主的宏蛋白质组平行评估在功能上揭示了塑造胃肠道生态学的跨界互作组,同时为微生物组相关疾病提供个性化的诊断和治疗见解。
一、研究结果
1、MIM新型宏蛋白质组工作流程和性能测试
宏蛋白质组是基于质谱平台的对微生态样本进行非靶向蛋白质组检测的方法。本研究在传统宏蛋白质组的基础上增添了多物种蛋白参考数据库进行蛋白鉴定和物种归属,蛋白参考数据库包括样本宏基因组测序获得的细菌蛋白数据库、宿主蛋白数据库和近300种食源物种蛋白数据库,命名为metagenome-informed metaproteomics (MIM)(图1)。该方法可以全面的表征肠道内不同物种来源的蛋白表达量和功能,从而对疾病机制、生物标志物、膳食暴露组和小肠功能特征进行跨物种评估。通过与宏基因组和已有的宏蛋白质组进行测试性能比较,MIM宏蛋白质组能准确的实现种水平的功能微生物组表征,同时对宿主肠道分泌蛋白进行全局性评估,因此MIM宏蛋白质组在物种分辨率、活性功能蛋白表征、宿主反应特征方面优于宏基因组和传统的蛋白质组。
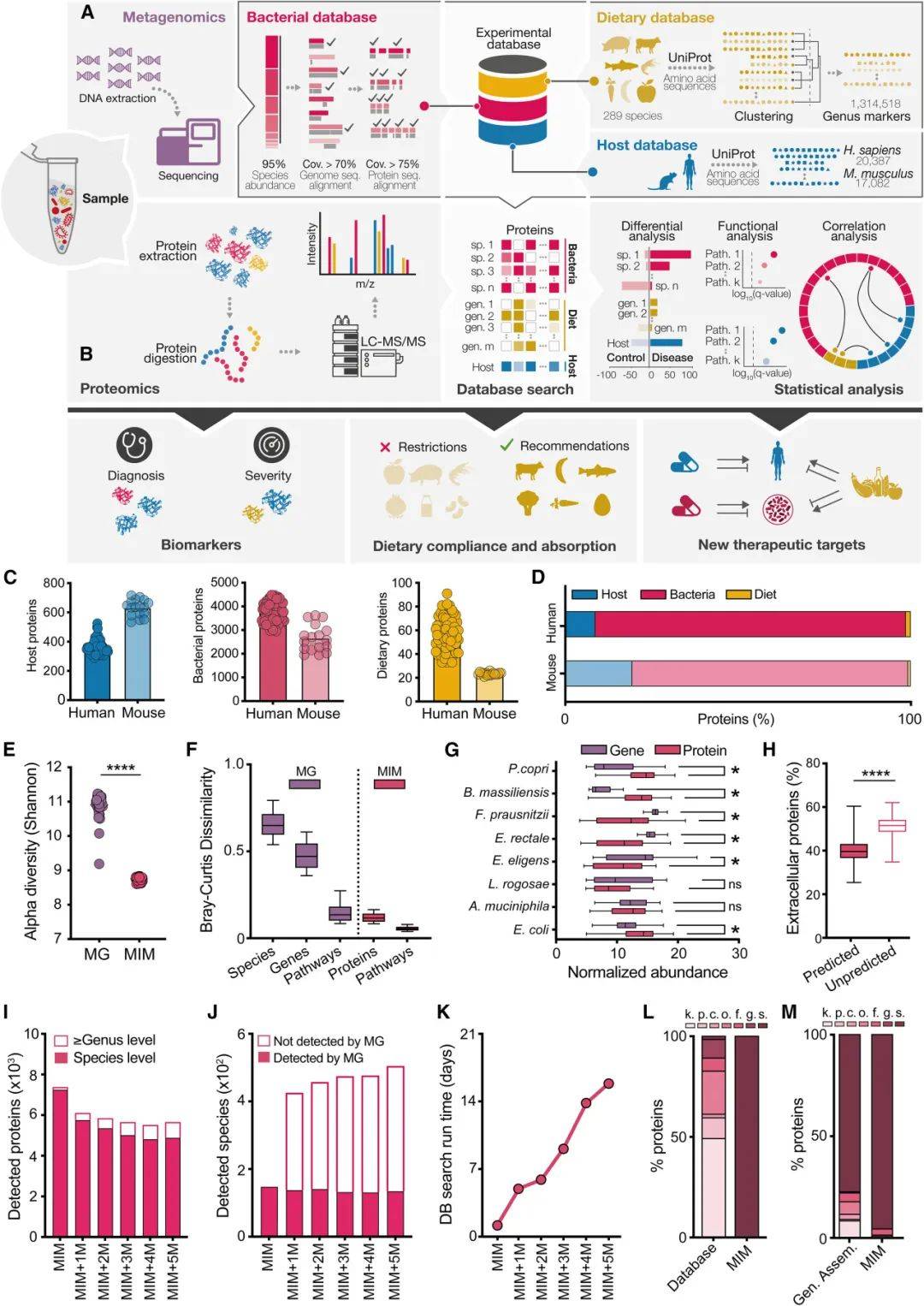 图1 MIM分析流程(图源:Valdes-Mas et al., Cell, 2025)
图1 MIM分析流程(图源:Valdes-Mas et al., Cell, 2025)
2、MIM宏蛋白质组的应用案例
MIM评估消化道系统不同生态位点微生物组-宿主交互作用
作者选取抗生素治疗组和未经治疗组人群消化道位点样本(胃、十二指肠、空肠、末端回肠、盲肠、降结肠和粪便的管腔和粘膜的样本)进行MIM分析。结果显示抗生素治疗组/未经治疗组呈现差异性的微生物分布(图2A)、抗生素耐药蛋白和宿主蛋白特征。不同消化道位点呈现较大差异性,比如微生物蛋白和物种丰度随着消化道远端逐渐增加,抗生素治疗导致微生物蛋白数量的降低(图2B)。接受抗生素治疗的参与者呈现更多样本性的抗生素耐药蛋白,这可能解释了他们在抗生素耐药谱方面具有更明显的个体化改变(图2C)。总的来说,MIM宏蛋白质组全面表征了抗生素治疗对不同生态位点微生物组-宿主蛋白景观,阐述了不同生态位点共生菌定植特征以及宿主蛋白的表达特征。
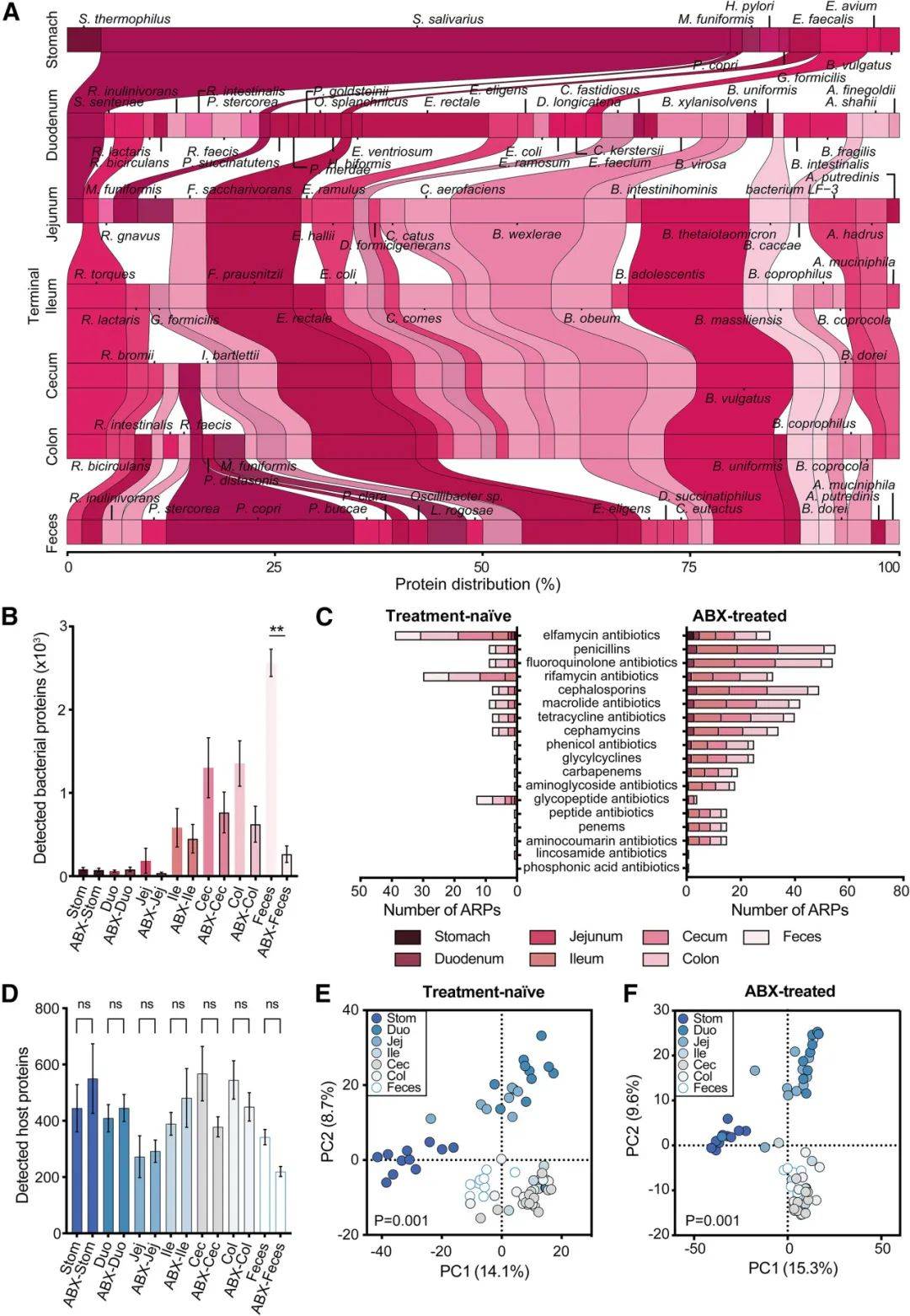 图2 抗生素治疗状态下微生物组-宿主互作的宏蛋白质组景观
图2 抗生素治疗状态下微生物组-宿主互作的宏蛋白质组景观
(图源:Valdes-Mas et al., Cell, 2025)
MIM定量评估膳食蛋白暴露组
以控制饮食的小鼠为对象利用MIM分析不同饮食小鼠的粪便样本宏蛋白质组。纯酪蛋白饮食小鼠中专一性的检出了α-酪蛋白,氨基酸饮食小鼠检测不到食物来源蛋白信号(图3AB),豌豆和大米喂食的小鼠中专一性检出了豌豆和水稻蛋白(图3C),MIM宏蛋白质组也能准确区分麸质饮食和非麸质饮食的小鼠(图3D)。作者在人群样本中同样利用MIM宏蛋白质组定量了膳食暴露组。基于MIM的宏蛋白质组营养评估可以准确捕捉基于人群由饮食习惯文化差异驱动的食物暴露差异。例如,来自以色列 队列(n=54) 和德国人队列 (n=100) 的基于MIM的饮食暴露确定队列检测到两国居民粪便中对含小麦食物的膳食暴露水平相似(图3K)。然而,与以色列人几乎不存在的信号相比,来自德国人的粪便中猪肉相关的信号显著增加(图3L,M)。研究还显示宏基因组的方法无法准确的鉴定饮食暴露组。
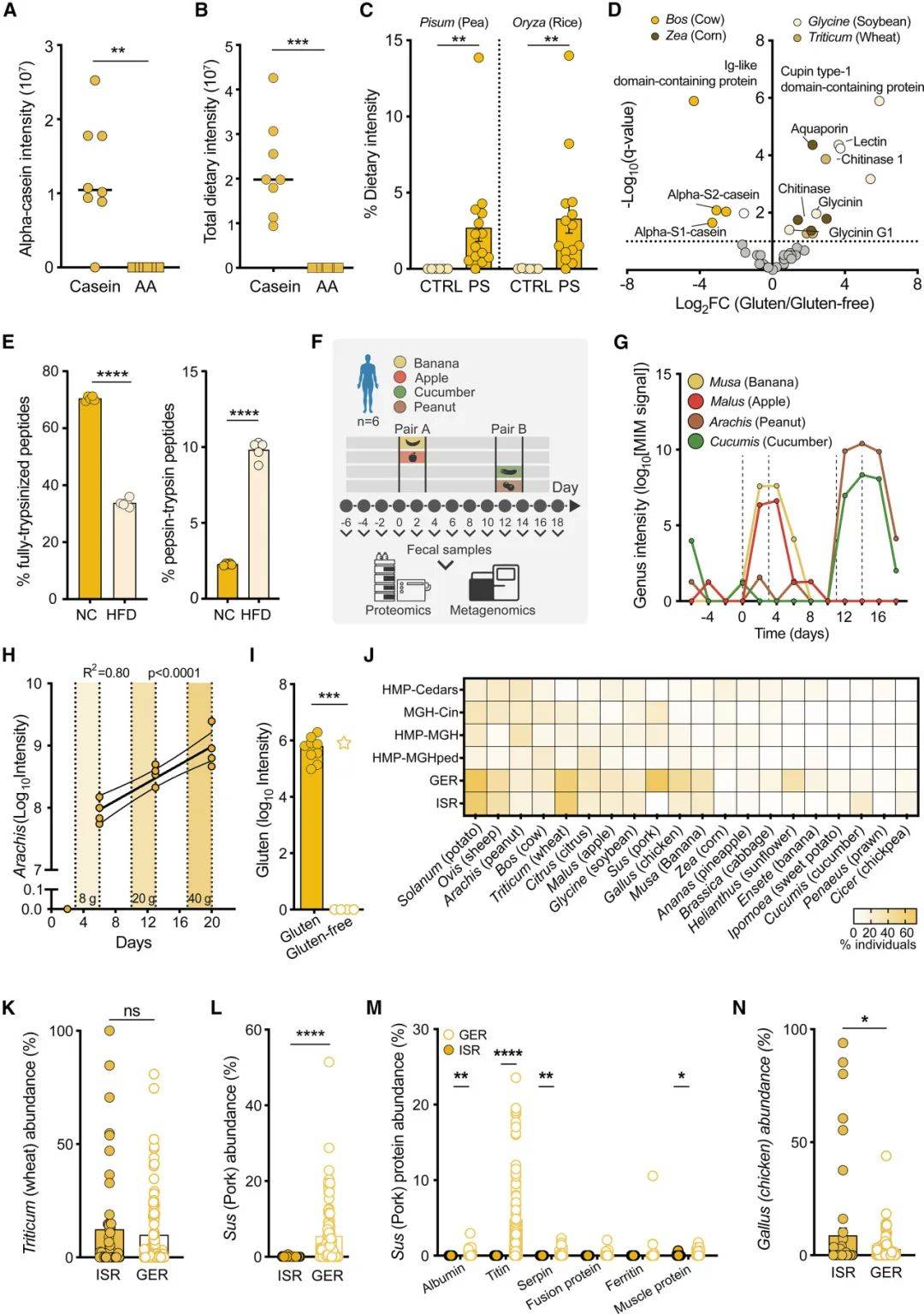 图3 MIM宏蛋白质组准确鉴定小鼠和人膳食蛋白暴露组
图3 MIM宏蛋白质组准确鉴定小鼠和人膳食蛋白暴露组
(图源:Valdes-Mas et al., Cell, 2025)
MIM揭示IBD疾病宿主-共生菌群-饮食交互调节作用
首先作者利用MIM研究了IBD急性炎症小鼠模型中微生物组-宿主-饮食暴露组的纵向动态特征。主要发现以下结果:①MIM表征了炎症进展过程中不同的菌群失调模式,包括“菌群组成失调”和“菌群功能失调”。“菌群组成失调”是以物种对应大部分蛋白上调或下调来衡量的。“菌群功能失调”是指某物种大部分“看家蛋白”表达无差异而其它蛋白发生差异表达。值得一提的是,宏基因组检测结果与MIM宏蛋白质组在某些菌群变化特征上存在差异,这主要是有些基因未发生表达,所以不能检测到相关蛋白。②MIM鉴定了多种宿主分泌的炎症因子蛋白和抗菌肽,且宿主蛋白的表达量随着炎症进展而改变。宿主抗菌肽与微生物菌群相关性分析表明抗菌肽与特定的肠道细菌具有很强的相关性。③饮食蛋白谱分析显示随着炎症进程,粪便中的食物蛋白呈现增加的趋势,这可能由于炎症导致的小肠消化吸收功能受损。
接着作者利用MIM探究了IBD患者中微生物-宿主交互作用。在克罗恩病患者队列中(n=26/28),粪便样本MIM宏蛋白质组分析显示两组蛋白组有显著差异(PCA分析,图4AD),物种水平的细菌蛋白功能富集到Bacteroides vulgatus的糖原降解和鞘脂代谢等通路(图4B),宿主差异蛋白富集到免疫相关通路(图4F)。在另一个溃疡性结肠炎队列中(n=50/50),MIM分析显示细菌和宿主蛋白组均显著差异(图4GI),细菌差异蛋白富集到Segatella copri的烟酰胺代谢通路,宿主蛋白与免疫和抗病原物反应相关(图4HK)。研究显示MIM宏蛋白质组获得的差异蛋白在IBD诊断方面优于宏基因组获得差异基因(图4L)。
最后利用MIM评估了膳食在IBD进展中的作用。在EEN饮食干预的IBD患者中(n=7)发现膳食蛋白数量的下降,且膳食蛋白数量与炎症标志物S100A9呈现正相关性,表明MIM方法可以对EEN饮食干预或肠道炎症进行量化。作者在更多的IBD队列中利用MIM方法评估和膳食蛋白与疾病的关系,发现在IBD患者中膳食蛋白丰度显著高于健康对照,可能是小肠吸收不良导致粪便中膳食蛋白质的积累。
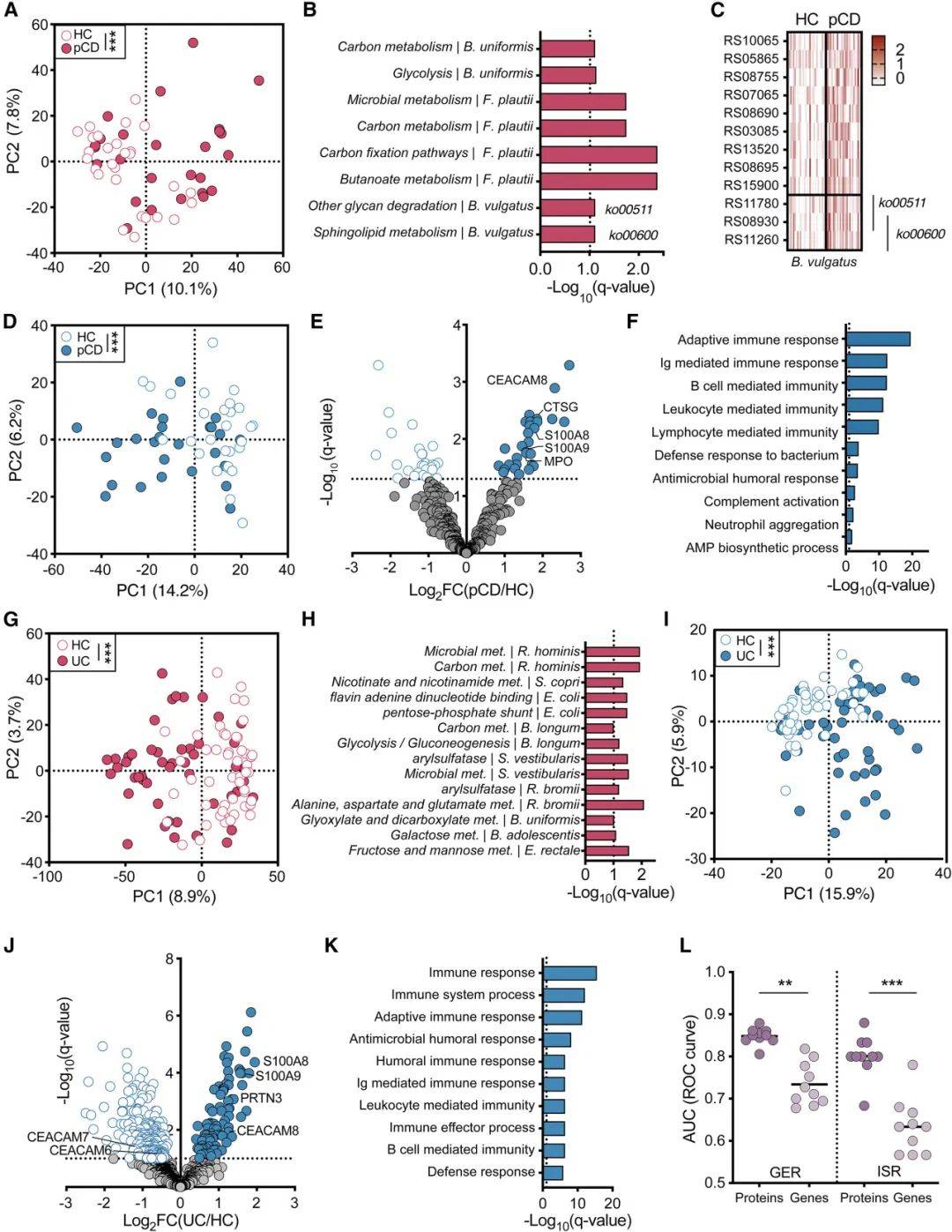 图4 MIM宏蛋白质组分析IBD患者粪便样本蛋白表达和功能分析
图4 MIM宏蛋白质组分析IBD患者粪便样本蛋白表达和功能分析
(图源:Valdes-Mas et al., Cell, 2025)
MIM宏蛋白质组发现潜在的IBD生物标志物
以HMP-MGH队列(溃疡性结肠炎=12,克罗恩病=34,健康对照=52)和HMP-Cin队列(溃疡性结肠炎=29,克罗恩病=48,健康对照=45)为对象,MIM分析筛选差异蛋白,利用机器学习(随机森林)建立分类器,选择top50候选标志物在独立验证队列中进行验证,再次利用随机森林评估预测性能。最后发现肠道细菌和宿主蛋白的组成的panel具有较好的预测性能。另外,作者还利用MIM筛选了能预测IBD疾病进展程度的生物标志物。研究显示MIM筛选获得的生物标志物的诊断性能优于已有的标志物S100A8和S100A9。
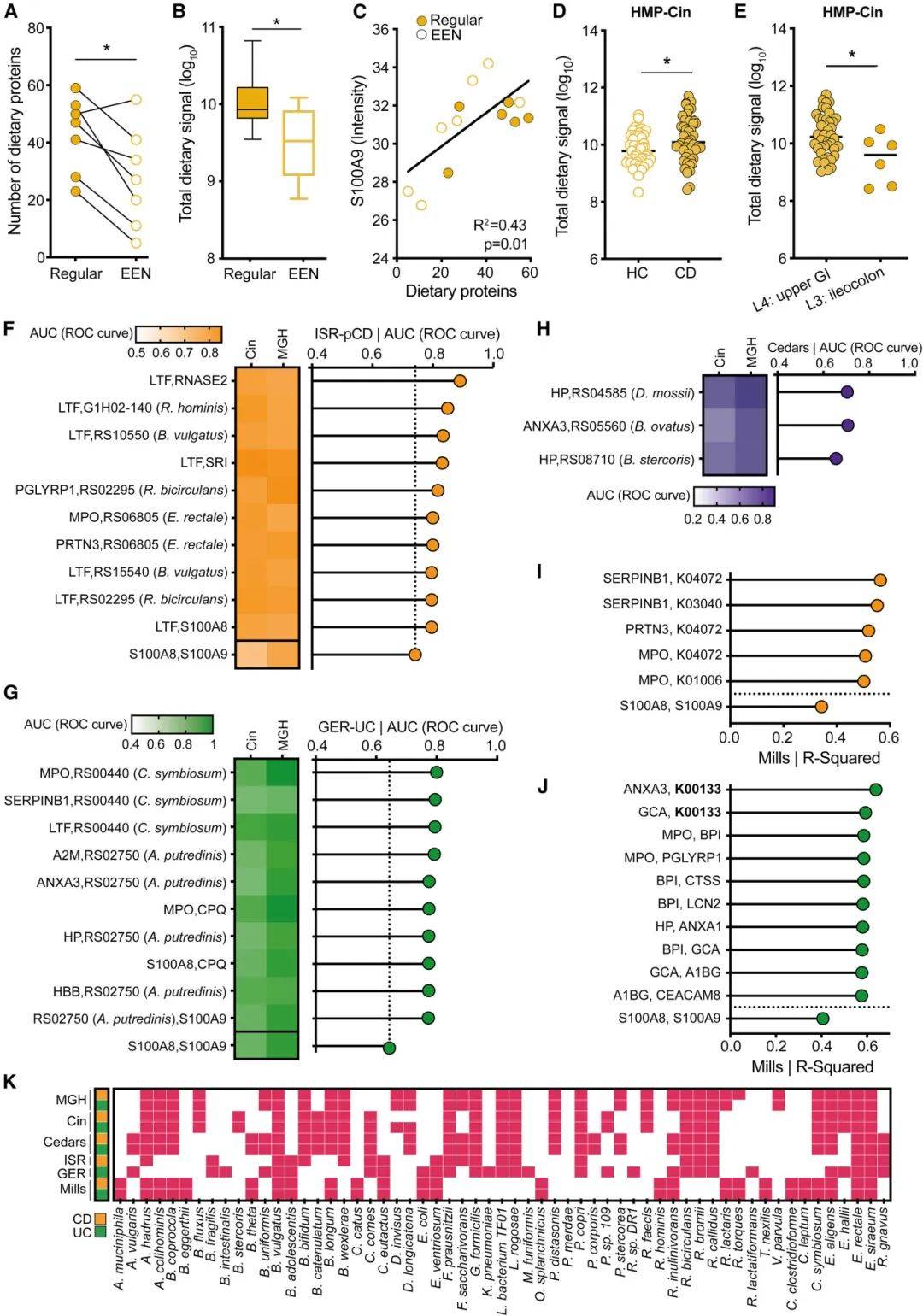 图5 MIM宏蛋白质组筛选IBD生物标志物
图5 MIM宏蛋白质组筛选IBD生物标志物
(图源:Valdes-Mas et al., Cell, 2025)
二、小结
综上, 本研究介绍了一种全面新型的宏蛋白质组研究流程。该方法具有以下优势:(1)直接检测具有活性的微生物菌群及其功能,而且能对活性蛋白进行种水平的归属,这有助于发现微生物组扰动的直接驱动因素(菌群或蛋白)。(2)能表征宿主来源蛋白特征,从而研究宿主对微生物组的反应以及宿主-微生物组的互作。(3)蛋白质相对比较稳定,是生物标志物的主要来源,因此宏蛋白质组更适用于发现疾病诊断、监测和预后的生物标志物。(4)能定量消化道系统中的膳食蛋白,从而研究饮食对宿主-微生物组互作的影响,且能评估消化道特别是小肠的营养吸收功能。
三、拜谱小结
拜谱生物作为国内领先的多组学技术服务公司,可提供完善成熟的蛋白质组学、修饰蛋白质组学、代谢组学、转录组学等多组学产品技术服务体系。围绕微生物研究,拜谱生物建立了16s、宏基因组、宏转录组、宏蛋白组等全方位“宏组学”检测服务体系。其中拜谱生物 “深度宏蛋白质组”,通过尖端Astral质谱平台对微生物组的蛋白质进行高通量定性和定量分析,实现万级超高深度蛋白鉴定,并提供菌群注释、蛋白定量分析、蛋白功能注释、差异蛋白分析和高级分析等丰富的生信分析结果,助力揭示复杂样本中微生物种群与共生协作关系。深度宏蛋白质组学可以把微生物群落的菌群信息和功能信息进行关联,揭示群体中发挥关键作用的微生物和与其相关的蛋白质功能,在“肠脑轴”、发病机制研究、生物标志物研究等多领域具有广泛的应用。欢迎咨询!
参考文献:
Rafael Valdés-Mas, Avner Leshem, Danping Zheng,et al. Metagenome-informed metaproteomics of the human gut microbiome, host, and dietary exposome uncovers signatures of health and inflammatory bowel disease, Cell, 2025, doi.org/10.1016/j.cell.2024.12.016