

肺动脉高压(PAH)是一种危害严重的心肺疾病,它的特点在于病情会逐渐加重,伴随着明显的症状,并且在病情持续发展下可能会致命。PAH的主要病理特征是肺动脉的结构发生改变,同时血液循环的动力学也出现异常。尽管在过去十年中,PAH的治疗取得了显著进展,但诊断延迟和治疗效果不理想仍然是实现最佳结果的主要障碍。PAH的发病机制复杂,涉及多种病理生理过程,其中炎症和代谢紊乱的作用逐渐受到关注。
2025年1月23日美国匹兹堡大学Stephen Y. Chan的教授团队在Science杂志(IF:44.7)上发表了题为“Lysosomal dysfunction and inflammatory sterol metabolism in pulmonary arterial hypertension”的研究文章,该研究探究了溶酶体功能障碍和炎症性类固醇代谢与PAH之间的联系。研究发现,核受体辅激活因子7(NCOA7)在炎症性PAH下会被上调,它通过调节溶酶体酸化和类固醇代谢来抑制内皮细胞炎症。而NCOA7基因中的单核苷酸多态性rs11154337与PAH严重程度和死亡率相关,其G等位基因可以增加NCOA7表达,降低炎症,改善PAH。基于这些发现,研究人员开发了一种NCOA7激活剂,可以逆转内皮细胞炎症和动物PAH,为PAH的诊断和治疗提供了新的思路。

流程图
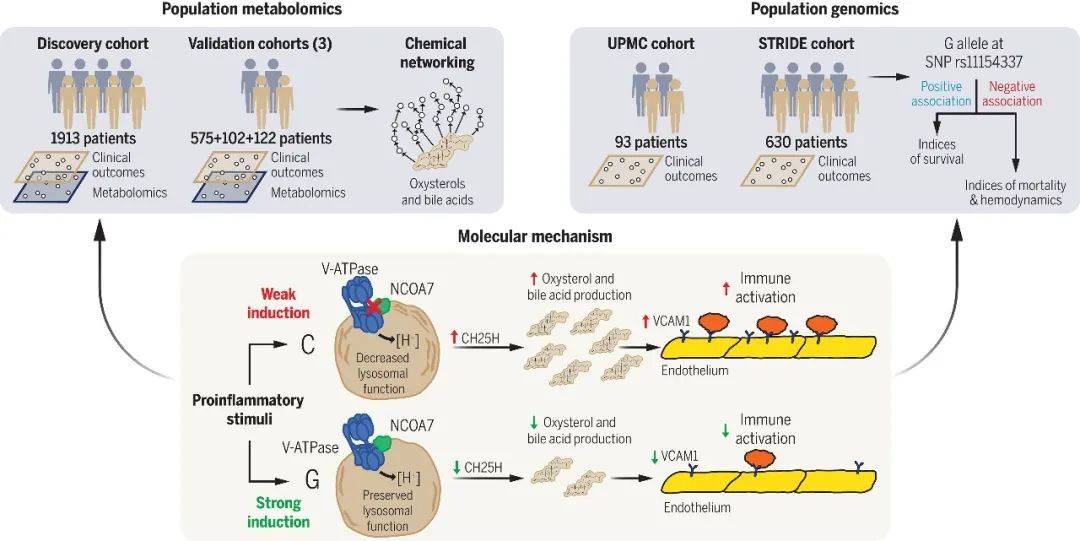 图1流程图(图源:Harvey, et al., Science, 2025)
图1流程图(图源:Harvey, et al., Science, 2025)
探究NCOA7与溶酶体功能的关系
研究团队研究了NCOA7在溶酶体功能中的关键作用。他们首先对暴露于IL-1β的人肺动脉内皮细胞进行了无偏转录组分析,并利用携带组成型肺IL-6表达的转基因小鼠和慢性缺氧小鼠模型,研究NCOA7在PAH中的作用。此外,他们对PAH患者的肺组织进行了单细胞RNA测序分析。研究发现,促炎症因子IL-1β和IL-6均能上调NCOA7的表达,而缺氧对其表达的影响较小。在小鼠和人类的PAH模型中,NCOA7的表达在血管壁中显著升高,尤其是在内皮细胞中。NCOA7的抑制导致溶酶体功能障碍,表现为V-ATPase亚基表达下调、溶酶体酸化减弱、溶酶体酶活性降低和溶酶体肥大。NCOA7缺陷还导致脂质在溶酶体中积累,并上调胆固醇25-羟化酶(CH25H)的表达,从而增加氧化胆固醇和胆汁酸的产生。这表明,NCOA7在促炎症状态下作为稳态制动器,通过维持溶酶体功能和类固醇代谢来抑制内皮细胞的免疫激活,从而减轻PAH。
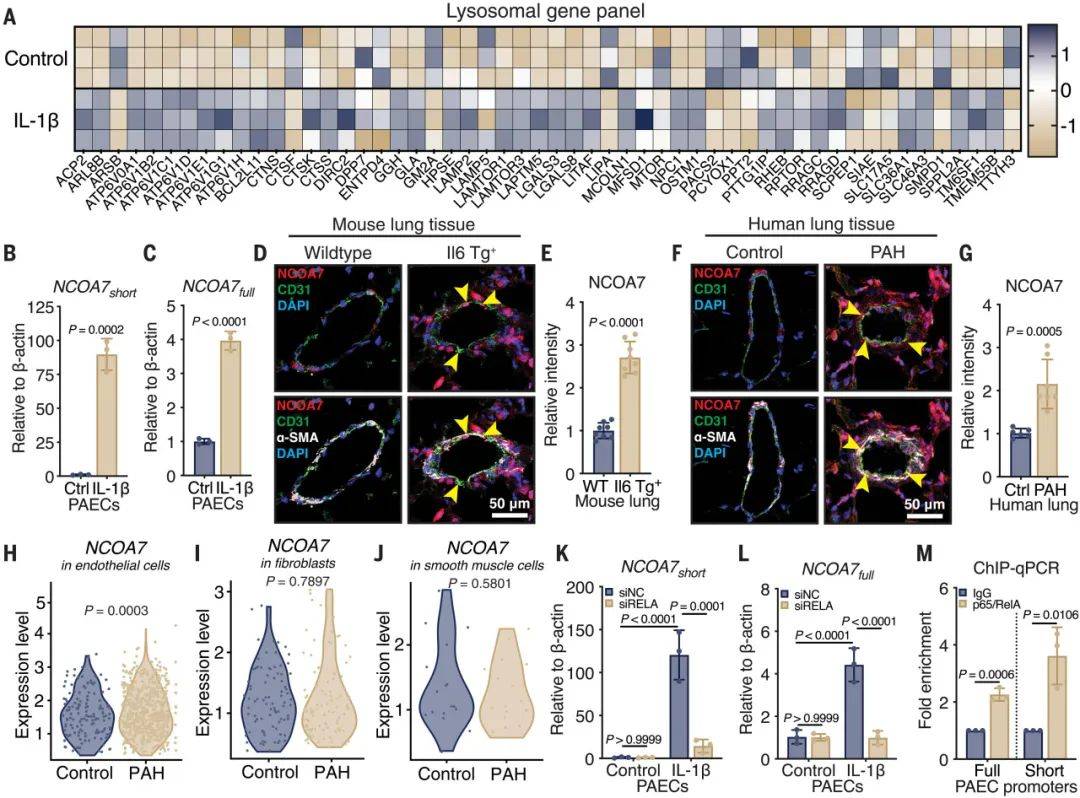 图2 NCOA7在PAH的细胞、动物和人类实例中的聚合炎症调节
图2 NCOA7在PAH的细胞、动物和人类实例中的聚合炎症调节
(图源:Harvey, et al., Science, 2025)
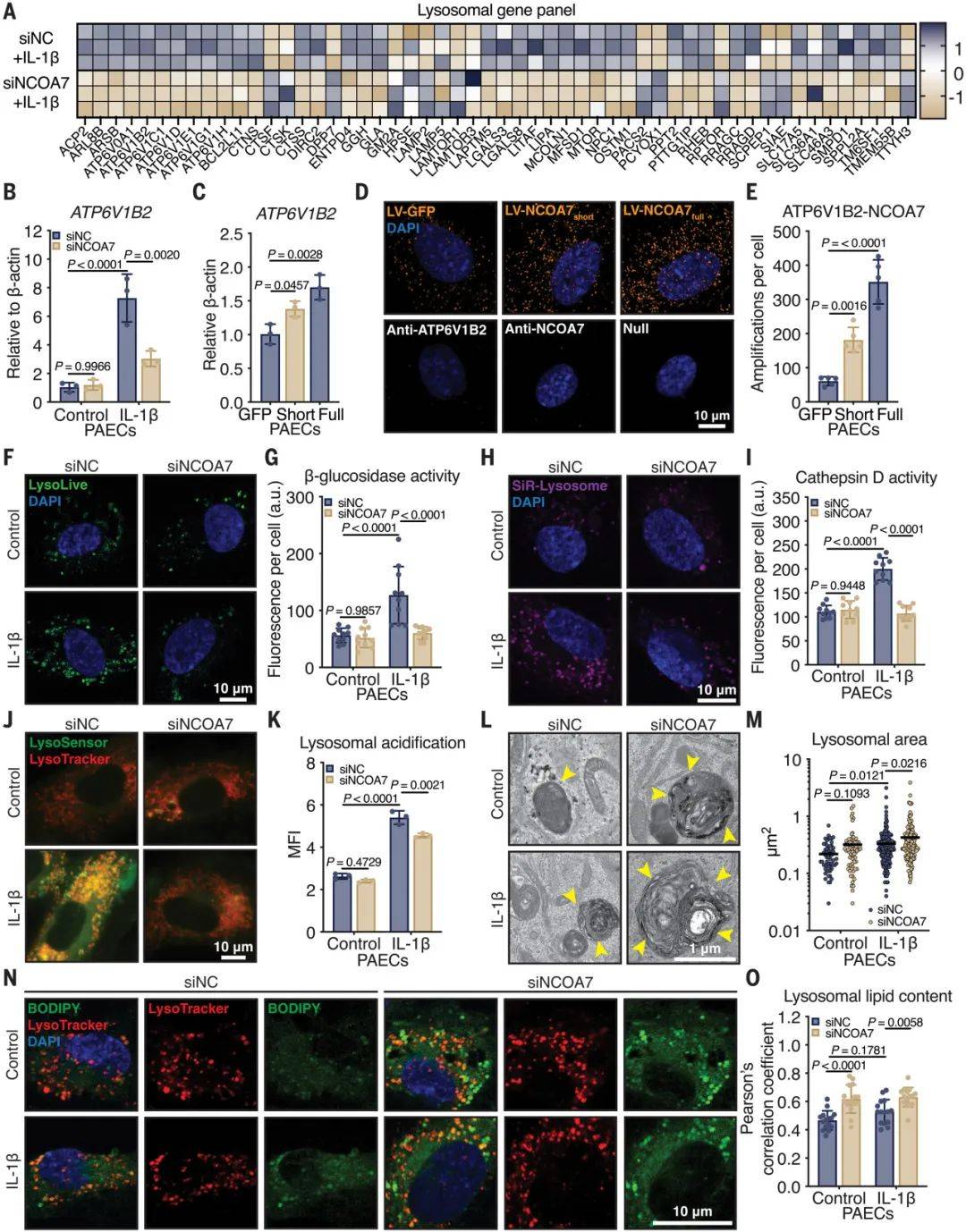 图3 在促炎条件下,NCOA7缺乏会导致溶酶体功能障碍和脂质积聚
图3 在促炎条件下,NCOA7缺乏会导致溶酶体功能障碍和脂质积聚
(图源:Harvey, et al., Science, 2025)
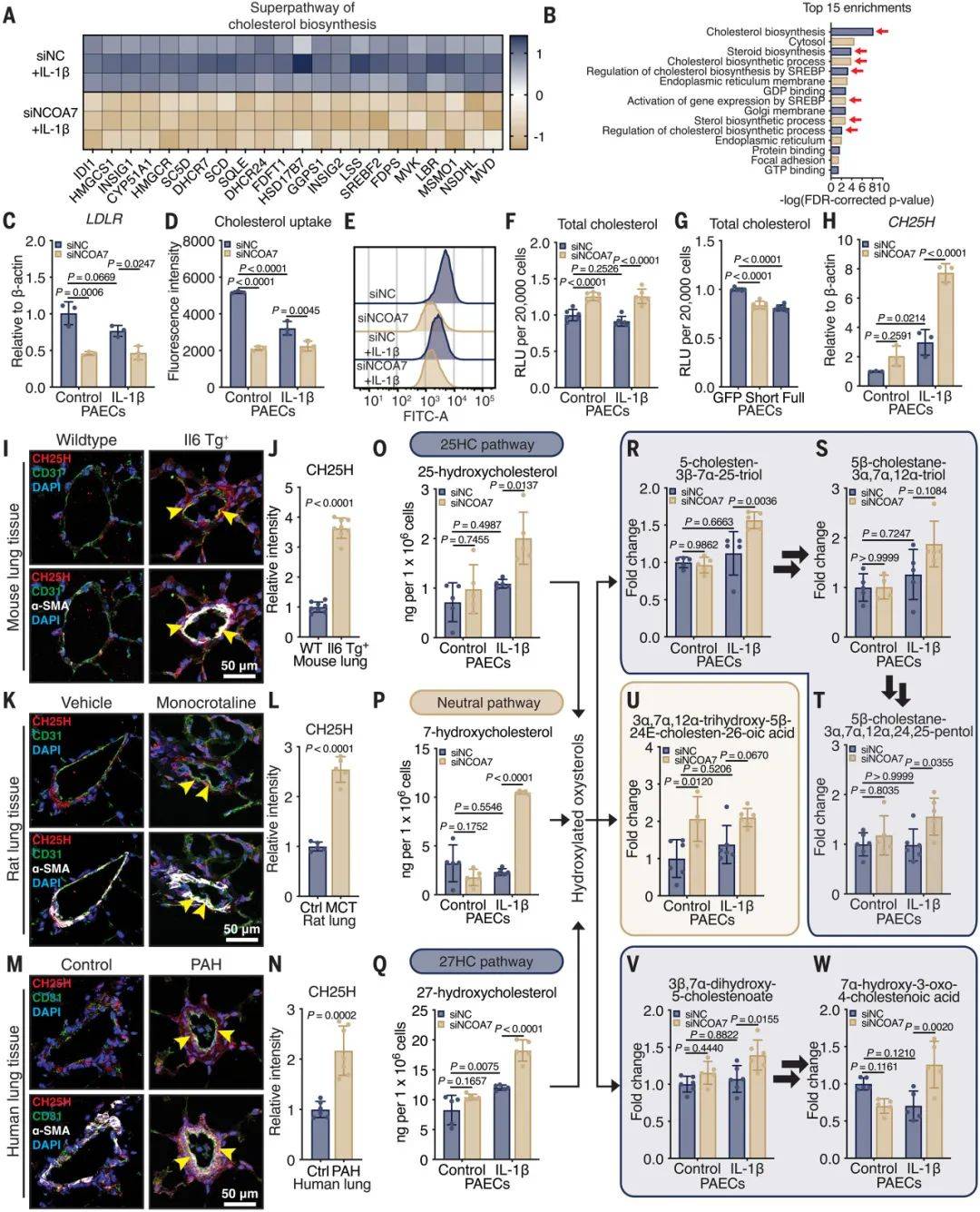 图4 NCOA7缺乏会重新编程甾醇代谢,以上调氧甾醇和胆汁酸
图4 NCOA7缺乏会重新编程甾醇代谢,以上调氧甾醇和胆汁酸
(图源:Harvey, et al., Science, 2025)
验证NCOA7与EC功能障碍的关系
研究团队深入探究了NCOA7缺陷是否通过产生氧化胆固醇和胆汁酸来促进肺血管内皮细胞功能障碍。他们的研究目的是验证NCOA7缺陷是否通过这一机制促进EC功能障碍。为了实现这一目标,研究团队采用了多种方法。首先,他们使用 靶向脂质组学分析检测了NCOA7缺陷PAECs中的氧化胆固醇和胆汁酸水平。此外,他们使用荧光染料和免疫荧光染色检测了EC的免疫激活和白细胞粘附。在培养的PAECs中,他们直接添加了胆汁酸,并检测了其免疫激活作用。研究结果发现,NCOA7缺陷导致氧化胆固醇和胆汁酸的产生增加。NCOA7缺陷增强IL-1β诱导的血管细胞粘附分子1(VCAM1)表达,促进白细胞粘附。胆汁酸,特别是7α-羟基-3-氧-4-胆固醇烯酸(7HOCA),直接激活EC,增加VCAM1表达并促进白细胞粘附。这意味着NCOA7缺陷通过产生氧化胆固醇和胆汁酸来促进EC功能障碍和免疫激活。
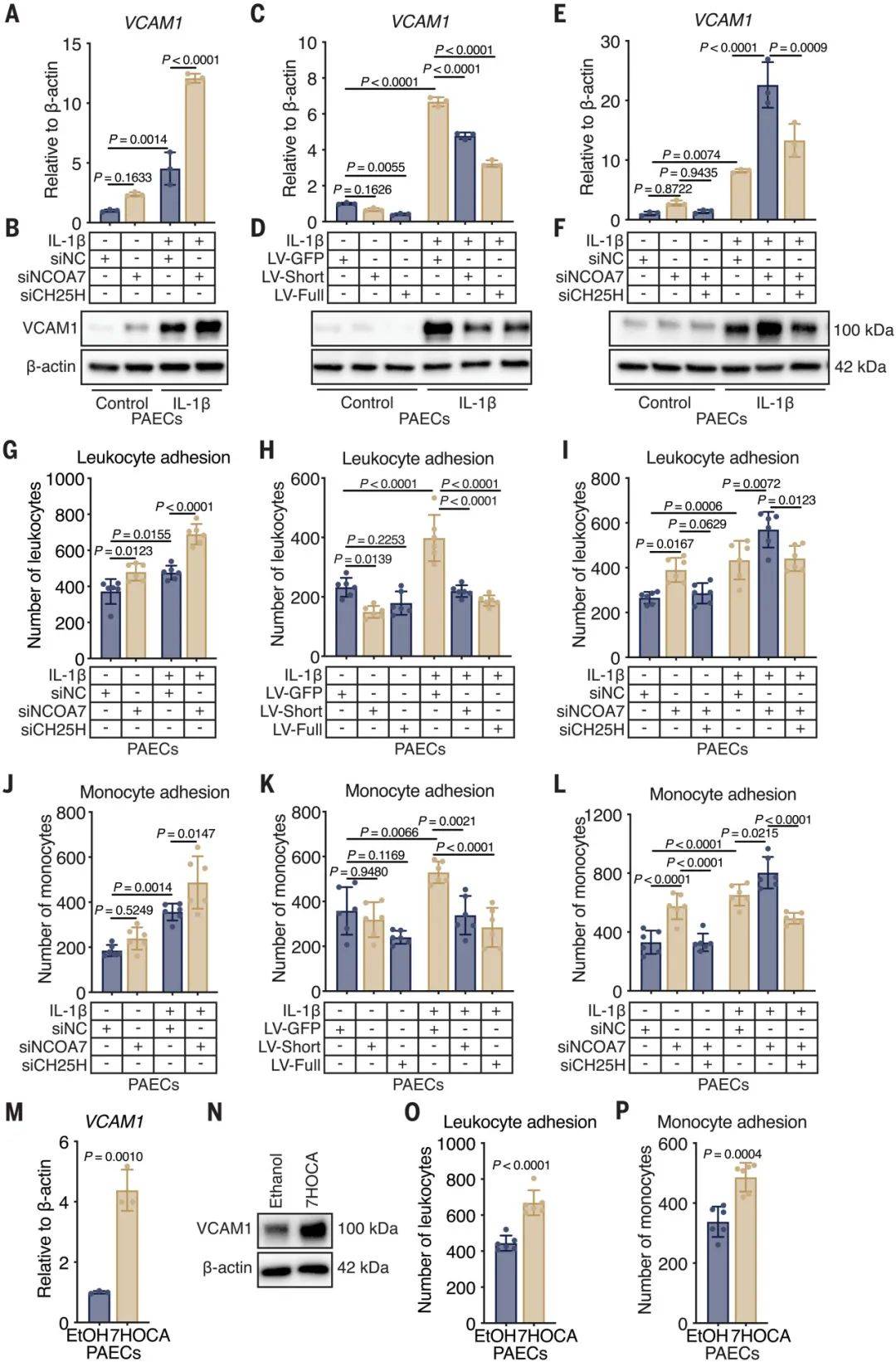 图5 NCOA7-CH25H 轴驱动肺内皮免疫激活
图5 NCOA7-CH25H 轴驱动肺内皮免疫激活
(图源:Harvey, et al., Science, 2025)
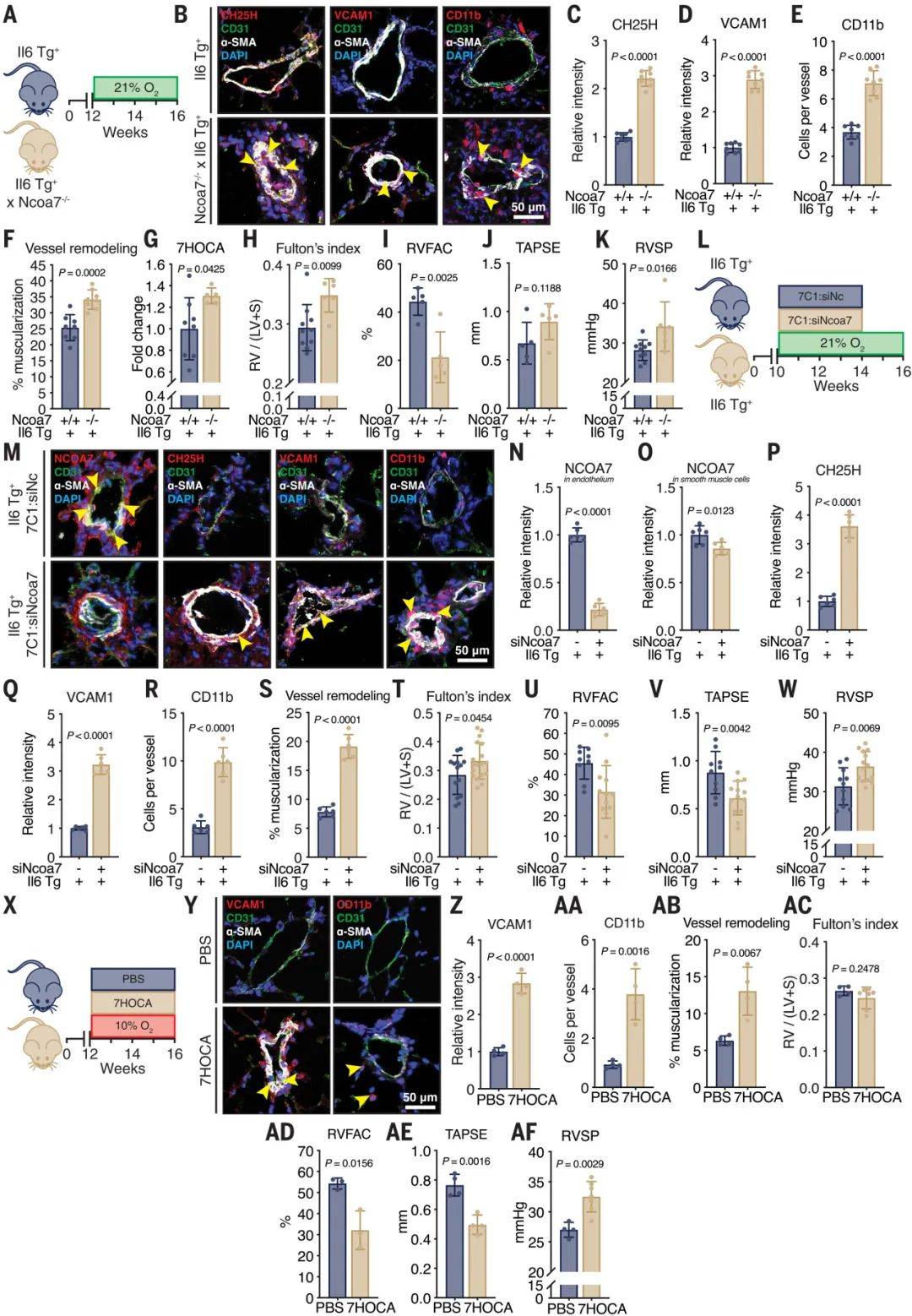 图6 Ncoa7基因缺失和气管内输送7HOCA会加重PAH的病情
图6 Ncoa7基因缺失和气管内输送7HOCA会加重PAH的病情
(图源:Harvey, et al., Science, 2025)
探究NCOA7与PAH的关系
研究团队深入探究了NCOA7缺陷是否与PAH的严重程度和死亡率相关。为了实现这一目标,研究团队采用了多种方法。首先,他们进行了代谢组学和基因组学的关联研究,识别了与PAH严重程度和死亡率相关的血浆代谢物。此外,他们分析了来自UPMC和STRIDE临床试验的PAH患者队列中的SNP rs11154337的基因型。对SNP rs11154337的C/C基因型携带者进行了iPSC-ECs分化,并分析了NCOA7表达、溶酶体活性、氧化胆固醇和胆汁酸产生以及EC免疫激活。研究结果发现,与PAH严重程度和死亡率相关的血浆代谢物中,包括NCOA7依赖的氧化胆固醇和胆汁酸。SNP rs11154337的G等位基因与UPMC和STRIDE队列中PAH患者的生存率提高相关。在iPSC-ECs中,G等位基因增加NCOA7表达,促进溶酶体酸化,减少氧化胆固醇和胆汁酸的产生,并抑制EC免疫激活。由此可以得知NCOA7缺陷与PAH的严重程度和死亡率相关,而SNP rs11154337的G等位基因可以增强NCOA7表达,从而减轻PAH。
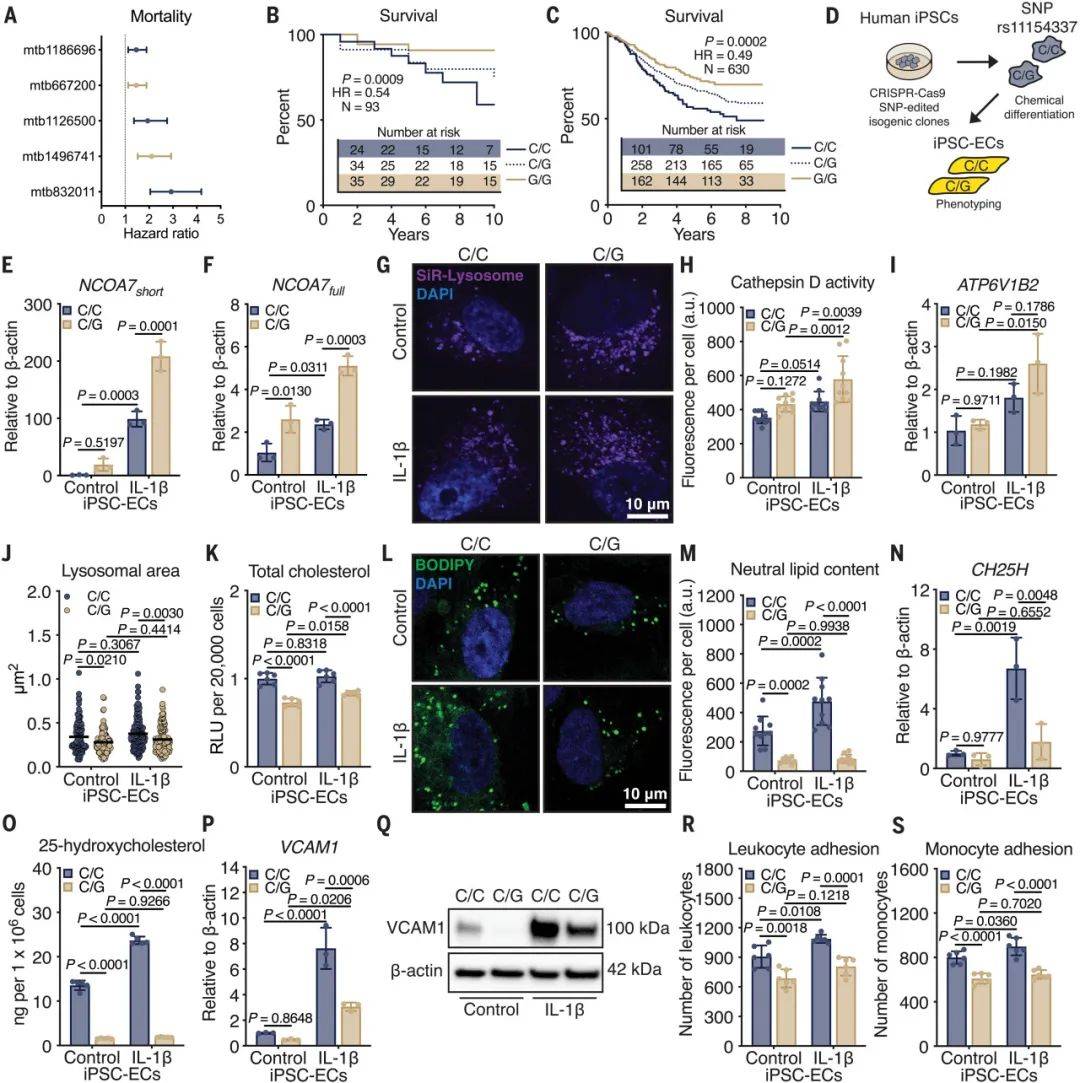 图7 SNP rs11154337的G等位基因可防止溶酶体脂质积聚,并减弱iPSC EC中氧固醇介导的免疫激活
图7 SNP rs11154337的G等位基因可防止溶酶体脂质积聚,并减弱iPSC EC中氧固醇介导的免疫激活
(图源:Harvey, et al., Science, 2025)
探究NCOA7激活剂的潜在治疗作用
最后,研究团队致力于开发NCOA7激动剂,并评估其在逆转PAH中的作用。他们使用计算机模拟和虚拟筛选技术识别了潜在的NCOA7激动剂,评估了这些激动剂对溶酶体功能、氧化胆固醇和胆汁酸产生以及肺血管EC免疫激活的影响,在单克隆毒性肺动脉高压大鼠模型中评估了NCOA7激动剂的治疗效果。研究结果发现,计算机模拟和虚拟筛选识别了NCOA7激动剂958ami 。 958 ami增强了ATP6V1B2-NCOA7相互作用,促进了溶酶体酸化,抑制了CH25H的表达,并减少了EC免疫激活。在单克隆毒性肺动脉高压大鼠模型中, 958 ami抑制了EC免疫激活和血管重构,改善了右心功能。这证明了NCOA7激动剂 958 ami可以逆转PAH的病理过程,为PAH的治疗提供了新的策略。
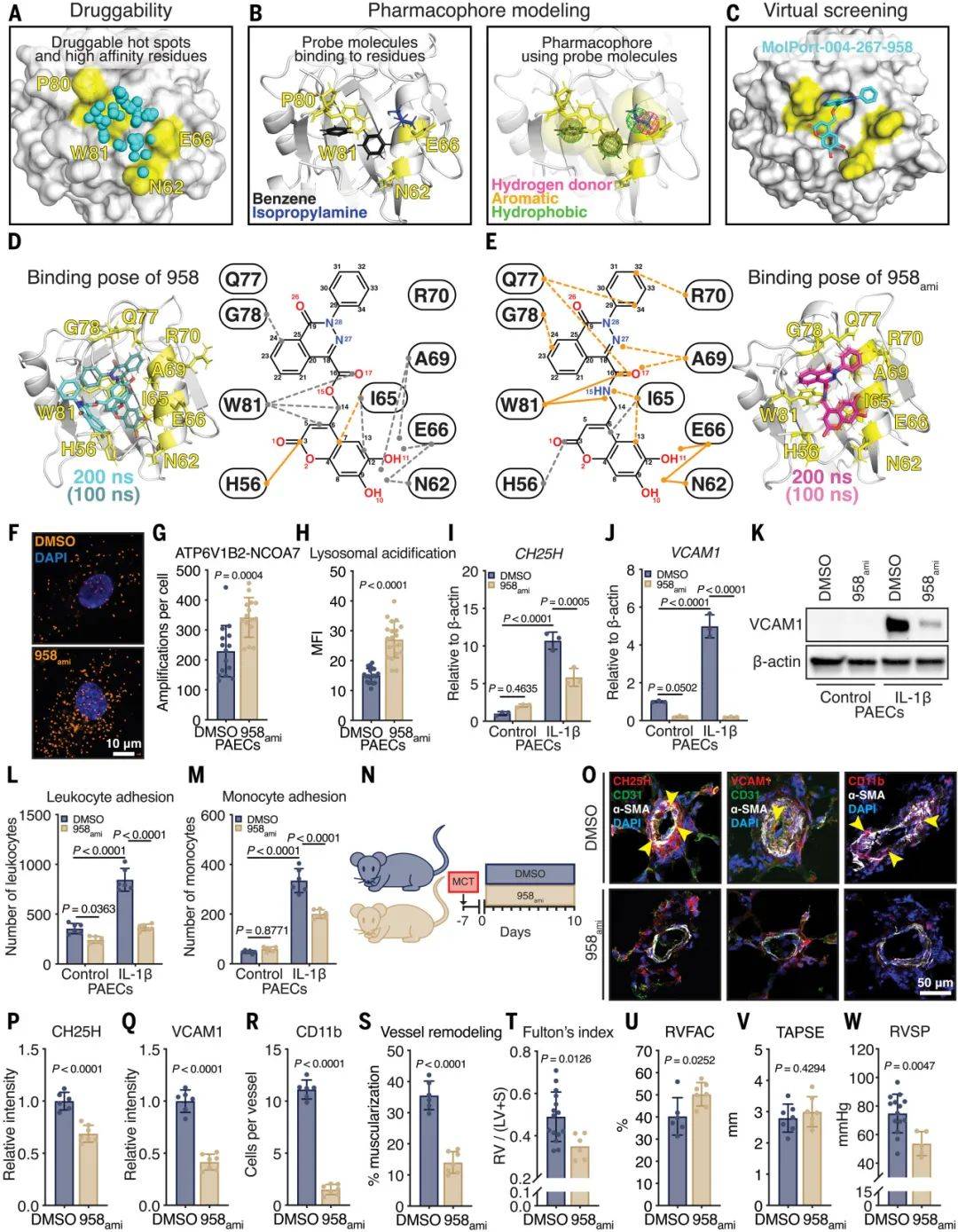 图8 计算建模确定了958AMI作为消除内皮免疫激活和PAH的NCOA7激活剂
图8 计算建模确定了958AMI作为消除内皮免疫激活和PAH的NCOA7激活剂
(图源:Harvey, et al., Science, 2025)
小结
综上所述,本研究揭示了溶酶体生物学和炎症性类固醇代谢在血管内皮细胞炎症和PAH中的作用机制,为PAH的诊断和治疗提供了新的思路,并为开发针对NCOA7的治疗药物提供了重要的理论依据。这一研究不仅为理解NCOA7在衰老和疾病中的作用提供了新的视角,也为未来的临床应用和药物开发奠定了基础。
拜谱小结
拜谱生物,作为国内领先的多组学公司,可提供完善成熟的蛋白组学、代谢组学、转录组学等多组学产品技术服务体系。在代谢组学领域,拜谱生物全面布局非靶代谢、靶向代谢组、广靶代谢、非靶脂质和靶向脂质产品,并针对动物/医学类样本、植物样本、中药等不同样本类型,推出特色代谢和脂质检测产品,如MT1000医学全靶、GT-MAX植物广靶、中药代谢、MLT4500医学靶向脂质组学等。拜谱全新推出的QMT1000医学绝对定量靶向代谢组学产品,面向医学/动物类样本,可实现1000+医学专属性代谢物的高通量绝对定量检测,助力医学领域研究,欢迎咨询!
参考文献:
Harvey LD, Alotaibi M, Tai YY, Tang Y, Kim HJ, Kelly NJ, Sun W, Woodcock CC, Arshad S, Culley MK, El Khoury W, Xie R, Al Aaraj Y, Zhao J, Hafeez N, Rao RJ, Jiang S, Negi V, Kirillova A, Perk D, Watson AM, St Croix CM, Stolz DB, Lee JY, Cheng MH, Zhang M, Detmer S, Guzman E, Manan RS, Saggar R, Haley KJ, Waxman AB, Okawa S, Schwantes-An TH, Pauciulo MW, Wang B, Webb A, Chauvet C, Anderson DG, Nichols WC, Desai AA, Lafyatis R, Nouraie SM, Wu H, McDonald JG, Cheng S, Bahar I, Bertero T, Benza RL, Jain M, Chan SY. Lysosomal dysfunction and inflammatory sterol metabolism in pulmonary arterial hypertension. Science. 2025 Jan 24;387(6732):eadn7277. doi: 10.1126/science.adn7277.