

糖尿病伤口是糖尿病最常见的并发症。糖尿病创面患者往往存在延迟愈合、感染甚至截肢的风险。创面中,高血糖导致三羧酸循环(TCA)中的电子供体增加,损害细胞内抗氧化酶如超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GPx)和过氧化氢酶(CAT)的活性,导致过量活性氧(ROS)的产生,激活巨噬细胞内NF-κB信号通路,诱导其向M1表型极化,导致免疫微环境的破坏。
2024年10月,川北医学院在Journal of Nanobiotechnology(IF=10.6)上发表题为“Zinc-based Polyoxometalate Nanozyme Functionalized Hydrogels for optimizing the Hyperglycemic-Immune Microenvironment to Promote Diabetic Wound Regeneration”的研究文章。本文研究者开发了一种纳米酶功能化再生微环境调节剂(AHAMA/ CS-GOx@Zn-POM),用于有效修复糖尿病伤口。这种新型结构将醛和甲基丙烯酸酐修饰的透明质酸水凝胶(AHAMA)和壳聚糖纳米颗粒(CS NPs)结合在一起,包封了锌基多金属氧酸盐纳米酶(Zn-POM)和葡萄糖氧化酶(GOx),模拟ROS清除相关酶的活性,同时发挥锌离子的免疫调节作用,为糖尿病伤口修复提供一种有前途的治疗方法。该研究成果中拜谱生物为其提供RNA-seq检测服务。

文章名称:Zinc-based Polyoxometalate Nanozyme Functionalized Hydrogels for optimizing the Hyperglycemic-Immune Microenvironment to Promote Diabetic Wound Regeneration(Journal of Nanobiotechnology,IF=10.6,2024.10)
客户单位:川北医学院
研究材料:巨噬细胞(n=3)
拜谱提供技术:RNA-seq
研究思路:
一、研究结果
01、Zn-POM的制备与表征
本研究采用一步还原法合成了Zn-POM,并用不同技术方法对其进行了表征(图1a-h)透射电镜(TEM)结果表明,在PBS(pH 7.4)溶液中,纳米材料均匀分布,粒径约为5 nm。当pH值降低到6.0和4.0时,纳米酶自组装并聚集成更大的纳米颗粒;由碳、氮、氧、钼和锌元素组成。
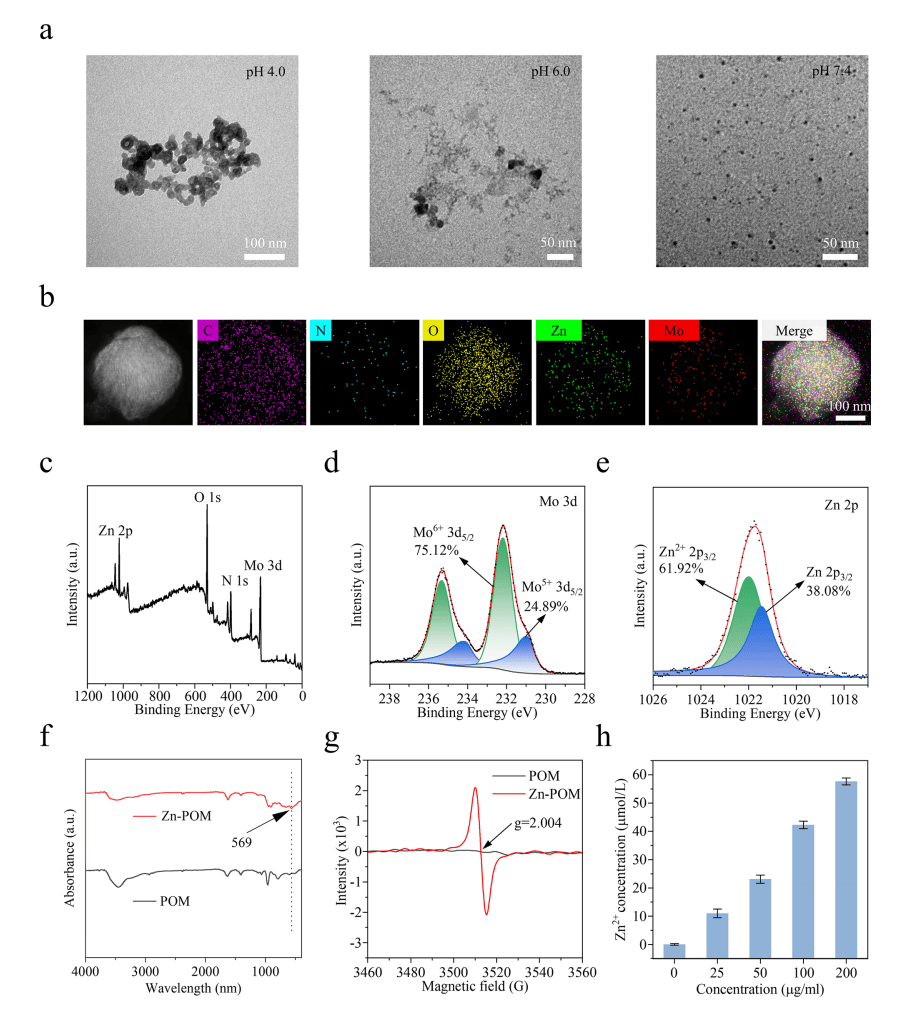 图1| Zn-POM的制备与表征
图1| Zn-POM的制备与表征
(图源:Chaoyu Pu., et al., J Nanobiotechnology., 2024)
02、GOx与Zn-POM的酶催化活性
GOx将葡萄糖氧化为葡萄糖酸和过氧化氢,其降糖作用与GOx浓度呈正相关。当GOx浓度超过200µg/mL时,24 h内葡萄糖浓度下降至0 mmol/L(图2b)。在pH范围为4~6时,糖代谢效率为最佳(图2c)。不同浓度的Zn-POM与过氧化氢反应10 min后,紫外光谱分析显示Zn-POM的紫外吸收峰下降,清除过氧化氢的效率与其浓度呈正相关,与pH呈负相关(图2e-g)。活性氧清除效率也与其浓度呈正相关(图2j-l)。
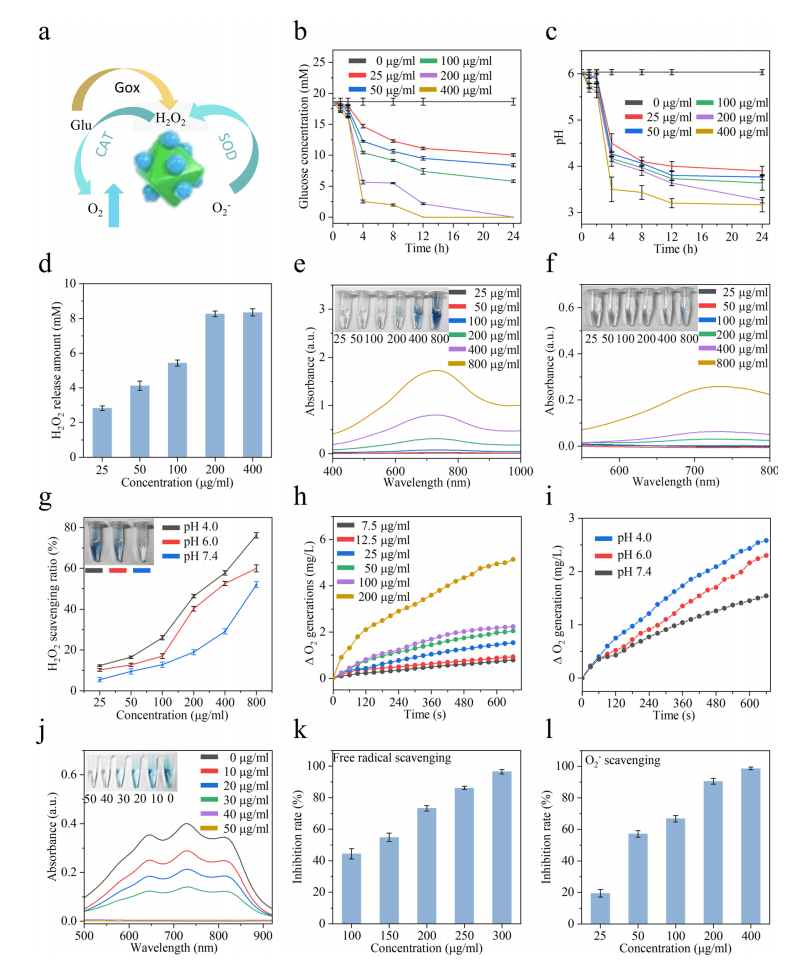 图2| GOx的酶催化活性
图2| GOx的酶催化活性
(图源:Chaoyu Pu., et al., J Nanobiotechnology., 2024)
03、AHAMA/CS-GOx@Zn-POM的表征
采用离子交联法合成了壳聚糖纳米颗粒。透射电镜观察其形态,呈圆形(图3a)。带正电荷的壳聚糖纳米颗粒与带负电荷的GOx和Zn-POM结合的透射电镜成像显示,Zn-POM均匀分布在壳聚糖纳米颗粒周围(图3b)。XPS分析证实,载药纳米颗粒中含有碳、氧、锌、钼、磷等元素(图3c)。粒径测量结果表明,壳聚糖纳米颗粒随GOx和Zn-POM的负载增加,纳米颗粒的粒径增大,而它们的zeta电位逐渐减小(图3d和e)。
 图3| AHAMA/CS-GOx@Zn-POM的表征
图3| AHAMA/CS-GOx@Zn-POM的表征
(图源:Chaoyu Pu., et al., J Nanobiotechnology., 2024)
04、AHAMA/CS-GOx@Zn-POM体外细胞实验
相较于HG处理的HUVECs出现的抑制细胞增殖和细胞死亡增加,其他两组则表现出快速的细胞增殖和较低的细胞死亡率,表明纳米酶水凝胶具有良好的生物相容性(图4a)。细胞迁移和血管形成实验表明,清除ROS的A-C-Z组的细胞迁移率比HG组增加了1.8倍。A-C-G-Z组可改善高血糖微环境和氧化应激,与HG组相比,细胞迁移率增加了2.4倍,且显著促进血管的形成,淋巴结数和总管长度明显高于其他治疗组。(图4b-f)。
 图4| AHAMA/CS-GOx@Zn-POM体外细胞实验
图4| AHAMA/CS-GOx@Zn-POM体外细胞实验
(图源:Chaoyu Pu., et al., J Nanobiotechnology., 2024)
05、AHAMA/ CS-GOx@Zn-POM处理巨噬细胞实验
LPS刺激诱导进入M1巨噬细胞,模拟糖尿病创面的免疫失衡,与PBS组相比,A-C-Z组和A-C-G-Z组显著降低ROS表达,减轻细胞氧化应激,且A-C-G-Z组CD86的表达量最低,CD206表达量最高(图5a-e)。表明,AHAMA/ CS-GOx@Zn-POM可以清除ROS,改善氧化应激,促进巨噬细胞向M2表型极化。
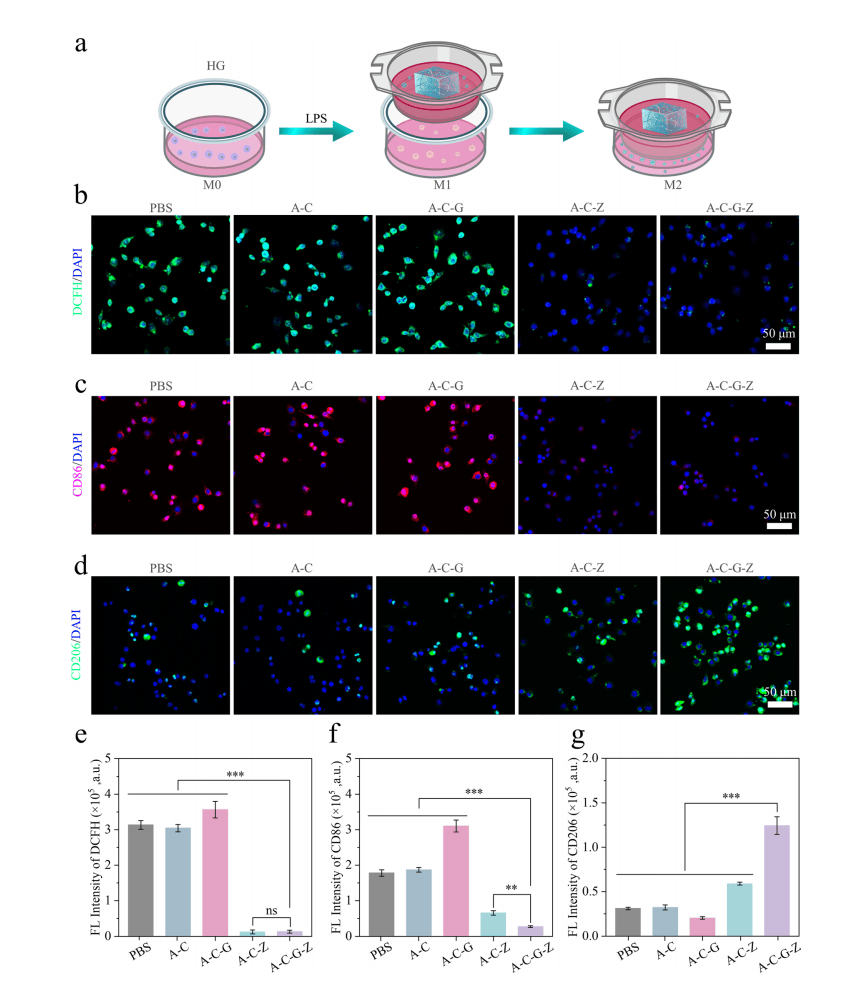 图5| AHAMA/ CS-GOx@Zn-POM处理巨噬细胞实验
图5| AHAMA/ CS-GOx@Zn-POM处理巨噬细胞实验
(图源:Chaoyu Pu., et al., J Nanobiotechnology., 2024)
06、AHAMA/CS-GOx@Zn-POM促进体外血管生成和胶原蛋白生成
在体外实验中,收集各组的巨噬细胞上清液,用于处理HUVECs和成纤维细胞。A-C-G-Z组的CD31和I型胶原蛋白表达量明显高于其他各组(图6a,b)。
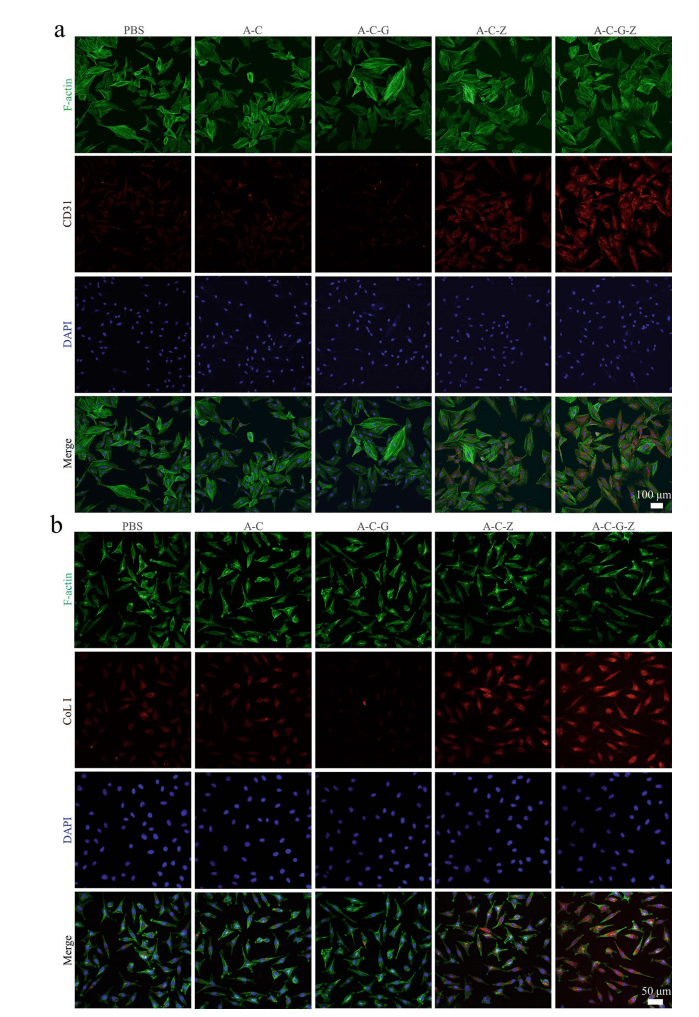 图6|AHAMA/CS-GOx@Zn-POM促进体外血管生成和胶原蛋白生成
图6|AHAMA/CS-GOx@Zn-POM促进体外血管生成和胶原蛋白生成
(图源:Chaoyu Pu., et al., J Nanobiotechnology., 2024)
07、AHAMA/CS-GOx@ Zn-POM促进巨噬细胞极化的机制的验证
用LPS刺激RAW264.7细胞诱导M1极化后,用PBS和Zn-POM处理M1巨噬细胞。RNA-seq分析显示(图7a-f),与PBS组相比,Zn-POM组有1328个基因表达上调,1096个基因表达下调,KEGG富集分析显示,与PBS组相比,Zn-POM组的ROS相关信号通路如MAPK、TNF、NF-κB通路均下调,提示免疫微环境中炎症受到抑制,GO富集分析表明,Zn-POM组增强了免疫应答的调控。
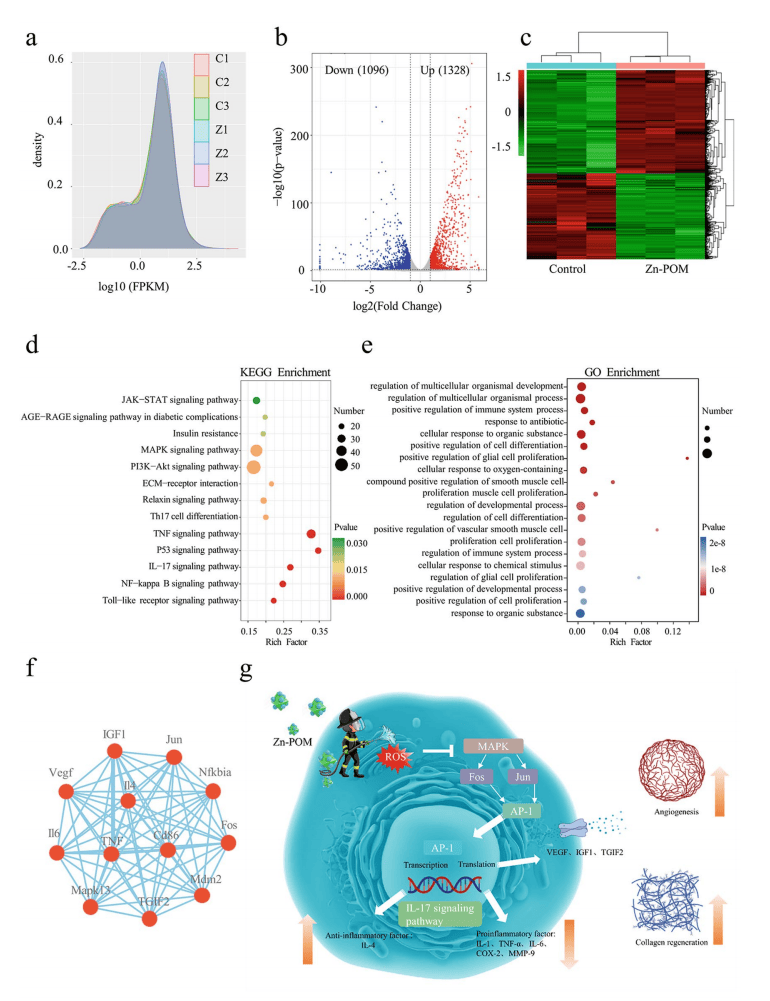 图7|AHAMA/CS-GOx@ Zn-POM促进巨噬细胞极化的机制的验证
图7|AHAMA/CS-GOx@ Zn-POM促进巨噬细胞极化的机制的验证
(图源:Chaoyu Pu., et al., J Nanobiotechnology., 2024)
08、AHAMA/CS-GOx@Zn-POM体内实验促进糖尿病创面愈合
与PBS组相比,A-C-G组和A-C-Z组的伤口愈合率显著升高。GOx和Zn-POM的联合应用进一步增强了促愈合作用,协同加速了创面愈合。A-C-G-Z组的愈合率高达90%(图8a-f)。
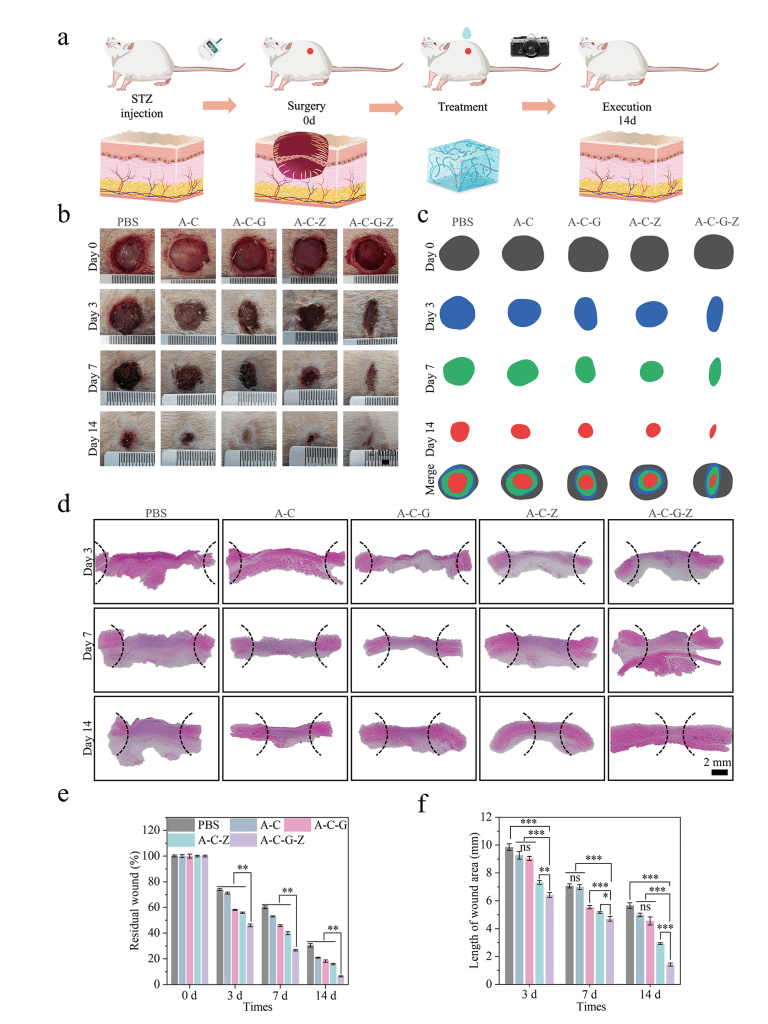 图8|AHAMA/CS-GOx@Zn-POM体内实验促进糖尿病创面愈合
图8|AHAMA/CS-GOx@Zn-POM体内实验促进糖尿病创面愈合
(图源:Chaoyu Pu., et al., J Nanobiotechnology., 2024)
二、文章小结
本文通过合成AHAMA/CS-GOx@Zn-POM,以及体内外实验揭示:纳米颗粒进入巨噬细胞后清除ROS并调节MAPK/IL-17信号通路。这导致炎症因子IL-1、IL-6、TNF-α、COX-2、MMP-9和CD86的下调,以及细胞因子IL-4的上调,促进巨噬细胞向M2表型极化。M2巨噬细胞随后上调IGF-1、VEGF、TGIF2等细胞因子,促进内皮细胞和成纤维细胞的增殖和分化,增强促愈合细胞的功能(图9)。
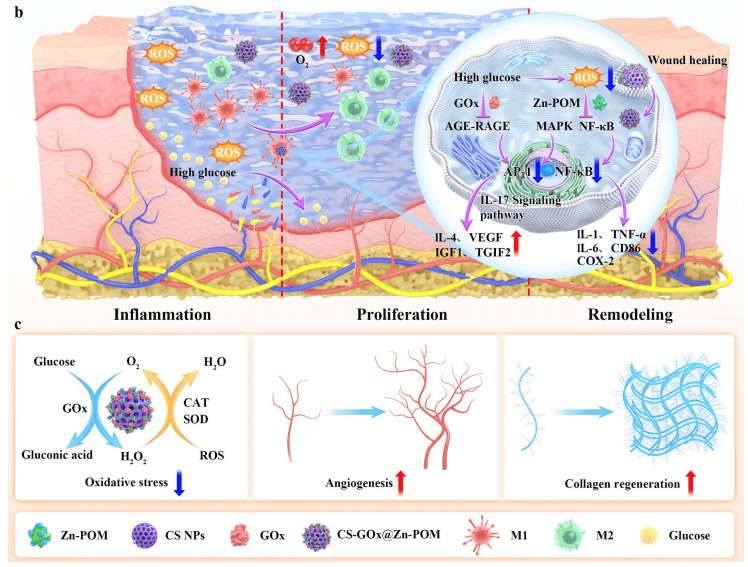 图9|AHAMA/CS-GOx@Zn-POM促进糖尿病创面愈合作用机制
图9|AHAMA/CS-GOx@Zn-POM促进糖尿病创面愈合作用机制
(图源:Chaoyu Pu., et al., J Nanobiotechnology., 2024)
三、拜谱小结
本文系统地展示了锌基多金属氧酸盐纳米酶功能化水凝胶在糖尿病伤口愈合中的应用潜力,并通过对AHAMA/CS-GOx@ Zn-POM处理M1极化巨噬细胞进行RNA-seq,揭示其作用机制,为相关领域的研究提供了新的视角和方法。该研究成果中拜谱生物为其提供RNA-seq检测服务。拜谱作为国内领先的多组学服务公司,可提供蛋白组、修饰组、代谢组、转录组等多组学技术服务助力发表高分文献,欢迎致电咨询!
参考文献:
Pu C, Wang Y, Xiang H, He J, Sun Q, Yong Y, Chen L, Jiang K, Yang H, Li Y. Zinc-based Polyoxometalate Nanozyme Functionalized Hydrogels for optimizing the Hyperglycemic-Immune Microenvironment to Promote Diabetic Wound Regeneration. J Nanobiotechnology. 2024 Oct 8;22