

在细胞的复杂网络中,N-糖基化扮演着至关重要的角色。这是一种精细调控蛋白质功能的生物过程,通过在蛋白质上附加糖链,N-糖基化对蛋白质的稳定性、功能以及细胞间的通信起着关键作用。它不仅影响单个蛋白质的命运,还对整个细胞的行为产生深远的影响。N-糖基化过程的微妙变化能够决定细胞如何响应外部信号,从而在发育、免疫反应和疾病发生中发挥重要作用。
2024年11月8日斯坦福大学医学院Rajat Rohatgi教授及其团队在Science杂志(IF:44.7)上发表了题为“Regulated N-glycosylation controls chaperone function and receptor trafficking”的研究文章,通过N-糖肽组学分析揭示了内质网中一个调控N-糖基化的新途径,该途径由CCDC134、OST-A和HSP90B1三个蛋白组成。CCDC134与HSP90B1的N端无序肽段结合,并招募OST-A,形成一个保护性支架,从而抑制HSP90B1的过度糖基化,维持其稳定性和功能。这对于WNT信号传导至关重要,其功能障碍可能导致骨发育障碍。本文将带您深入了解N-糖基化的神秘面纱,探索它如何在细胞内施展魔力。

英文标题:Regulated N-glycosylation controls chaperone function and receptor trafficking
中文题目:调节的 N-糖基化控制伴侣功能和受体运输
发表期刊:Science
影响因子:44.7
作者单位:斯坦福大学
研究材料:RKO细胞系
组学技术:N-糖肽组学
机制模型:
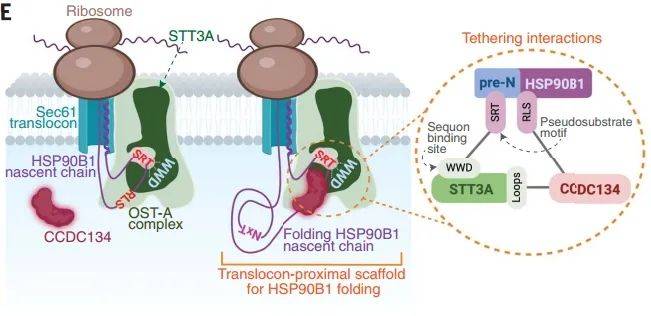 图1机制模型图
图1机制模型图
(图源:Ma, et al., Science, 2024)
1、研究结果
筛选影响 WNT 信号通路的基因
研究团队利用CRISPR-Cas9技术在人类细胞系中进行了全基因组范围内的失活筛选,以鉴定激活WNT/β-catenin信号通路所需的基因。这一筛选过程不仅确认了已知的WNT信号组分,如β-catenin、LRP6(WNT配体的共受体)等,还发现了CCDC134、STT3A和OSTC等基因与WNT信号通路的调控密切相关。这些基因的发现为理解WNT信号通路的复杂性提供了新的视角。通过荧光基的转录报告系统,研究人员监测了WNT3A对WNT/β-catenin信号通路的激活效应,从而识别出这些关键基因。
验证基因功能
通过基因敲除和功能恢复实验,研究团队深入探究了CCDC134、STT3A和OSTC等基因对WNT信号通路的影响。实验结果表明,CCDC134的缺失会导致HSP90B1分子伴侣的过度糖基化和稳定性下降,进而影响WNT信号通路的活性。这一发现揭示了CCDC134在WNT信号通路中的关键作用。通过免疫印迹和免疫荧光等技术,研究人员评估了这些基因敲除对HSP90B1稳定性和WNT信号通路的影响。功能恢复实验通过重新引入野生型或突变型基因,以评估它们对HSP90B1糖基化和WNT信号通路的恢复效果。
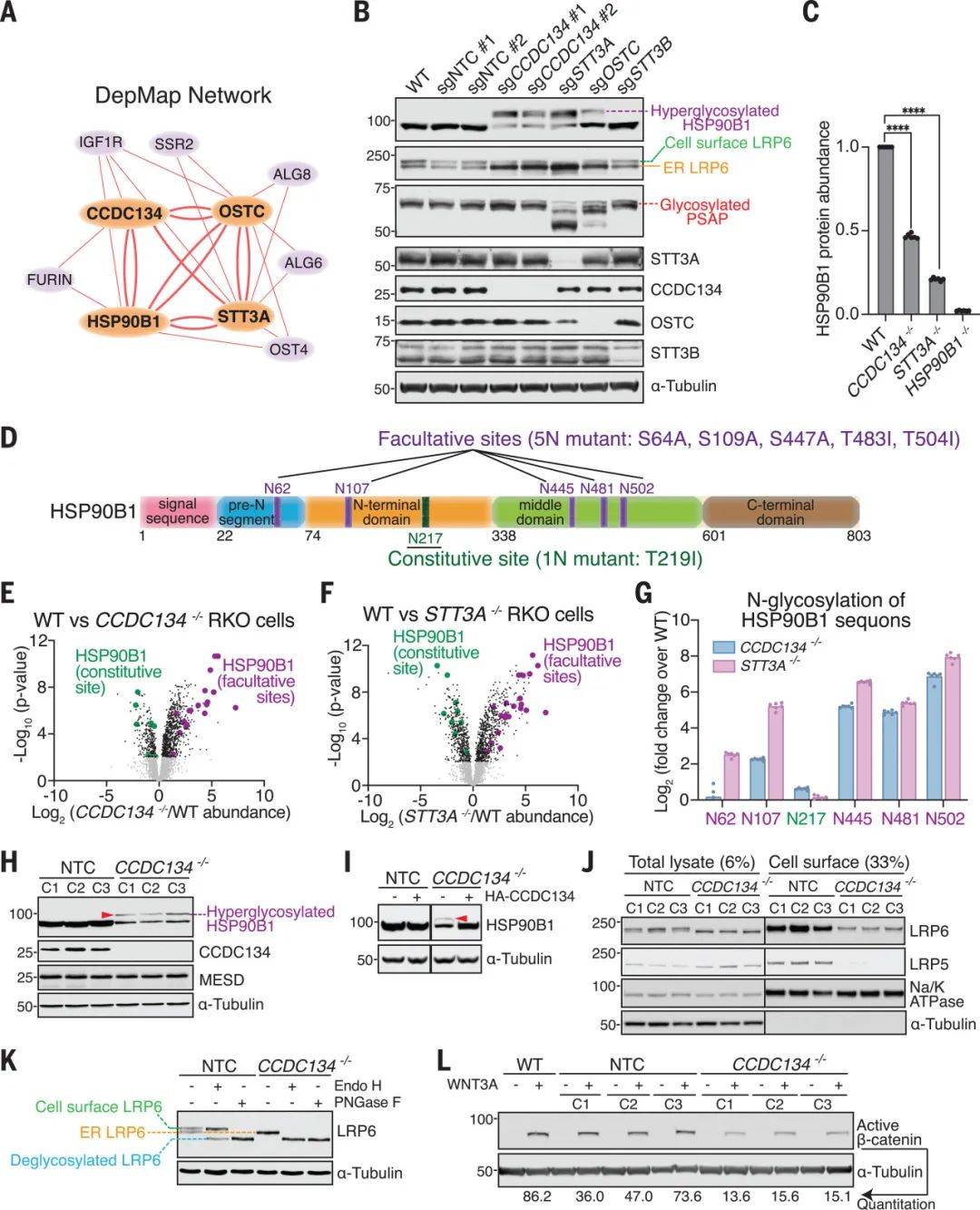 图2 内质网蛋白网络对HSP90B1 N-糖基化和WNT信号的调控
图2 内质网蛋白网络对HSP90B1 N-糖基化和WNT信号的调控
(图源:Ma, et al., Science, 2024)
HSP90B1蛋白的糖基化状态研究
研究团队利用N-糖肽组学技术,详细研究了HSP90B1的糖基化状态。他们从基因敲除细胞中提取蛋白质,并通过酶解和色谱分离技术,对HSP90B1的糖肽段进行了鉴定和定量。质谱数据揭示了CCDC134和STT3A缺失导致的HSP90B1糖基化模式的变化,为理解这些基因在糖基化调控中的作用提供了直接证据。研究发现,在CCDC134和STT3A基因敲除的细胞中,HSP90B1的过度糖基化现象显著增加,表明这两个基因在调控HSP90B1的N-糖基化中发挥着重要作用。
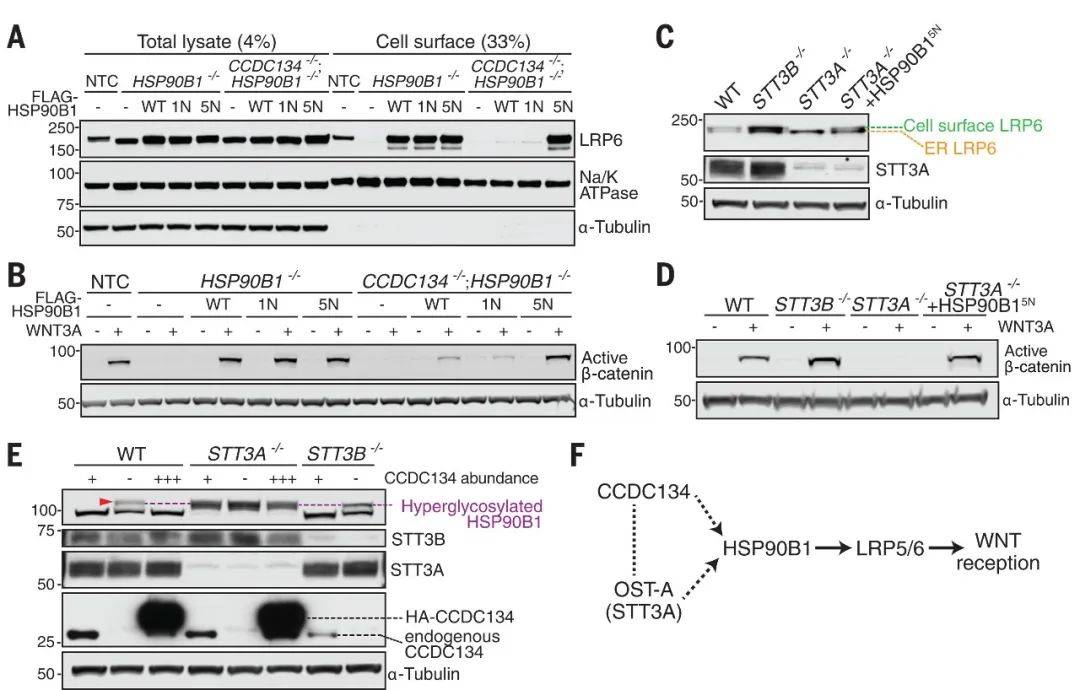 图3 HSP90B1的高糖基化调节WNT信号强度
图3 HSP90B1的高糖基化调节WNT信号强度
(图源:Ma, et al., Science, 2024)
HSP90B1 的自调控机制研究
通过突变分析、细胞表面蛋白分析和细胞功能分析等,研究团队探索了HSP90B1 N端肽段对其自身糖基化的影响。他们发现HSP90B1 N端的无序肽段可以抑制其自身的糖基化,并通过CCDC134调控其稳定性。这一自调控机制的发现为理解HSP90B1的功能提供了新的分子层面的解释。研究人员通过构建HSP90B1的突变体并进行体外翻译和糖基化分析,揭示了HSP90B1 N端的一个特定区域(1-93氨基酸)对其自身糖基化的调控作用。通过突变这一区域的关键氨基酸,研究团队进一步阐明了HSP90B1自调控糖基化的分子机制。
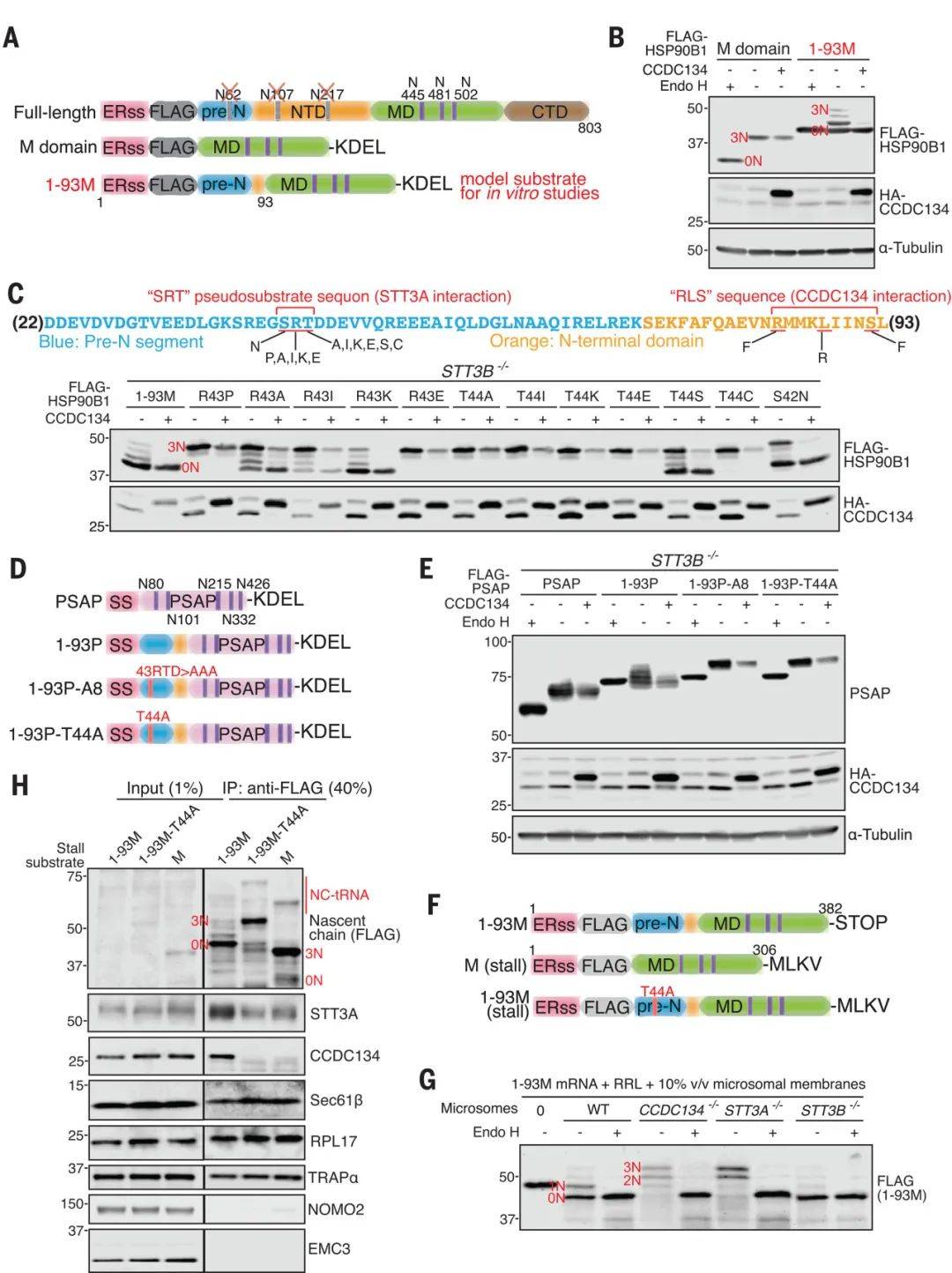 图4 HSP90B1的前N片段通过将CCDC134募集到含有OST-A的分泌位上抑制其自身的N-糖基化
图4 HSP90B1的前N片段通过将CCDC134募集到含有OST-A的分泌位上抑制其自身的N-糖基化
(图源:Ma, et al., Science, 2024)
STT3A 和 CCDC134 的作用机制研究
利用基因敲除、过表达实验和蛋白质相互作用分析,研究团队进一步研究了STT3A和CCDC134在HSP90B1糖基化调控中的作用机制。他们发现STT3A和CCDC134与HSP90B1形成复合物,在HSP90B1转运和折叠过程中发挥保护作用,抑制其过度糖基化。这一发现揭示了STT3A和CCDC134在内质网中的新功能。通过构建STT3A和CCDC134的突变体,并在体外进行表达和糖基化分析,研究人员发现这些基因与HSP90B1的相互作用对于其糖基化状态至关重要。
OST-A 的作用探究
通过突变分析,研究团队研究了OST-A的糖基转移酶活性对HSP90B1糖基化的影响。他们发现OST-A的糖基转移酶活性对于抑制HSP90B1过度糖基化并非必需。这一发现挑战了我们对OST-A功能的传统理解,提示OST-A可能通过非酶活性的方式参与蛋白质的折叠和质量控制。研究人员通过构建OST-A的突变体,并在细胞中表达这些突变体,发现即使在OST-A的糖基转移酶活性被抑制的情况下,HSP90B1的糖基化仍然受到抑制,表明OST-A可能通过其他机制调控HSP90B1的糖基化。
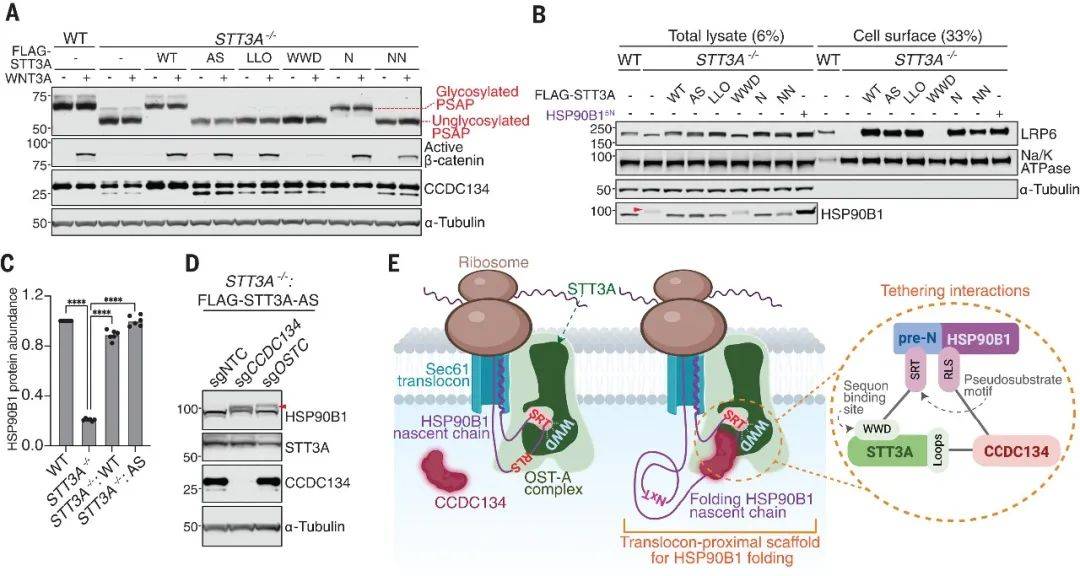 图5 OST-A的寡糖转移酶活性并不促进HSP90B1的稳定性和WNT信号传导
图5 OST-A的寡糖转移酶活性并不促进HSP90B1的稳定性和WNT信号传导
(图源:Ma, et al., Science, 2024)
2、小结
这项研究的发现不仅在分子层面上揭示了N-糖基化的新调控机制,而且在细胞和组织层面上展示了其对信号传导和疾病发展的影响。未来的研究将需要进一步探索CCDC134和HSP90B1在不同组织和发育阶段中的作用,以及它们如何响应不同的生理和病理信号。此外,这些发现为开发新的治疗策略提供了潜在的靶点,特别是在治疗骨质疏松。
3、拜谱小结
随着对N-糖基化调控机制的进一步研究,我们可能会发现更多的分子靶点和治疗机会。这项研究为我们提供了一个全新的视角,让我们重新审视N-糖基化在生命活动中的作用。随着质谱技术的不断发展,针对O-糖基化、N-糖基化以及完整糖肽的分析能力已经实现质的飞跃。拜谱生物推出的完整糖肽产品可以有效检测蛋白质糖基化的位点和糖型结构,包括但不限于糖链组成、糖链长度、分支情况、糖基化位点等分析内容,该产品适用于癌症、免疫疾病、神经退行性疾病等领域的糖基化研究,助力科研人员深入挖掘糖基化在疾病发生与发展中的机制。同时,拜谱生物提供专业的技术支持和定制化服务,确保每一位客户都能获得高质量的实验结果和精准的分析数据。未来,拜谱生物将继续致力于糖基化领域的创新与突破,为推动生命科学研究和临床应用提供坚实保障。想了解更多关于完整糖肽产品的信息,欢迎咨询!
参考文献:
Ma M, Dubey R, Jen A, Pusapati GV, Singal B, Shishkova E, Overmyer KA, Cormier-Daire V, Fedry J, Aravind L, Coon JJ, Rohatgi R. Regulated N-glycosylation controls chaperone function and receptor trafficking. Science, 2024 Nov 7. doi: 10.1126/science.adp7201