

肉的宰后嫩化主要归因于肌原纤维结构的破坏,肌原纤维结构是由内源性蛋白水解酶降解肌原纤维和细胞骨架蛋白造成的。与几十年来一直是关注焦点的钙蛋白酶不同,胱天蛋白酶(caspases)最近成为感兴趣的话题。胱天蛋白酶在细胞凋亡的执行阶段起着至关重要的作用,其中caspase-3在死后蛋白水解中的作用是多方面和复杂的,因此值得进一步研究。S-亚硝基化通过调节钙释放、能量代谢、蛋白质降解和细胞凋亡来调节肉质,包括嫩度和持水能力。前期研究发现S-亚硝基化可以下调依赖线粒体的caspase-3级联反应,这可能是肌肉细胞凋亡和牛肉品质变化的原因。caspase-3的研究重点是其与细胞凋亡的关系,然而,很少有研究探讨S-亚硝基化调节caspase-3的机制。
2024年9月由南京农业大学张万刚教授团队在期刊Journal of Agricultural and Food Chemistry发表题为“Exploring the Effects of S‑Nitrosylation on Caspase‑3 Modification and Myofibril Degradation of Beef In Vitro”文章,研究发现了GSNO处理后caspase-3的活性显著降低(P < 0.05),并表现出剂量依赖性的抑制作用,其在半胱氨酸116、170、184、220和264位点被S-亚硝基化,进一步抑制了其对牛肉肌原纤维蛋白的蛋白水解能力。拜谱生物为该研究提供了亚硝基化修饰组学检测服务,助力发现目的蛋白上的亚硝基化修饰位点。

中文标题:体外研究S-亚硝基化对牛肉Caspase-3修饰和肌原纤维降解的影响
期刊:Journal of Agricultural and Food Chemistry
2024年影响因子:5.7
发表时间:2024年9月
客户单位:南京农业大学
研究材料:蛋白
拜谱提供技术:亚硝基化修饰组学
技术路线:

一、研究结果
01.Caspase-3活性
目前尚不清楚NO对caspase-3的抑制作用是否归因于NO介导的S-亚硝基化,不同浓度梯度的GSNO作为外源性NO供应,以诱导caspase-3的体外S-亚硝基化。结果表明,与没有GSNO的组相比,100、200和400μM GSNO组的caspase-3活性显著降低(图1),与先前报道一致。GSNO处理降低caspase-3活性的潜在原因仍有待阐明。
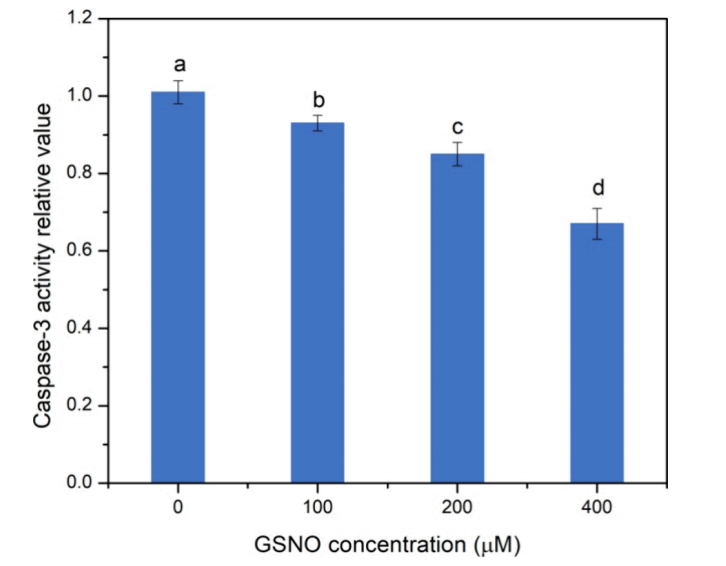 图1 不同浓度的GSNO处理对caspase-3活性的影响
图1 不同浓度的GSNO处理对caspase-3活性的影响
(图源:Hou, Qin et al., J Agric Food Chem.. 2024)
02.Caspase-3的S-亚硝基化程度
研究Caspase-3的亚硝基化程度,以阐明GSNO对Caspase-3的反应性。经GSNO处理后,检测到caspase-3蛋白S-亚硝基化强度增加(图2)。这些结果表明,外源性GSNO培养可成功诱导caspase-3的体外S-亚硝基化。令人惊讶的是,在没有GSNO存在的对照组中检测到一个微弱的S-亚硝基化带,这表明caspase-3可能发生内源性的S-亚硝基化。此外,本研究中caspase-3的S-亚硝基化程度较高,而caspase-3的活性降低,这与之前的研究一致。然而,caspase-3的特异性S-亚硝基化修饰位点尚不清楚,还需要进一步的探索。
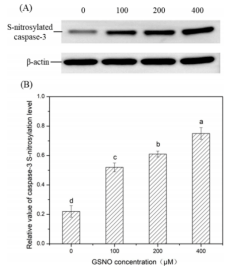 图2 GSNO处理对caspase-3S-亚硝基化水平的影响
图2 GSNO处理对caspase-3S-亚硝基化水平的影响
(图源:Hou, Qin et al., J Agric Food Chem.. 2024)
03.Caspase-3的S-亚硝基化位点
通过亚硝基化修饰组学检测caspase-3的S-亚硝基化位点。结果表明,caspase-3上的4个多肽中有5个半胱氨酸残基被蛋白S-亚硝基化修饰(图3)。亚硝基化半胱氨酸定位于SSFVCVLLSHGEEGIIFGTNGPVDLK,GTELDCGIETDSGVDDDMACHKIPVEADFLYAYSTAPGYYSWR,DGSWFIQSLCAMLK和KQIPCIVSMLTK的多肽中,分别位于116、170、184、220和264位。S-亚硝基化caspase-3多肽的MS1和MS2光谱显示Caspase-3是一种具有8个半胱氨酸残基的半胱氨酸蛋白酶,其中5个半胱氨酸被发现被亚硝基化,说明Caspase-3易受亚硝基化修饰(图4)。此外,据先前报道casase-3的催化残留亚硝基化Cys163,这不同于本研究的结果。S-亚硝基化caspase-3的丰度、位点的修饰水平和检测方法的灵敏度的差异可能是导致结果不一致的原因之一。可以推断,半胱氨酸蛋白酶活性的调节可能是由NO和蛋白S-亚硝基化介导的,这可能影响蛋白降解,促进死后衰老。
 图 3 caspase-3的序列。蓝色标记的序列表示S-亚硝基化肽,红色标记的C表示S-亚硝基化半胱氨酸
图 3 caspase-3的序列。蓝色标记的序列表示S-亚硝基化肽,红色标记的C表示S-亚硝基化半胱氨酸
(图源:Hou, Qin et al., JAgric Food Chem.. 2024)
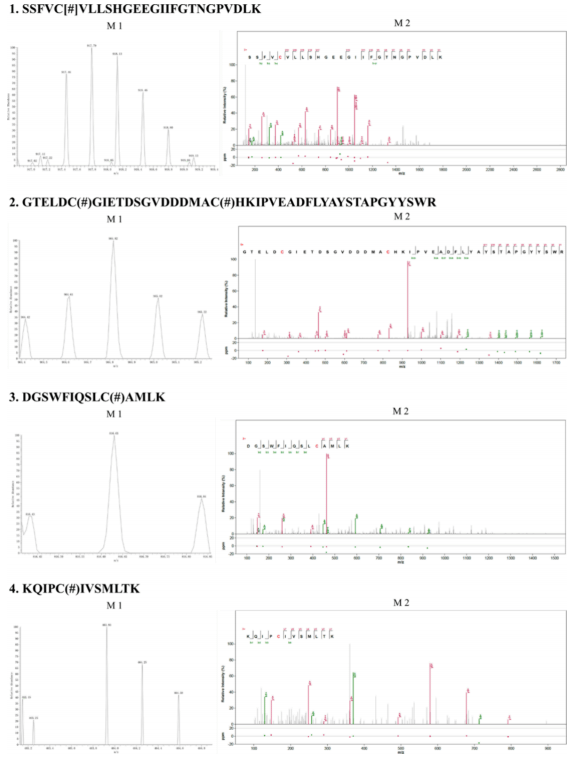 图4. s-亚硝基化肽和caspase-3位点的MS1和MS2光谱
图4. s-亚硝基化肽和caspase-3位点的MS1和MS2光谱
(图源:Hou, Qin et al., J Agric Food Chem.. 2024)
04.S-亚硝基化Caspase-3降解结蛋白
结蛋白作为一种重要的细胞骨架蛋白,在维持肌细胞结构的结构完整性和收缩性方面起着重要作用,研究S-亚硝基化caspase-3对结蛋白降解的敏感性具有重要意义。与Std(未用胱天蛋白酶-3和GSNO孵育的初始肌纤维蛋白)组相比,0 μM GSNO组(肌原纤维和caspase-3的孵育,无GSNO)的完整结蛋白含量显著降低,提示caspase-3对结蛋白具有潜在的蛋白水解能力。在GSNO孵育后,完整结蛋白的含量明显增加(P < 0.05)。此外,当GSNO浓度升高时,完整结蛋白的含量持续上调(P < 0.05)(图5)。这一发现表明,SNO修饰的caspase-3以水平依赖的方式抑制结蛋白的降解。
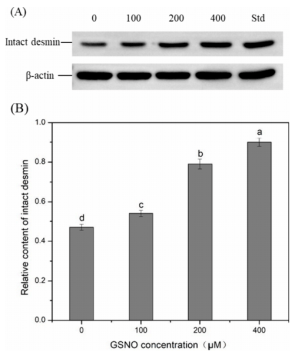 图5.S-亚硝基化caspase-3降解结蛋白
图5.S-亚硝基化caspase-3降解结蛋白
(图源:Hou, Qin et al., J Agric Food Chem.. 2024)
05.S-亚硝基化Caspase- 3降解肌钙蛋白-T
肌钙蛋白-T (TnT)是原肌球蛋白调节负责肌肉收缩的细丝的必需肌原纤维蛋白。TnT的降解特征是检测到28和30 kDa的TnT。在亚硝基化条件下,caspase-3对TnT的降解情况如图6所示,与Std组(不含caspase-3和GSNO的肌原纤维)相比,caspase-3组中30 kDa TnT片段显著增加,表明caspase-3参与了TnT的降解,此外,caspase-3与GSNO的孵育导致30 kDa TnT下降。在100和200 μM GSNO组之间没有检测到明显的差异(P > 0.05),而当GSNO的浓度达到400 μM 时,该片段显著减少(P < 0.05)。这些发现表明了SNO修饰的caspase-3对TnT降解的抑制作用。结蛋白和TnT是caspase-3的敏感底物,而GSNO处理降低caspase-3的活性可能导致肌原纤维蛋白降解程度降低。综上所述,NO诱导的S-亚硝基化可以通过修饰半胱氨酸残基来调节caspase-3的活性,进而进一步影响其对结蛋白和TnT的蛋白水解能力,从而影响牛肉品质。
 图6. S-亚硝基化caspase- 3降解肌钙蛋白-T
图6. S-亚硝基化caspase- 3降解肌钙蛋白-T
(图源:Hou, Qin et al., J Agric Food Chem.. 2024)
二、小结
本研究旨在探讨S-亚硝基化对caspase-3修饰的影响及其随后对牛肉肌原纤维体外降解的影响。蛋白S-亚硝基化可以修饰caspase-3的半胱氨酸残基,从而导致caspase-3活性降低,进一步抑制了其对牛肉肌原纤维蛋白的蛋白水解能力。
三、拜谱小结
研究采用了酶活测定,亚硝基化修饰组学分析,WB等检测手段,发现蛋白S-亚硝基化可以修饰caspase-3的半胱氨酸残基,这导致了caspase-3活性的降低,并进一步抑制了其对牛肉肌原纤维蛋白的蛋白水解能力。本研究为解释蛋白质亚硝基化对肉质的调控机制提供了一个新的视角。
拜谱生物作为一家国内领先的多组学服务公司,可提供完善成熟的蛋白质组学、修饰蛋白质组学、代谢组学、转录组学等多组学产品技术服务体系,整合多组学数据进行深入挖掘分析,全面解析机制机理等,助力高分文章发表。除此之外,拜谱生物还可提供半胱氨酸系列产品,包括亚硝基化、谷胱甘肽化、硫巯基化、次磺酸化、total氧化还原、游离巯基,欢迎大家咨询!
参考文献:
Qin Hou, Chao Ma, Rui Liu, Zhuangli Kang, and Wangang Zhang.Exploring the Effects of S-Nitrosylation on Caspase-3 Modification and Myofibril Degradation of Beef In Vitro. Journal of Agricultural and Food Chemistry. doi.org/10.1021/acs.jafc.4c06663