

背景介绍
为什么在同样的流感季,有人安然无恙,有人却轻易中招?为什么面对同一种肿瘤免疫疗法,患者的响应率却天差地别?这种免疫力的差异,并非完全由基因决定,而与肠道菌群密切相关。
近日,加州大学旧金山分校的研究团队在《Cell》发表了一项具有里程碑意义的研究,通过多组学整合分析证实:人体免疫系统中一个关键的“总开关”——干扰素(IFN)反应的强度,与肠道菌群的组成和代谢产物密切相关。换言之,肠道微生物群是塑造个体免疫系统的重要调控因素。

研究背景
寻找免疫差异的“暗物质”
人类的免疫系统存在巨大的个体差异。即使在没有感染或自身免疫疾病的健康状态下,不同个体的免疫细胞组成和细胞因子水平也大相径庭。这种“免疫基线”直接决定了我们对病原体的抵抗力以及对疫苗和免疫治疗的反应。
过去的研究多聚焦免疫学表型观察,较少关注肠道微生物组的系统性作用。本研究旨在打破壁垒,通过超高维度的多组学手段,系统绘制健康人群免疫系统与肠道菌群的互作图谱,寻找决定个体“免疫基线”的核心驱动力。
深度解读
多组学视角下的核心发现
1、全景式多组学分析
研究团队对110名健康个体进行了系统性的整合分析发现:CyTOF、CITE-seq揭示NKT、NK以及T细胞亚群差异显著;转录组发现干扰素反应相关基因是主要变异轴;宏基因组显示菌属丰度个体差异突出。这些差异,甚至比年龄、性别带来的影响还要大。
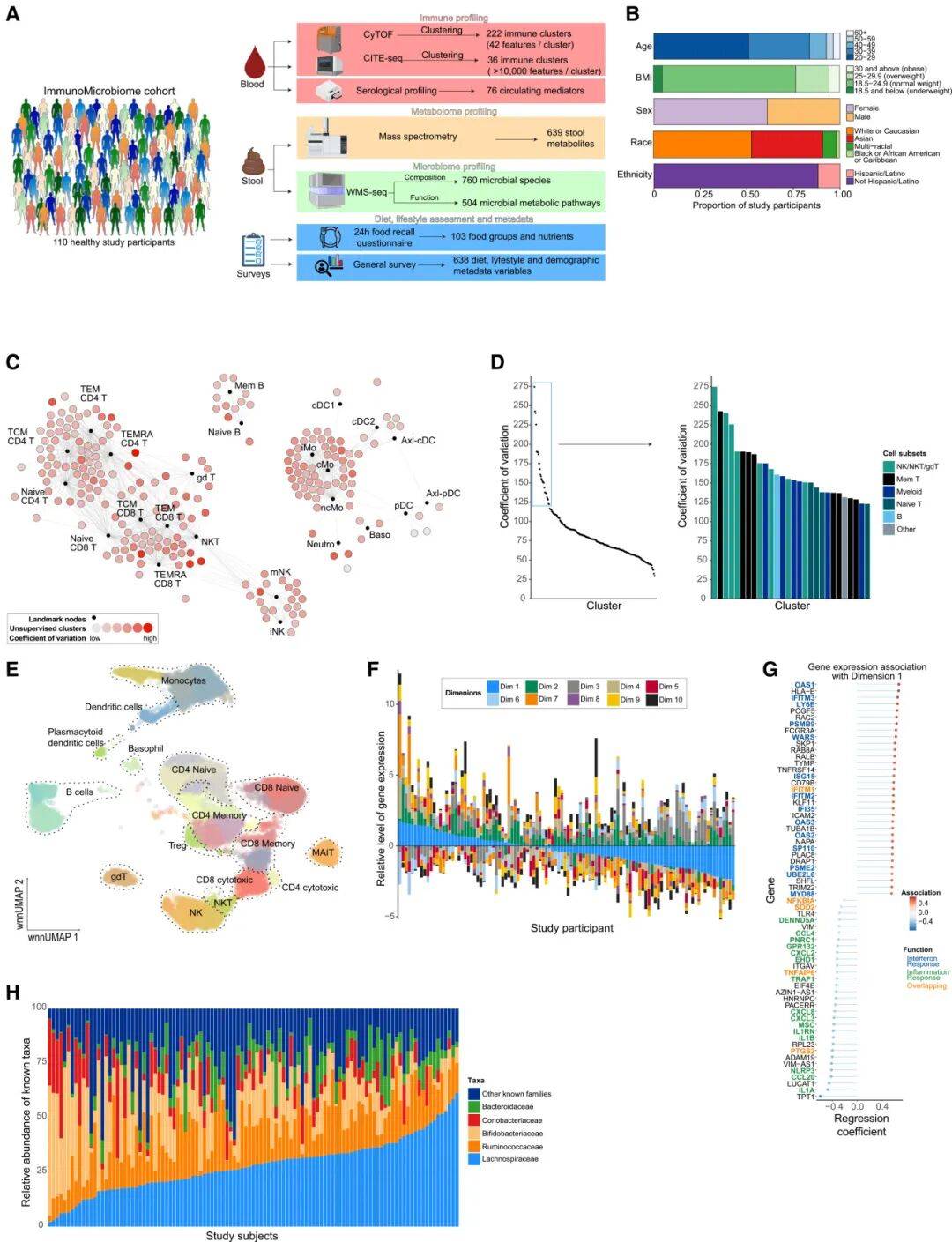
图1:健康人群队列中的免疫和微生物组变异
2、免疫变异的两大核心轴
研究人员采用了多组学因子分析(MOFA)识别出两条主要的免疫变异轴:
IMCV(免疫-微生物组协同变异轴)
该变异轴不仅与血液中特定的免疫细胞特征相关,还与消化道微生物的组成高度协同。
IIV(独立免疫变异轴)
该变异轴同样反映了免疫系统的变异,但完全独立于微生物组。
其中,IMCV更显著地富集干扰素(Tonic-IFN)和炎症通路。
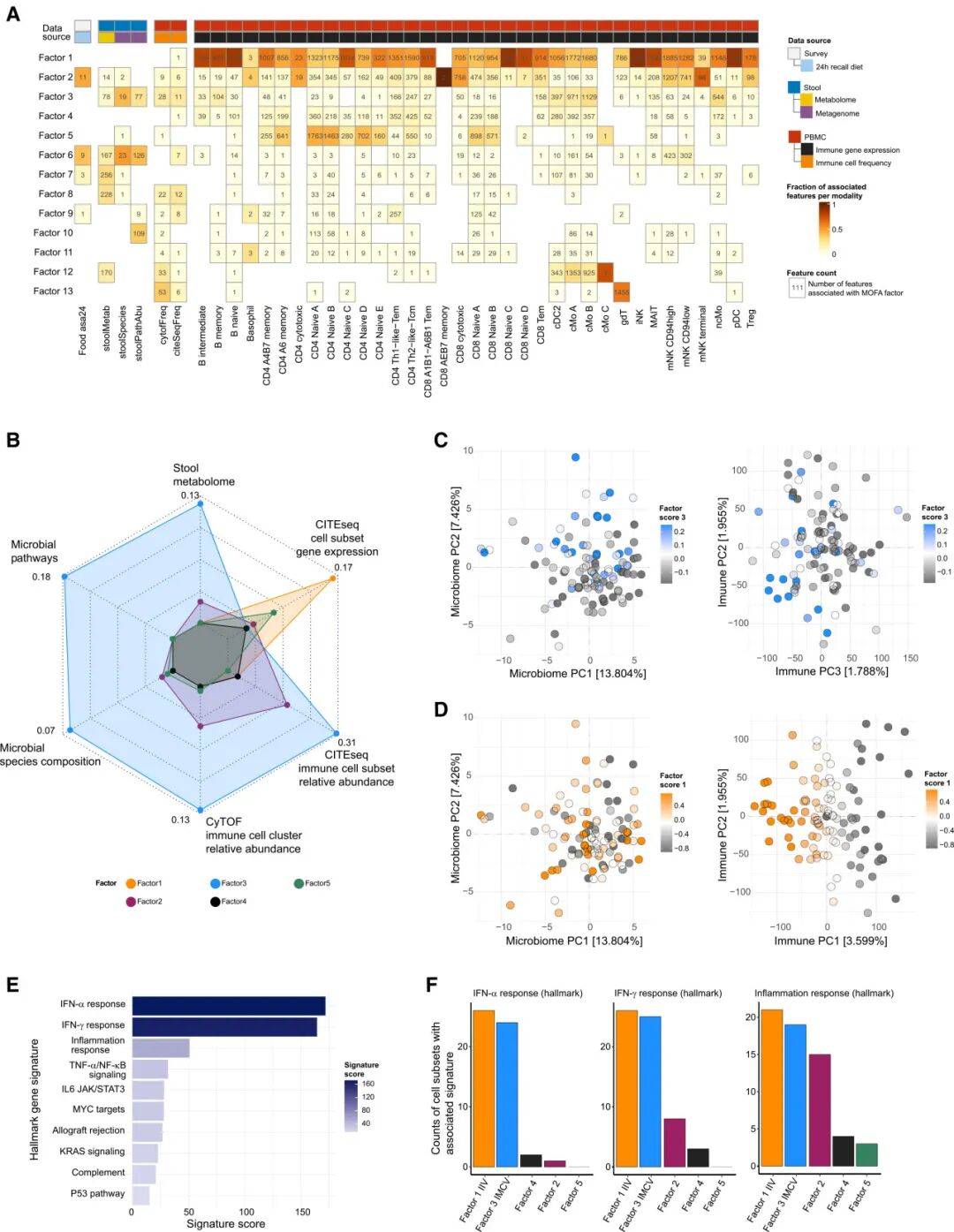
图2:鉴别免疫变异轴
3、免疫细胞活化特征
CITE-seq和CyTOF数据进一步证实,IMCV与特定免疫细胞群体的丰度变化密切相关。高IMCV评分的个体中,高抗原递呈单核细胞,以及记忆T细胞、MAIT与NK细胞均呈现明显的活化状态。
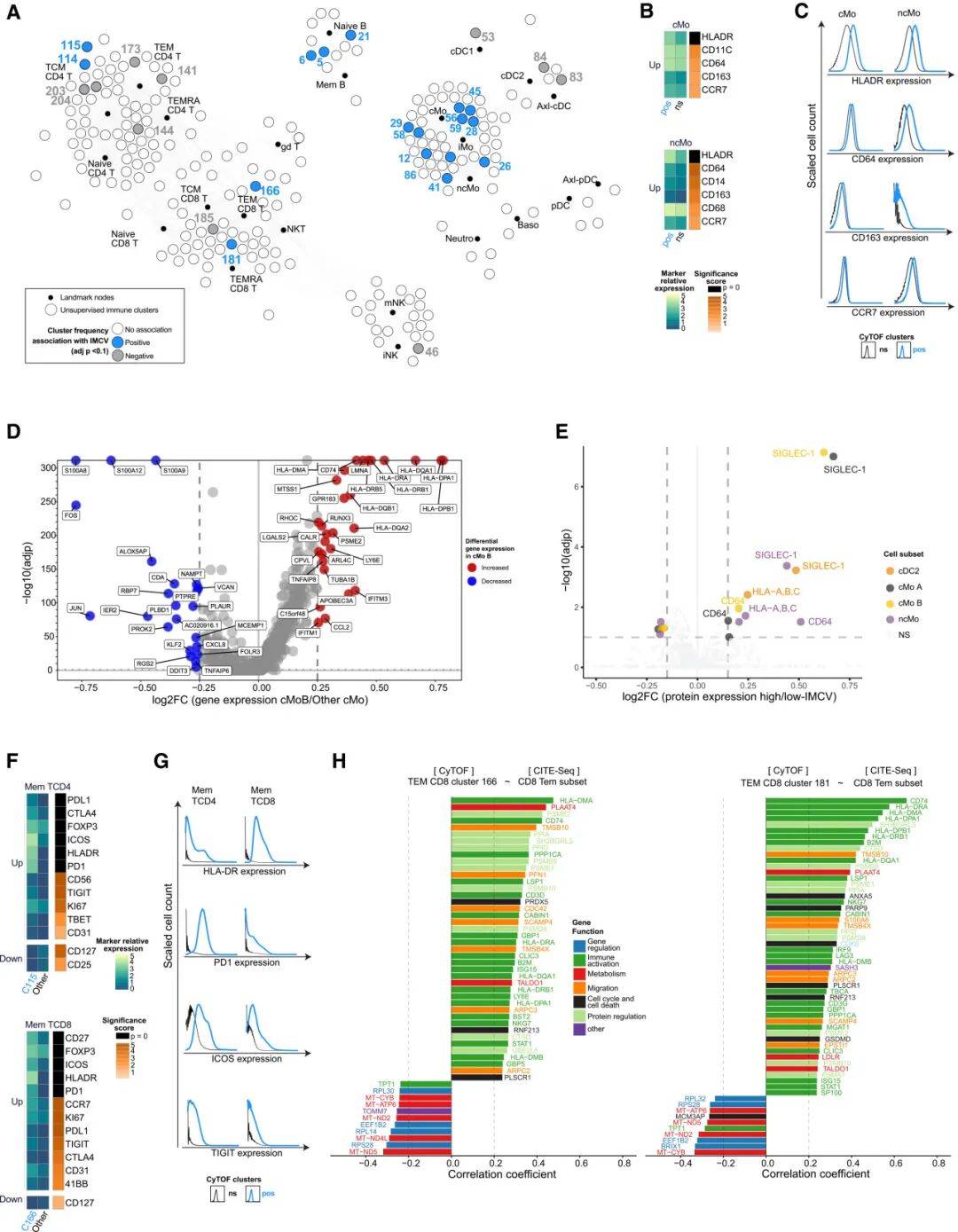
图3:IMCV队列中免疫细胞的活化状态
4、菌群代谢调控通路
肠道微生物群功能分析进一步揭示,多个具有免疫调节作用的代谢途径与IMCV密切相关。特定的微生物类群(如Bifidobacterium,Collinsella等)及其代谢产物(如短链脂肪酸(SCFA)、多胺、LPS 和初级胆汁酸)共同驱动IMCV相关的免疫调控。
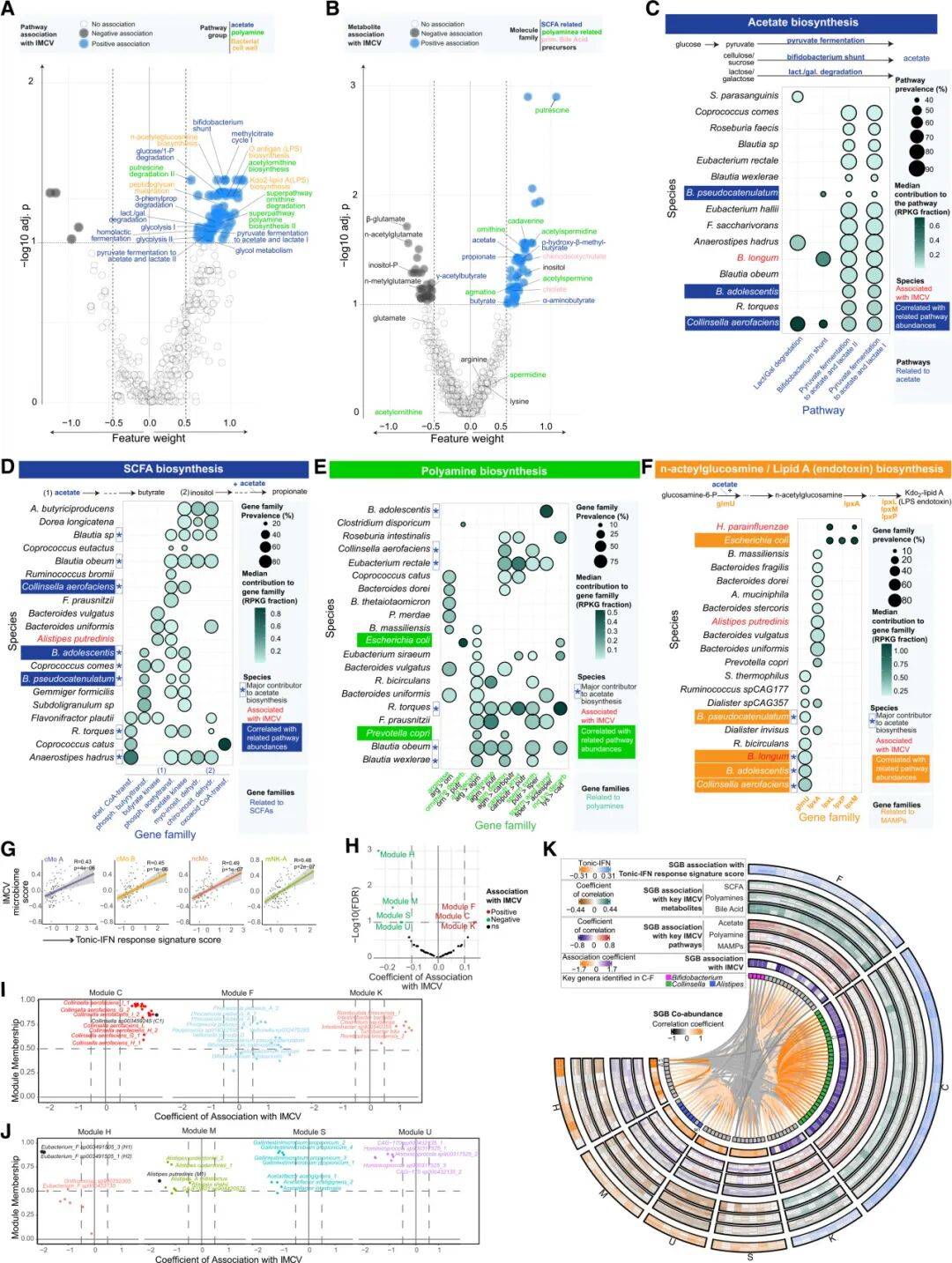
图4:IMCV队列中菌群代谢通路
5、免疫基线长期稳定
纵向随访分析提示,个体的IMCV特征及其相关的肠道菌群丰度随时间推移表现出高度稳定性。这表明“微生物-免疫基线”不是短暂波动的,而是每个人固有且长期存在的生物学指纹。
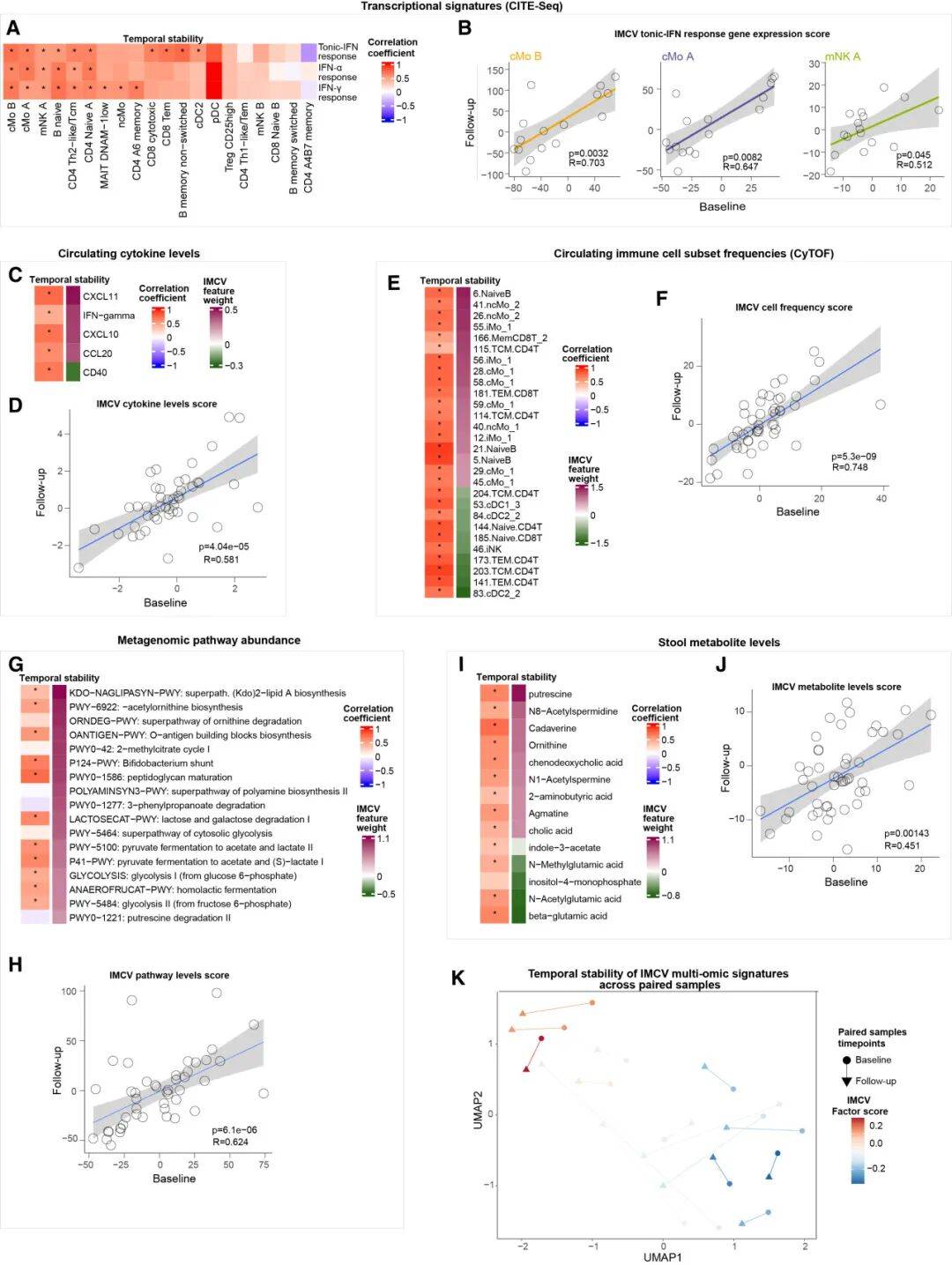
图5:IMCV特征长期稳定
文章小结
肠道菌群—免疫调控的核心机制
本研究通过全景多组学整合分析,系统解析了健康人群免疫基线差异的形成机制,证实肠道菌群及其代谢产物是调控个体免疫状态的核心因素。研究建立的免疫—微生物组协同变异轴(IMCV),不仅解释了人群中天然免疫力差异的底层逻辑,也为感染防御、疫苗响应、肿瘤免疫治疗异质性提供了全新解释框架。同时,研究证明免疫—菌群特征具备长期稳定性,可作为个体免疫表型的稳定标志物,为免疫调控、疾病风险预测与精准干预奠定了重要理论基础。
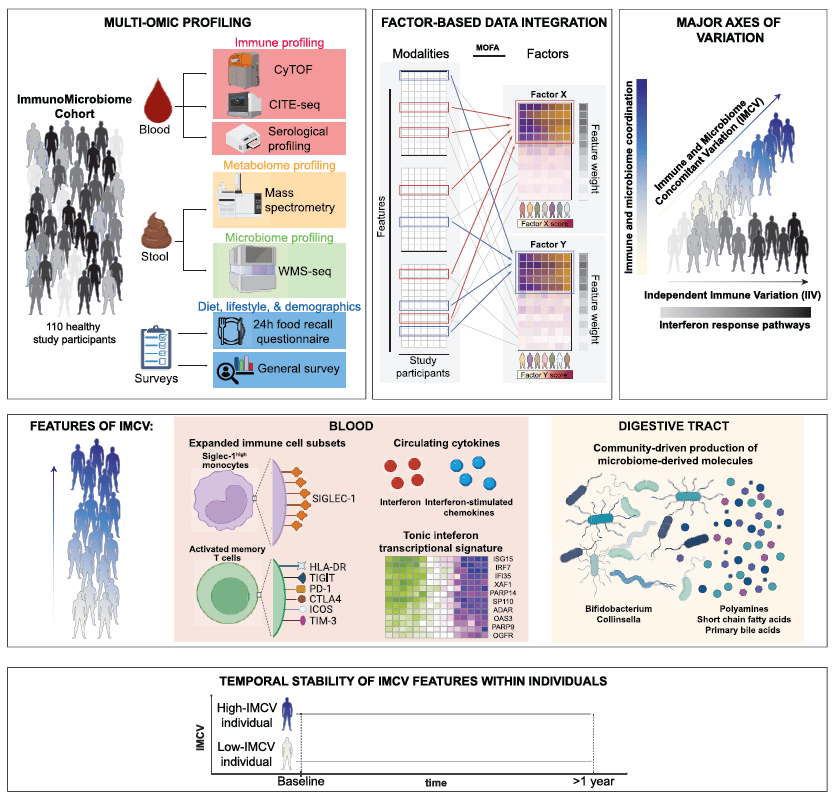
参考文献
Babdor J, et al. Immune-microbiome coordination defines interferon setpoints in healthy humans. Cell. 2026 Mar 9:S0092-8674(26)00168-6. doi: 10.1016/j.cell.2026.02.003.