

髓鞘损伤是脑衰老及多发性硬化症、阿尔茨海默病等多种神经退行性疾病的共同病理特征。目前已知葡萄糖代谢紊乱与髓鞘病变密切相关,但成熟少突胶质细胞通过何种代谢途径维持髓鞘功能,以及代谢异常为何会导致髓鞘修复失败,仍有待阐明。
2026年3月,陕西师范大学生命科学学院张媛、李星和闫亚平团队在Neuron期刊(IF:15.3)发表题为“Oligodendrocyte-encoded Lactate Dehydrogenase A Couples Glycolysis to Remyelination via Protein Lactylation”的研究论文。该文章阐明了糖酵解、乳酸化和成熟少突胶质细胞之间的代谢相互作用,并为目前缺乏有效治疗的脱髓鞘疾病提供了新的治疗视角。拜谱生物为该研究提供了乳酸化修饰组学技术服务。

研究结果
1、少突胶质细胞分化代谢特征与脱髓鞘病理条件下的代谢重编程
研究人员对成熟少突胶质细胞(OL)和前体细胞进行转录组学检测,结果表明糖酵解是OL成熟期间的主要代谢途径。为研究脱髓鞘条件下成熟OLs的代谢变化,研究人员对多发性硬化症患者的OLs进行转录组学检测,结果表明脱髓鞘病变中乳酸合成和糖酵解效率被抑制,导致乳酸生成障碍,是髓鞘修复失败的关键诱因(图1)。
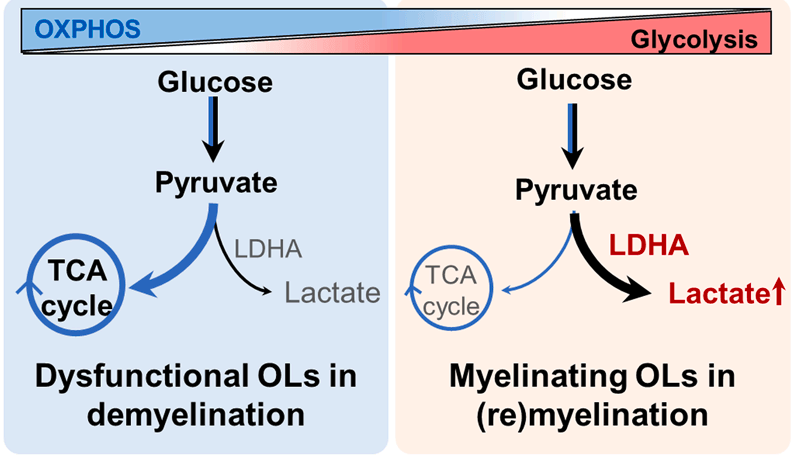
图1 脱髓鞘病理条件下的葡萄糖代谢重编程
2、乳酸促进前体细胞分化、中枢神经髓鞘生成和再髓鞘化
随后研究人员评估了糖酵解最终产物乳酸对前体细胞成熟的直接影响。在细胞和动物实验中均发现无论外源供给还是内源增强乳酸生成,均可有效驱动髓鞘生成和髓鞘修复。
3、乳酸通过蛋白质乳酸化促进前体细胞分化和髓鞘生成
研究人员证实了LDHA的活性及其产物乳酸在OL成熟和髓鞘化再生过程中,以细胞特异性和发育阶段依赖性的方式发挥着关键作用。
近些年乳酸化作为一种新型表观遗传修饰,在调控基因表达和细胞发育中起到重要作用。为阐明蛋白乳酸化在脱髓鞘作用中的作用,研究人员对铜松(CPZ)诱导脱髓鞘小鼠胼胝体进行蛋白质组和乳酸化修饰蛋白组检测。其中蛋白质组分析鉴定出252种差异表达的蛋白质,GO注释和KEGG分析发现“糖酵解/糖异生”等通路(图2A和B);乳酸处理上调MBP、PLP、ENPP61和LDHA等蛋白(图2C)。
乳酸化修饰和蛋白质组联合分析发现了560个蛋白上的2691个乳糖化位点,表明乳酸化是支撑再髓鞘化的表观遗传修饰机制。乳酸化蛋白主要定位于细胞质、细胞膜、线粒体和内质网(图2D),修饰主要集中在赖氨酸残基(图2E)。乳酸化参与髓鞘发育和代谢途径,这一全景剖析确定LDHA和CAII为关键靶点(图2F),并揭示了乳酸化作为一种广泛的调控机制,影响着对再髓鞘化至关重要的多种细胞功能。
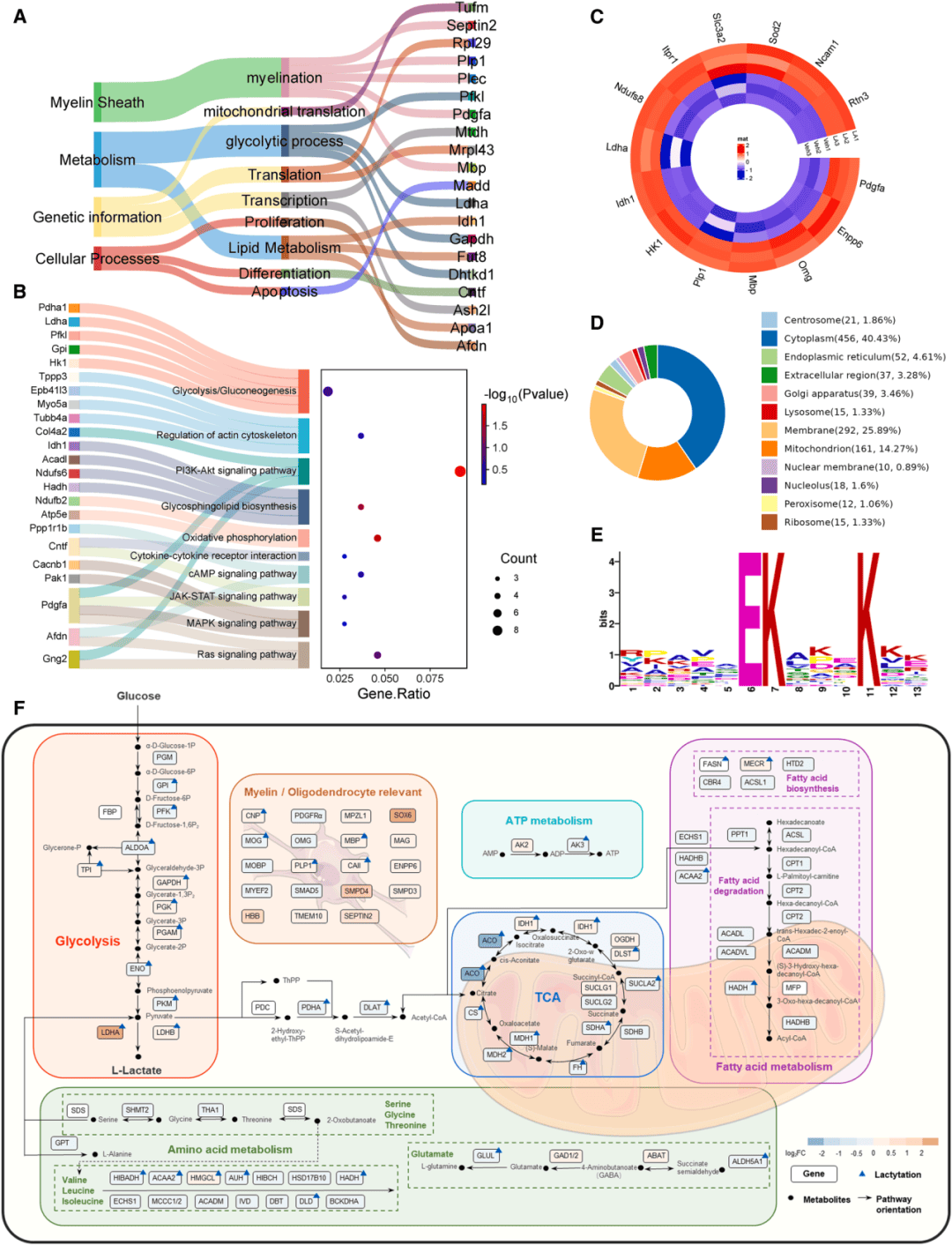
图2 CPZ诱导脱髓鞘小鼠胼胝体乳酸化全景图
4、LDHA通过乳酸化将糖酵解与OL的成熟偶联
研究人员选择了糖酵解中的关键酶LDHA进一步进行质谱分析发现赖氨酸残基K5和K232处的乳酸化(图3)。
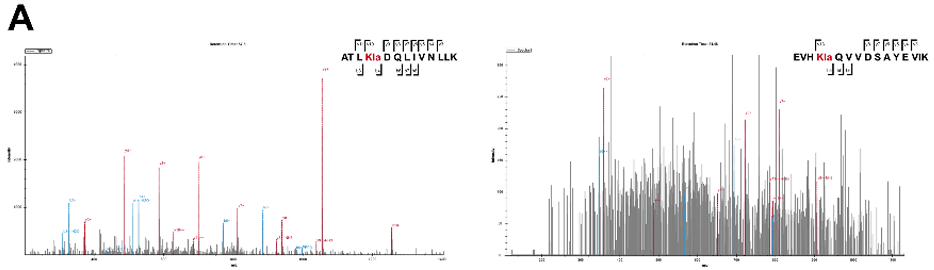
图3 LDHA上K5和K232乳酸化
此外还确定了CAII在K251的乳化(图4A),WB结果显示K251R是主要乳化位点(图4B)。CAII-WT的过表达显著增强前体细胞分化,而CAII-K251R的过表达则消除了这一效应(图4C和D)。LDHA-WT或非活性突变K232R(LDHA-K232R)共表达FLAG-CAII。LDHA增加了CAII乳酸化,而LDHA-K232R则完全消除了LDHA过度表达对CAII乳酸化的促进作用(图4E)。上述结果表明,LDHA乳化可以促进CAII乳化,从而将糖酵解与分化联系起来。
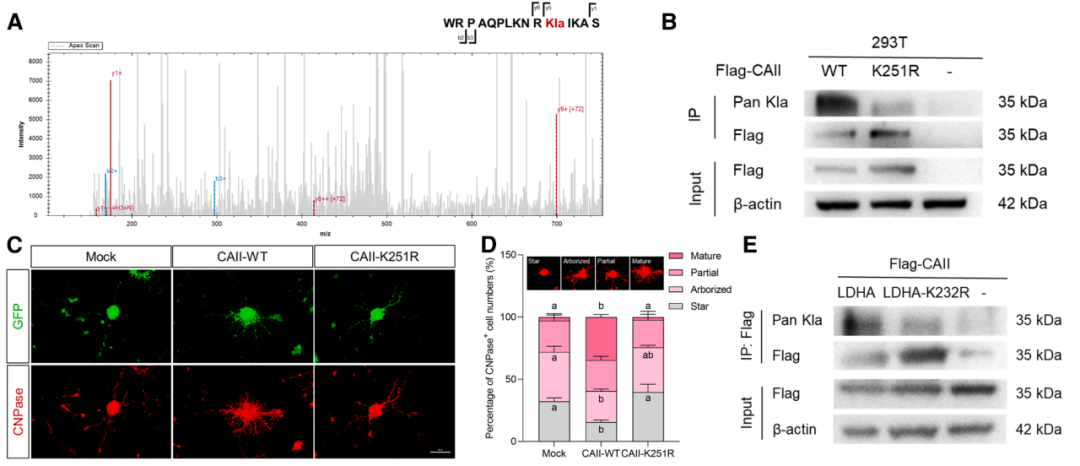
图4 CAII乳酸化突变体促进再髓鞘化
拜谱小结
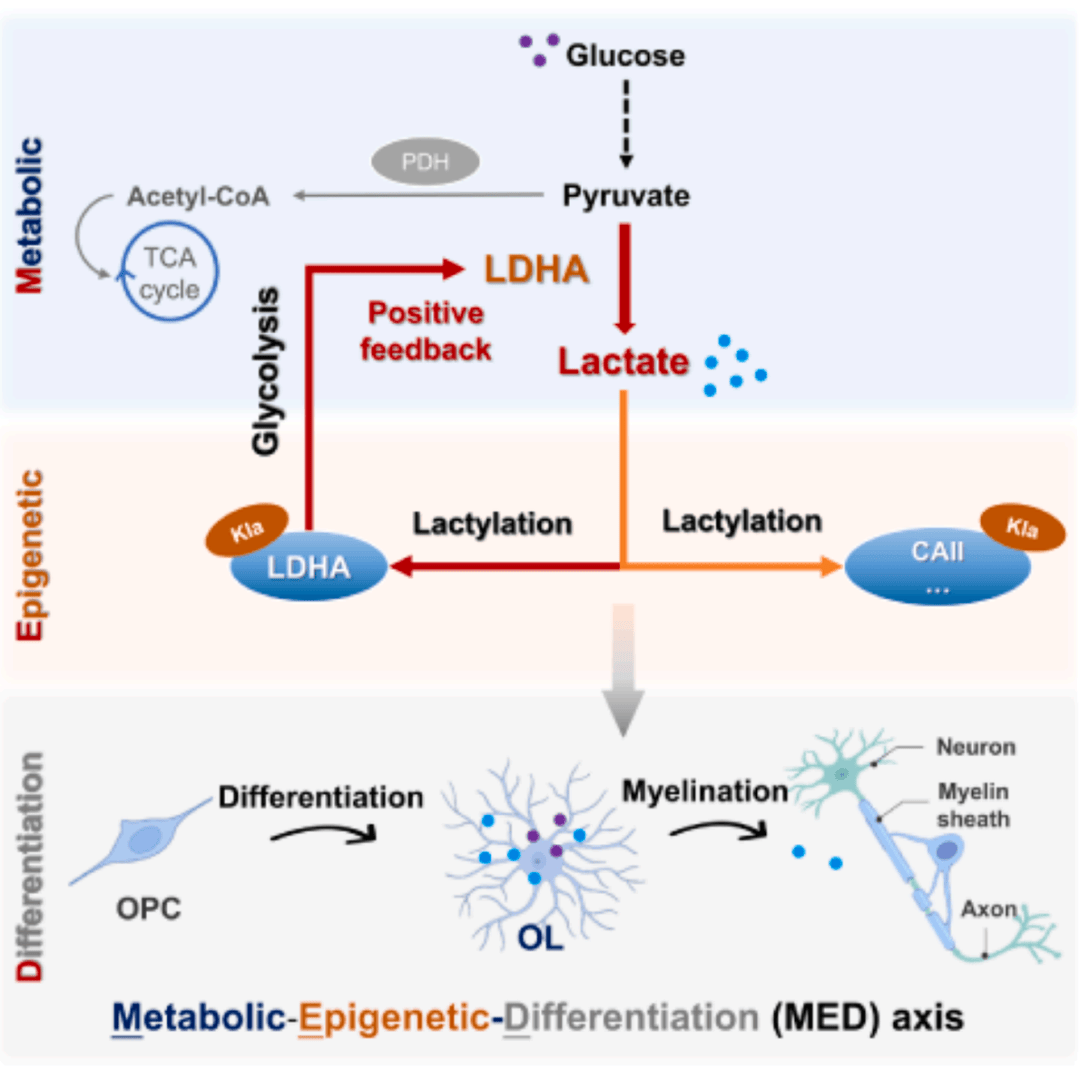
该研究绘制了脱髓鞘病灶的乳酸化修饰图谱,并构建了“代谢模式转换-表观遗传修饰-细胞分化增强”调控网络,阐明了中枢神经系统脱髓鞘中的乳酸和乳酸化功能,为理解髓鞘再生提供了全新研究视角并为脱髓鞘疾病的治疗提供了极具转化潜力的干预靶点。拜谱生物为其提供乳酸化修饰蛋白组学技术服务。
拜谱生物作为国内领先的多组学服务公司,可提供完善成熟的蛋白质组学、修饰蛋白质组学、代谢组学、转录组学等多组学产品技术服务体系,整合多组学数据进行深入挖掘分析,全面解析机制机理等,助力高分文章发表,欢迎致电咨询。
参考文献
Bao MY, Li XQ, Sun QQ, et al. Oligodendrocyte-encoded lactate dehydrogenase A couples glycolysis to remyelination via protein lactylation. Neuron. 2026 Mar 16:S0896-6273(26)00137-6. doi: 10.1016/j.neuron.