

半胱氨酸是构成蛋白质的含硫氨基酸,巯基是蛋白质残基中最具反应性的基团,可以发生可逆的氧化反应,如二硫键(S-S)形成、S-谷胱甘肽化(SSG)、S-亚硝基化(SNO)、S-次磺酸化(SOH)、S-硫巯基化(SSH)和棕榈酰化等。这些氧化还原修饰能够可逆地调节蛋白活性、互作与定位,进而实现对诸多生命活动的精细调控。在生理条件下,半胱氨酸氧化还原维持着动态平衡,而这些平衡失调则与许多重大疾病(如癌症、糖尿病、心血管疾病、神经退行性疾病等)存在密切关联。在2024年半胱氨酸修饰研究领域中,有诸多具有深远意义的科研成果。
此前,拜谱生物已对2024年度棕榈酰化修饰组高分文献进行盘点(年终盘点必收藏|2024年棕榈酰化高分文献及研究思路总结),本次关注S-谷胱甘肽化、S-亚硝基化、S-次磺酸化和S-硫巯基化,精选了多篇高分文献进行分享,希望能为各位科研工作者的研究提供帮助。
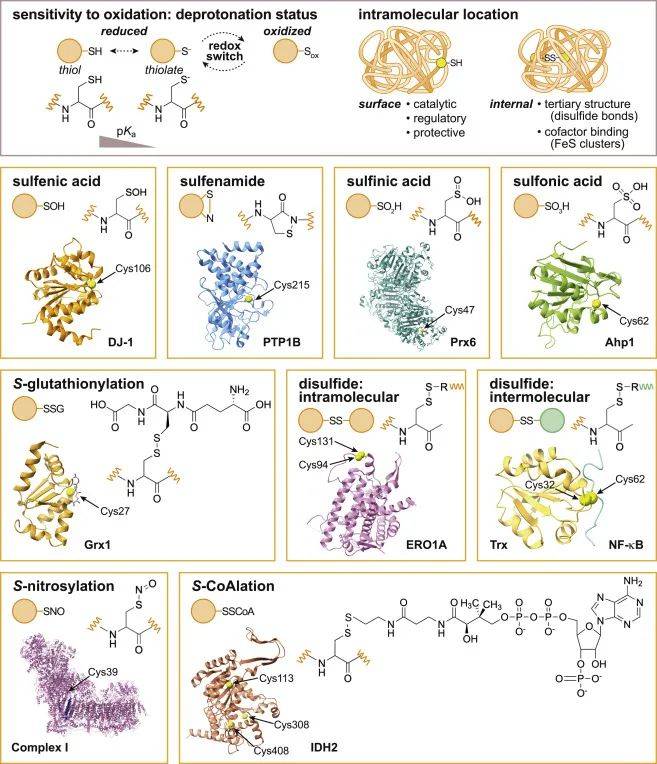 图1 半胱氨酸的氧化修饰
图1 半胱氨酸的氧化修饰
(图源:Lennicke C, et al., Mol Cell.,2021)
1. 亚硝基化修饰
1小胶质细胞激活诱导NO信号传导并改变细胞外囊泡中的蛋白质S-亚硝基化模式
文章标题:Microglial activation induces nitric oxide signalling and alters protein S-nitrosylation patterns in extracellular vesicles
发表期刊:J Extracell Vesicles (IF=15.5)
研究概述:神经炎症是神经退行性疾病的一个潜在特征,通常出现在疾病的早期病因中。活化的小胶质细胞EVs的亚硝基化修饰蛋白质组尚未被研究。研究人员在确定NO信号传导诱导神经炎症的蛋白质翻译后修饰。从脂多糖处理的小胶质细胞中分离的EV使用质谱进行质谱表面成像,此外还进行碘标记和比较蛋白质组学分析,以鉴定翻译后S-亚硝基化修饰。质谱成功鉴定了脂多糖处理的小胶质细胞衍生的EV蛋白中通过NO信号修饰的半胱氨酸游离巯基。此外,iodoTMT蛋白质组学分析显示,来自脂多糖处理的小胶质细胞的EV携带指示神经炎症的S-亚硝基化蛋白。这些包括已知的NO修饰蛋白和与脂多糖诱导的小胶质细胞激活相关的蛋白,这些蛋白可能在神经炎症通讯中起重要作用。结果表明活化的小胶质细胞可以在神经炎症期间通过EV的选择性包装导致广泛的NO信号变化。
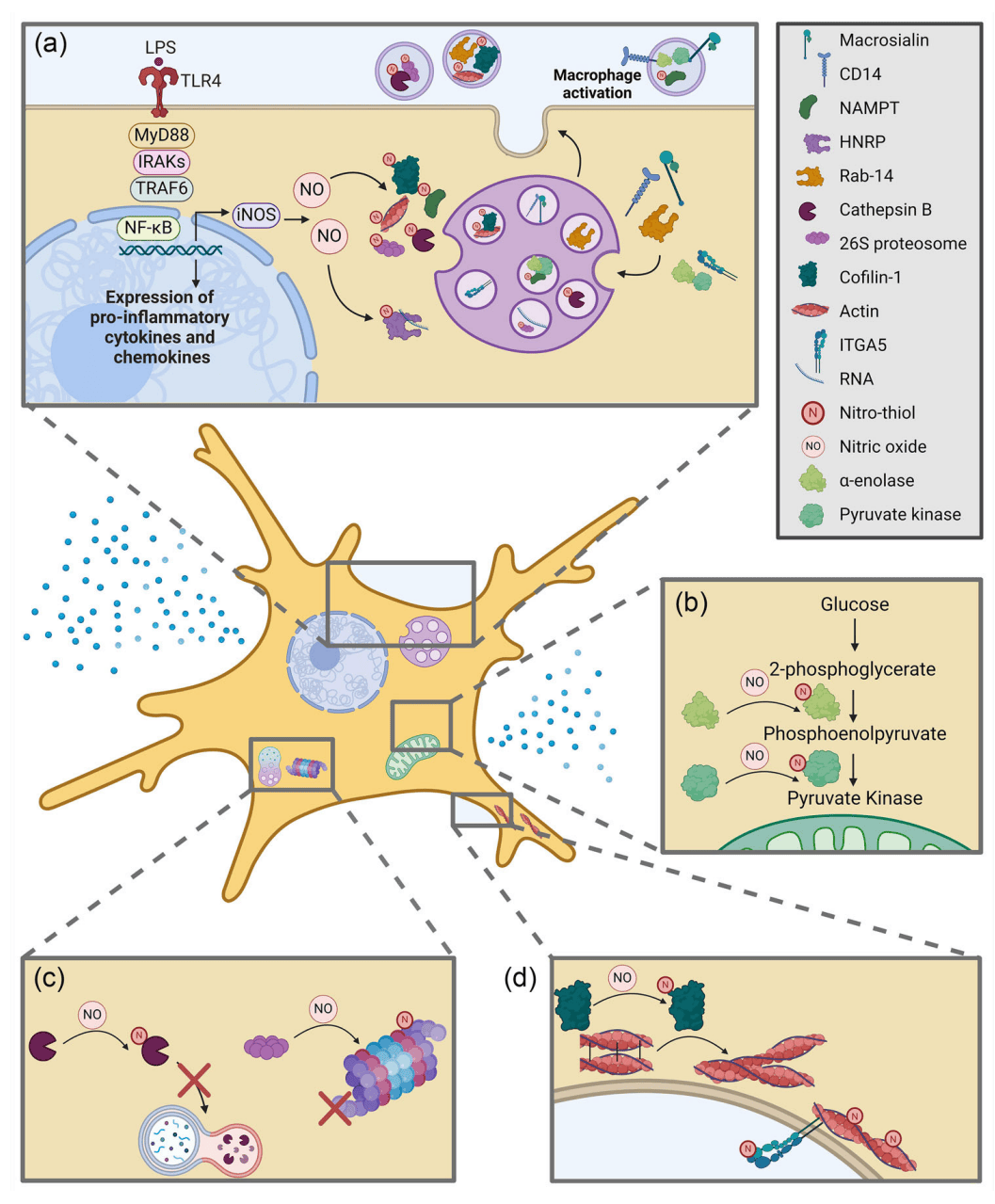 图2 神经炎症信号通过S-亚硝基化改变小胶质细胞
图2 神经炎症信号通过S-亚硝基化改变小胶质细胞
(图源:Vassileff N, et al., J Extracell Vesicles,2024)
2轮式跑步运动通过下调雄性大鼠基底外侧杏仁核中Gephyrin的 S-亚硝基化来缓解焦虑样行为
文章标题:Wheel-Running Exercise Alleviates Anxiety-Like Behavior via Down-Regulating S-Nitrosylation of Gephyrin in the Basolateral Amygdala of Male Rats
发表期刊:Adv Sci (Weinh) (IF=14.3)
研究概述:体育锻炼对焦虑症有有益的影响,但潜在的分子机制在很大程度上仍然未知。研究发现高焦虑大鼠基底外侧杏仁核中SNO-gephyrin水平显着升高,半胱氨酸212和284位SNO-gephyrin的下调产生抗焦虑作用。从机制上讲,Cys212或Cys284突变对SNO-gephyrin的抑制增加了GABA的表面表达一个Rγ2和GABA能神经传递,在雄性大鼠中发挥抗焦虑作用。另一方面,基底外侧杏仁核中神经元一氧化氮合酶的过表达消除了体育锻炼的抗焦虑样作用。
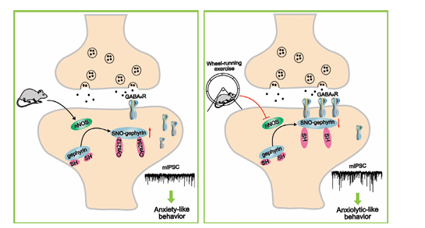 图3 体育锻炼对焦虑症治疗效果的分子机制
图3 体育锻炼对焦虑症治疗效果的分子机制
(图源:Yang PF, et al., Adv Sci (Weinh),2024)
2. 谷胱甘肽化
1GSTP通过KEAP1的S-谷胱甘肽化和NRF2通路的激活来减轻急性肺损伤
文章标题:GSTP alleviates acute lung injury by S-glutathionylation of KEAP1 and subsequent activation of NRF2 pathway
发表期刊:Redox Biol. (IF=10.7)
研究概述:氧化应激在急性肺损伤(ALI)的发病机制中起重要作用。研究发现GSTP介导的KEAP1 S-谷胱甘肽修饰过程增强解离KEAP1-NRF2相互作用,促进KEAP1-NRF2复合物的解离,从而促进NRF2核易位并激活下游蛋白表达,最终导致肺部炎症和损伤得到改善。GSTP是抗炎药开发的潜在靶点,并表明C434位点KEAP1的S-谷胱甘肽修饰在ALI的肺上皮细胞中起抗炎作用,揭示了肺上皮细胞在氧化应激下防止自我过度激活的潜在机制。
 图4 肺上皮细胞在氧化应激下防止自我过度激活的潜在机制
图4 肺上皮细胞在氧化应激下防止自我过度激活的潜在机制
(图源:Sun X, et al., Redox Biol.,2024)
3. 次磺酸化
1辐射促进S-次磺酸化驱动的抗原捕获以增强癌症免疫治疗
文章标题:S-Sulfenylation Driven Antigen Capture Boosted by Radiation for Enhanced Cancer Immunotherapy
发表期刊:ACS Nano. (IF=15.8)
研究概述:研究开发了一种高效的肿瘤抗原捕获纳米平台dAuNPs@CpG,可以显著改善肿瘤免疫治疗并诱导远隔效应。dAuNPs@CpG可以通过环己二酮和蛋白质次磺酸化之间的共价结合有效捕获放疗诱导的TDPAs,原位生成疫苗并将其排入淋巴结,促进DCs成熟和T细胞活化,实现对原发性和远处肿瘤的显着生长抑制以及PD-1阻断。与传统的Mal介导的捕获方法相比,由于产生大量次磺酸化TDPAs、强免疫原性和高抗肿瘤疗效,该方法在放疗诱导的原位疫苗接种方面具有相当大的优势。
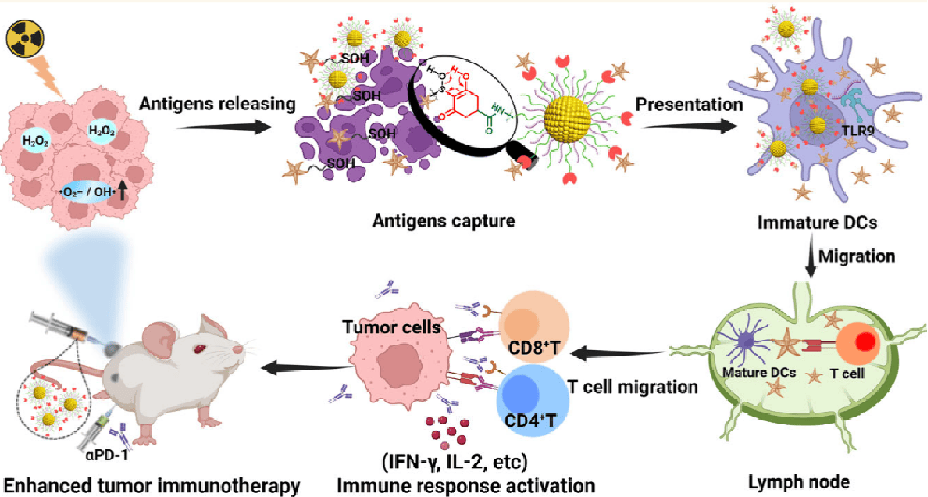 图5 辐射促进S-次磺酰化驱动的抗原捕获以增强癌症免疫治疗的机制
图5 辐射促进S-次磺酰化驱动的抗原捕获以增强癌症免疫治疗的机制
(图源:Sun X, et al., ACS Nano.,2024)
2H2O2次磺酸化CHE将局部感染与全身获得性耐药建立联系
文章标题:H2O2 sulfenylates CHE, linking local infection to the establishment of systemic acquired resistance
发表期刊:ACS Nano (IF=15.8)
研究概述:在植物中,局部感染可通过增加水杨酸(SA)的产生导致全身获得性耐药(SAR)局部感染后,转录因子CCA1 HIKING EXPEDITION(CHE)的保守半胱氨酸残基在全身组织中发生次磺酸化,这增强了它与SA合成基因启动子ISOCHORISMATE SYNTHASE1(ICS1)的结合,并增加了SA的产生。此外,通过NADPH氧化酶产生的H2O2是以浓度依赖性方式次磺酸化CHE的移动信号。SA和先前报道的信号分子(如N-羟基哌啶酸(NHP))的积累然后形成信号放大环以建立SAR。
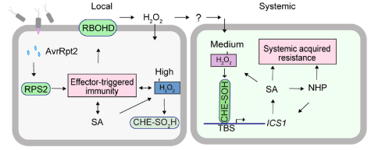 图6 H2O2次磺酸化CHE将局部感染与全身获得性耐药建立联系的机制
图6 H2O2次磺酸化CHE将局部感染与全身获得性耐药建立联系的机制
(图源:Sun X, et al., ACS Nano.,2024)
4. 硫巯基化
1H2S激活Keap1 S-硫巯基化和Nrf2通过SLC7A11/GSH/GPx4通路保护心肌细胞免受阿霉素诱导的铁死亡
文章标题:Hydrogen sulfide protects cardiomyocytes from doxorubicin-induced ferroptosis through the SLC7A11/GSH/GPx4 pathway by Keap1 S-sulfhydration and Nrf2 activation
发表期刊:Redox Biol. (IF=10.7)
研究概述:硫化氢(H2S)正在成为心血管系统中第三重要的气体介质。但是,H2S对阿霉素(DOX)诱导的铁死亡有影响仍然未知。内源性H2S的产生加剧了氧化还原稳态的破坏,并最终促进了DOX诱导的心肌细胞铁死亡。H2S上调SLC7A11/GSH/GPx4信号通路的活性,并通过协助GSH合成和减轻由于Keap1的S-硫巯基化和Nrf2的激活引起的脂质过氧化来防御DoIC中的铁死亡。
 图7 H2S激活S-硫巯基化保护心肌细胞免受阿霉素诱导的铁死亡的机制
图7 H2S激活S-硫巯基化保护心肌细胞免受阿霉素诱导的铁死亡的机制
(图源:Zhang H, et al., Redox Biol.,2024)
2GYY4137诱导的p65硫巯基化通过改善骨关节炎发展中的线粒体功能来保护滑膜巨噬细胞免受焦亡
文章标题:GYY4137-induced p65 sulfhydration protects synovial macrophages against pyroptosis by improving mitochondrial function in osteoarthritis development.
发表期刊:J Adv Res. (IF=11.4)
研究概述:GYY4137是一种新型且缓慢释放的硫化氢(H2S)具有可能调节骨关节炎进展的强效抗炎特性的供体,其潜在机制仍不清楚。研究发现GYY4137响应炎症刺激而增加NF-kB p65的硫巯基化,清除骨关节炎进展中的线粒体氧化应激来有效抑制滑膜巨噬细胞焦亡。GYY4137通过p65的氧化还原修饰参与抑制OA的NLRP3激活以调节炎症反应。
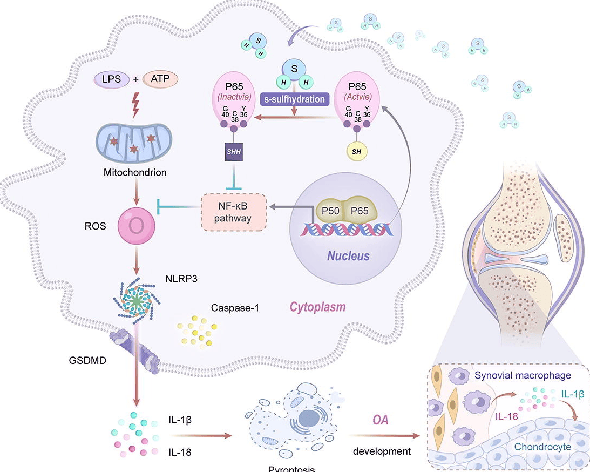 图8 GYY4137通过p65的硫巯基化修饰调节炎症反应的机制
图8 GYY4137通过p65的硫巯基化修饰调节炎症反应的机制
(图源:Zhang H, et al., J Adv Res.,2024)
拜谱小结
氧化还原反应本质上与能量代谢有关。因此,氧化还原过程对于生物体生理和生命本身都是不可或缺的。半胱氨酸氧化修饰介导氧化还原信号,从而调节细胞功能。此外,氧化还原信号还可以通过改变代谢酶和转录因子的活性以及调节基因表达、表观遗传修饰、昼夜节律等生理过程来控制细胞功能。在2024年的高分文献盘点中,多个研究团队研究半胱氨酸修饰,揭示了生命过程中的分子机制,为理解生物现象提供了理论基础。
拜谱作为国内领先的多组学服务公司,可提供基因组、转录组、蛋白组、代谢组等多组学服务。暨首家推出、国内唯一成熟商业化的棕榈酰化修饰蛋白组学后,拜谱生物研发团队经过反复实验,成功推出了亚硝基化、谷胱甘肽化、硫巯基化、次磺酸化、total氧化还原、游离巯基等修饰产品,构建了产品最全面、技术体系最成熟的半胱氨酸氧化还原系列修饰组学产品。拜谱生物半胱氨酸特色组学产品采用生物素交换法,能够更特异的结合修饰基团,大幅度提升修饰位点鉴定数目,并且进一步优化富集效率,提高半胱氨酸巯基稳定性,以提升低丰度修饰位点定量准确性,助力剖析半胱氨酸修饰的分子机制和调控作用,解析疾病相关分子机制等。欢迎各位老师前来咨询!!
参考文献
[1] Lennicke C, Cochemé HM. Redox metabolism: ROS as specific molecular regulators of cell signaling and function. Mol Cell. 2021 Sep 16;81(18):3691-3707. doi: 10.1016/j.molcel.2021.08.018B1
[2] Vassileff N, Spiers JG, Bamford SE, Lowe RGT, Datta KK, Pigram PJ, Hill AF. Microglial activation induces nitric oxide signalling and alters protein S-nitrosylation patterns in extracellular vesicles. J Extracell Vesicles. 2024 Jun;13(6):e12455. doi: 10.1002/jev2.12455B1
[3] Yang PF, Nie TL, Sun XN, Xu LX, Ma C, Wang F, Long LH, Chen JG. Wheel-Running Exercise Alleviates Anxiety-Like Behavior via Down-Regulating S-Nitrosylation of Gephyrin in the Basolateral Amygdala of Male Rats. Adv Sci (Weinh). 2024 Sep;11(34):e2400205. doi: 10.1002/advs.202400205B1
[4] Sun X, Guo C, Huang C, Lv N, Chen H, Huang H, Zhao Y, Sun S, Zhao D, Tian J, Chen X, Zhang Y. GSTP alleviates acute lung injury by S-glutathionylation of KEAP1 and subsequent activation of NRF2 pathway. Redox Biol. 2024 May;71:103116. doi: 10.1016/j.redox.2024.103116B1
[5] Zhu J, Li M, Zhang Y, Lv Z, Zhao Z, Guo Y, Chen Y, Ren X, Cheng X, Shi H. S-Sulfenylation Driven Antigen Capture Boosted by Radiation for Enhanced Cancer Immunotherapy. ACS Nano. 2024 Jul 27. doi: 10.1021/acsnano.4c02206
[6] Cao L, Karapetyan S, Yoo H, Chen T, Mwimba M, Zhang X, Dong X. H2O2 sulfenylates CHE, linking local infection to the establishment of systemic acquired resistance. Science. 2024 Sep 13;385(6714):1211-1217. doi: 10.1126/science.adj7249
[7] Zhang H, Pan J, Huang S, Chen X, Chang ACY, Wang C, Zhang J, Zhang H. Hydrogen sulfide protects cardiomyocytes from doxorubicin-induced ferroptosis through the SLC7A11/GSH/GPx4 pathway by Keap1 S-sulfhydration and Nrf2 activation. Redox Biol. 2024 Apr;70:103066. doi: 10.1016/j.redox.2024.103066
[8] Ma J, Yang P, Zhou Z, Song T, Jia L, Ye X, Yan W, Sun J, Ye T, Zhu L. GYY4137-induced p65 sulfhydration protects synovial macrophages against pyroptosis by improving mitochondrial function in osteoarthritis development. J Adv Res. 2024 Jun 4:S2090-1232(24)00223-6. doi: 10.1016/j.jare.2024.05.033