

年龄是老年人患病和残疾的一个关键风险因素。然而,相同实际年龄的个体往往表现出不同的生物衰老状态,导致不同的个体风险概况。基于组学数据和机器学习技术的年龄估计器,即衰老时钟,为解释分子水平的生物衰老提供了一个有价值的框架。代谢组学能全面分析生物样品中的小分子代谢物,提供与生理和病理过程相关的当前代谢状态的见解。受外界环境因素影响的代谢物是基因表达和酶活性的最终产物。因此,与表观遗传学、转录组学和蛋白质组学相比,代谢组学在组学研究中更接近衰老表型,为衰老的量化提供了丰富的生物学信息。
2024年11月,上海交通大学卜军课题组和新加坡国立大学Brian K. Kennedy等合作在Cell Metabolism杂志(27.7)上发表“Decoding aging clocks: New insights from metabolomics”的文章,本文综述了代谢组学衰老时钟方法的发展,重点介绍了代谢组学衰老时钟的建立和解释,同时强调了它们的优势、局限性和应用,并讨论了它们潜在的生物学意义,这有可能推动长寿研究和开发的创新。

Part.01、衰老时钟代谢组学方法
选择合适的生物样本
衰老是一个复杂的过程,在不同的生物体、组织和细胞类型中以不同的速率和部分不同的机制发生。目前,所有的代谢组学衰老时钟都是通过生物体液(如血液、尿液和脑脊液)构建的。
血液是循环系统的重要组成部分,作为重要的运输介质,有效地在全身循环营养物质和代谢产物,从而维持生理稳态和代谢平衡。血液的代谢组学特征可作为一面镜子,提供对发生在不同器官、组织和细胞结构中的各种病理生理过程的见解。在标准做法中,空腹全血样本在清晨采集,随后处理以获得血清或血浆。然后将这些标本小心地保存在生物库的超低温(即-80°C)下。血清在制备过程中需要一个凝血过程,在此过程中血小板活化可以释放物质(如脂质和磷脂酶),凝血过程中持续的糖酵解和代谢可导致葡萄糖水平降低和乳酸水平升高。收集血浆时,常用的抗凝剂包括肝素、EDTA和柠檬酸盐。有研究认为肝素管会在质谱中引入化学噪声;EDTA可能在核磁共振(NMR)分析中引入额外的信号并错误地增加样品中的肌氨酸浓度;柠檬酸盐会阻碍内源性分析物如柠檬酸盐及其衍生物的分析。在运输或储存过程中,如果不能将温度保持在-80°C,会导致脂质变化、半胱氨酸消耗和RNA降解产物的积累。此外,经历3-4次以上的冻融循环可能会影响血脂、氨基酸等代谢物的浓度。
与血清或血浆相比,尿液具有亲脂分子浓度较低和极性化合物丰度较高的特点,为代谢组学研究提供了独特的分析优势。尿液中含有多种内源性废物代谢物、食物、药物、环境污染物和细菌副产品。鉴于肾脏过滤和浓缩各种代谢物进入尿液的能力,基于尿液的代谢组学为开发检测泌尿系统退化的衰老时钟提供了一个有希望的窗口。建议采集中段晨尿样本,最好是在无菌干燥容器中。尽管尿液样本在室温下可保持24小时的代谢稳定,在-20℃或更低的温度下可保持3个月的代谢稳定,但仍建议在适当的条件下相对快速地冷冻,以获得最佳的代谢组学分析。
代谢组学平台选择
代谢组学数据采集主要涉及非靶向和靶向NMR或质谱方法。非靶向代谢组学用于检测、鉴定和量化广泛的代谢物,而不考虑预先存在的假设。这种方法的结果很大程度上受到样品制备、分离技术和仪器设置等因素的影响,特别是在没有先验知识的情况下,需要明智的选择和细致的文件。然而,非靶向代谢组学通过揭示新的衰老相关代谢特征,为衰老时钟研究提供了相当大的希望。另一方面,靶向代谢组学侧重于一组特定的代谢物,利用同位素标记的内部标准或外部校准曲线进行定量。一旦代谢物panel确定,分析工作流程和参数进行优化,以提高灵敏度和特异性。
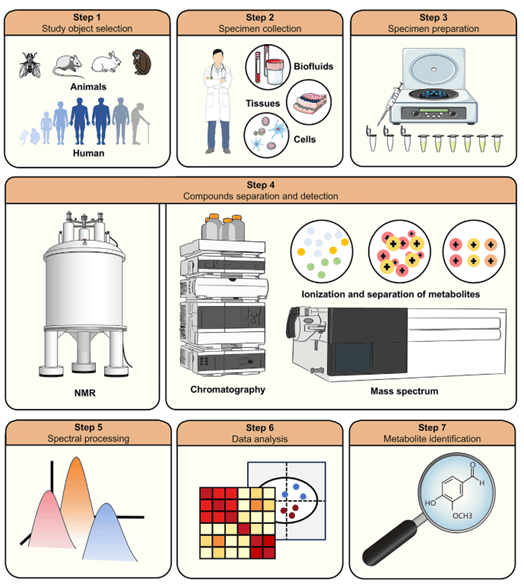 图1 代谢组学衰老时钟研究流程
图1 代谢组学衰老时钟研究流程
(图源:Huang et al., Cell Metabolism, 2024)
Part.02衰老时钟的进展:建立、评估和应用
准备代谢组学数据进行分析
在经典的衰老时钟研究中,实足年龄作为因变量,通过具有一系列综合特征的机器学习技术进行预测,得出一个被称为生物年龄的估计年龄。当基于代谢组学时,这种估计被称为代谢年龄。该过程的关键是代谢组学数据的预处理,解决诸如代谢组学漂移(由于样品降解或实验变化等因素),批次效应(由不同处理和测量批次引起),异常值/缺失值管理以及数据归一化和转换等问题。考虑到模型构建过程中确定最佳方法的复杂性,建议对代谢组学衰老时钟研究中预处理方法的报告进行标准化,并提供详细的解释,以提高这一领域的研究质量和可比性。
衰老时钟开发中的机器学习
在衰老时钟研究的典型机器学习工作流程中,研究队列被划分为子集,用于训练、验证和测试。模型在训练集上进行训练,使用验证集(或交叉验证等重新采样技术)来选择最优的预测模型。最后的测试集用于评估模型的性能。利用代谢组学方法,产生了大量的代谢组学特征。然后使用各种机器学习算法(包括线性和非线性方法)处理这些特征,以构建预测模型(图2A)。多元线性回归(MLR)是预测生物年龄的基本统计方法,其中实足年龄估计为加权代谢特征的线性函数。MLR在计算上很简单,具有很高的可解释性,权重表明了每个特征对年龄预测的影响方向和大小。然而,组学数据固有的复杂性和稀疏性给MLR带来了巨大的挑战,特别是当特征数量显著超过样本数量时,如在非靶向代谢组学数据中经常看到的那样,或者当同一途径中代谢物之间存在高度共线性时。解决方案包括大样本量、严格的特征选择或主成分分析(PCA)等降维技术。
实际年龄和代谢物之间的非线性关系往往更准确地反映了现实世界的动态(图2B)。研究发现了代谢物随年龄变化的多种非线性模式,包括成年前黄嘌呤和组氨酸代谢的强劲增长趋势,以及单酰基甘油和黄体酮类固醇代谢的抛物线型趋势。这就需要在衰老时钟模型中使用非线性机器学习算法。支持向量机(SVM)和决策树及其扩展(如随机森林和极端梯度增强)等算法已经有效地应用于代谢组学数据集。深度学习模型在分析大规模数据集中复杂的非线性关系方面显示出巨大的前景。
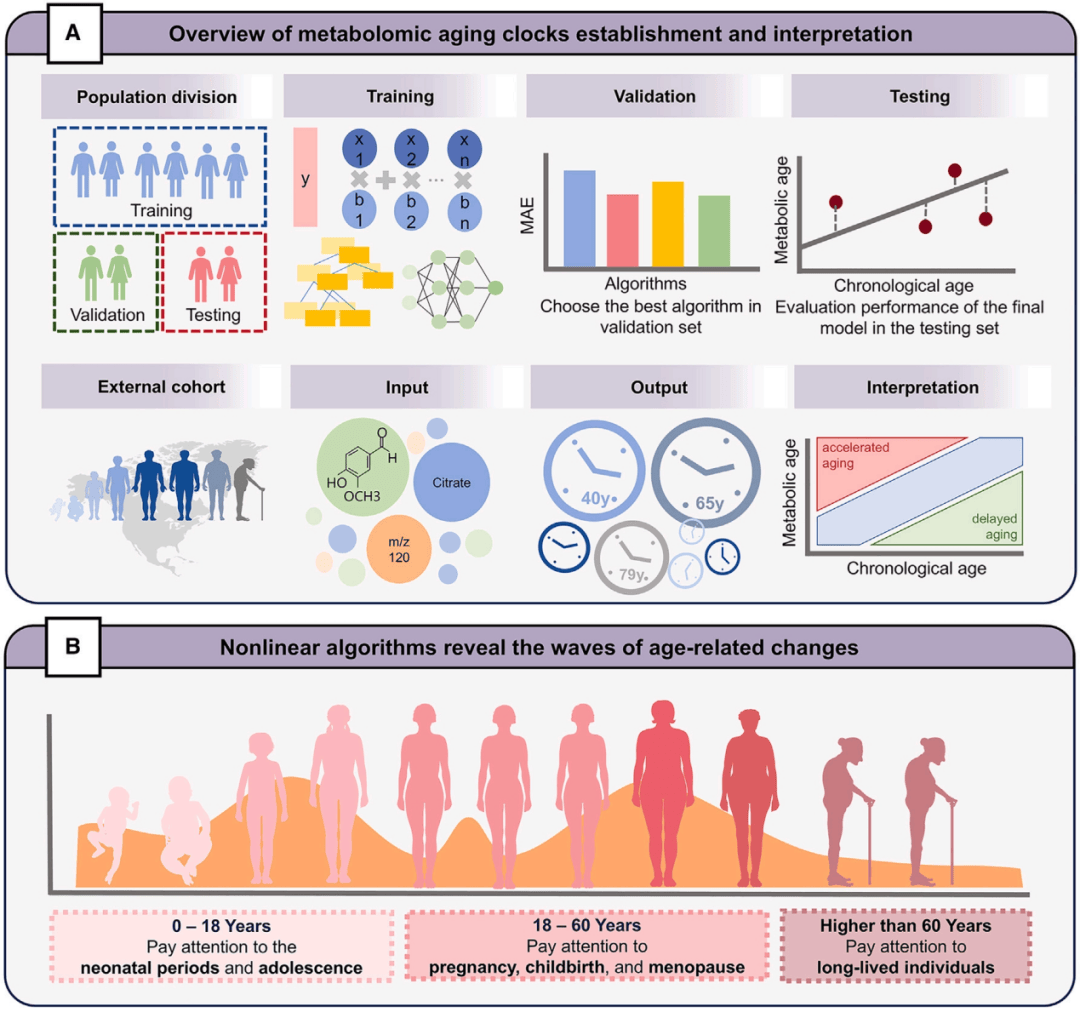
图2 代谢组学衰老时钟的开发和分析。(A) 开发和评估代谢组学衰老时钟的标准程序,强调了机器学习技术在其构建和测试中的应用。(B) 实际年龄与生物标志物:说明了实际年龄与代谢组学生物标志物之间的非线性关系,强调了非线性算法在构建更准确和反映代谢组学衰老时钟方面的适用性。
(图源:Huang et al., Cell Metabolism, 2024)
衰老时钟的实际应用
大众:保持日常生活习惯。许多研究探讨了生活方式因素对人体代谢物的影响。例如,睡眠剥夺是现代社会普遍存在的问题,它已被证明会显著提高27种代谢物的水平:色氨酸、血清素、牛磺酸、8种酰基肉碱、13种甘油磷脂和3种鞘脂。在日常生活中,这些因素相互作用,代谢组学衰老时钟的概念可以作为一个综合框架来整合和理解它们的整体影响。值得注意的是,吸烟和饮酒与加速生物衰老有关,这表明这些时钟有可能反映日常行为对代谢年龄的累积影响。
预防医学专家:疾病和死亡风险预测。衰老时钟在预测未来疾病发生、进展和死亡率方面具有重要潜力,因此在风险分层和告知公共卫生政策方面发挥着至关重要的作用。最近有超过10万名参与者的大规模研究强调了代谢组学在使用核磁共振衍生谱预测常见疾病方面的有用性,包括代谢、血管、呼吸、神经系统疾病和癌症等广泛的疾病。代谢年龄是一种全面的、可改变的代谢衰老标志物,能够识别出各种衰老相关疾病,特别是心脏代谢疾病的高风险个体。
临床医生:评估身体功能和指导决策。传统上,治疗决定以实际年龄为指导,导致老年人倾向于采用保守方法。然而,这可能会导致那些尽管年事已高,却可以从更积极的治疗中受益的人错过机会。因此,生物年龄的概念在这种情况下变得至关重要。例如,65岁以下的股骨颈骨折患者一般被定义为“年轻患者”,而75岁以上的患者被定义为“老年患者”。对于介于两者之间的患者,其损伤前的生理状态决定了其被分类为“年轻”或“老年”患者。对于年轻患者,手术治疗目标通常是保留股骨头并实现骨愈合,而髋关节置换术通常更适合老年人。然而,可以想象的是,70岁甚至80岁的健康状况良好且代谢年龄较年轻的患者可能从股骨头保存中获益更多,可能显著改善他们未来的生活质量。因此,衰老时钟可以作为许多传统实验室测试的替代品,为临床决策提供更全面的视角。
研究人员:评估抗衰老干预措施。衰老时钟的开发主要是为了量化抗衰老干预措施的功效,为评估抗衰老干预措施提供了一种创新的选择。代谢组学衰老时钟提供了两个显著的优势:它们对外部影响的敏感性允许在短期干预后评估急性衰老变化,并且某些代谢物对衰老的既定因果关系有助于对年龄变化的生物学解释。因此,代谢组学衰老时钟有望评估抗衰老干预措施(图3)。
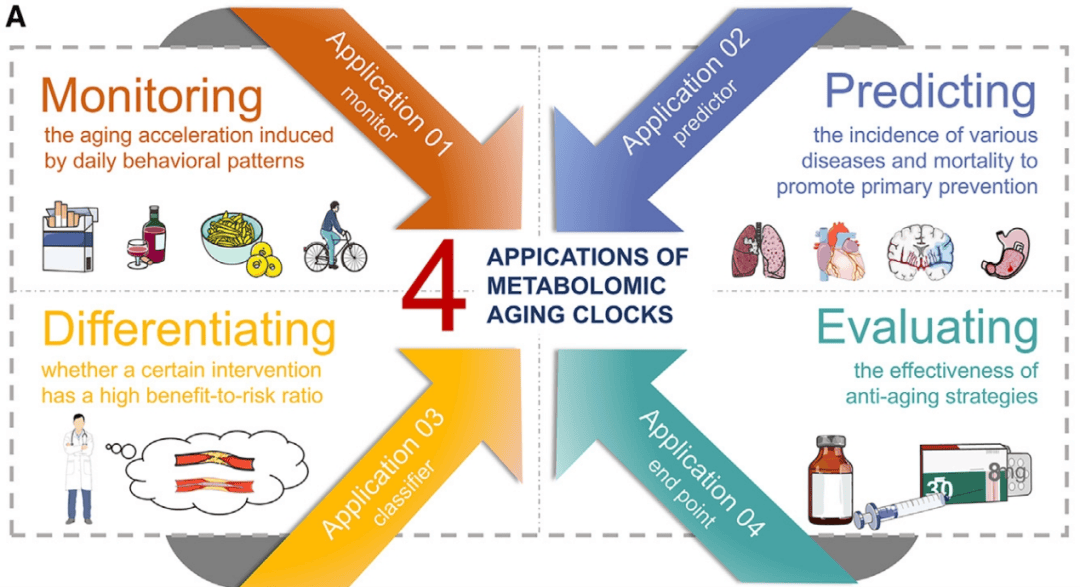
图3 代谢组学衰老时钟在各个领域的应用。生活方式影响评估:评估日常行为如何影响衰老加速。疾病和死亡率预测:利用时钟预测疾病发病和死亡率,协助初级预防战略。干预益处-风险分析:根据生理年龄而不是实际年龄区分医疗干预的适宜性。抗衰老策略评价:评估各种抗衰老方法的疗效。
(图源:Huang et al., Cell Metabolism, 2024)
Part.03衰老时钟生物学见解
虽然实际年龄与许多代谢物的变化有关,但这并不一定意味着因果关系。混杂因素(如人口统计、生活方式和健康状况)可能扭曲年龄与代谢物之间的关系,使这些代谢物无法准确反映衰老过程。此外,衰老标志物并不一定是有害的——它们也可以代表对衰老的中性反应,甚至是适应性反应。例如,a-酮戊二酸在老年人中增加,但已显示出改善衰老表型的潜力。同样的复杂性也适用于胰岛素和成纤维细胞生长因子-21 (FGF21),它们与衰老的关系是多方面的,不能仅仅通过它们在不同年龄组中的水平来捕捉。建立在因果关系基础上的衰老时钟可以更好地反映体内促衰老和抗衰老力量之间的动态平衡,指导有针对性的抗衰老干预。
代谢组学衰老时钟在衰老机制研究中具有巨大的潜力,因为已知许多小分子具有抗衰老作用,例如NAD+增强剂,如烟酰胺核苷(NR)和NMN,它们已经在抗衰老市场上获得了突出地位。常见的氨基酸如牛磺酸可以通过多种机制促进长寿,包括减少细胞衰老,防止端粒酶缺乏,改善线粒体功能。甘氨酸可以增强自噬,有助于其抗衰老作用。相反,限制支链氨基酸的摄入已显示出促进健康衰老的潜力。孟德尔随机化(MR)为识别代谢物与衰老之间的潜在因果关系提供了一种有价值的大规模方法。代谢组学和相关方法的不断发展有望更深入地了解衰老的生物学机制和代谢物-衰老关系的因果关系。这一进展有望将分子机制与临床应用更紧密地联系起来。
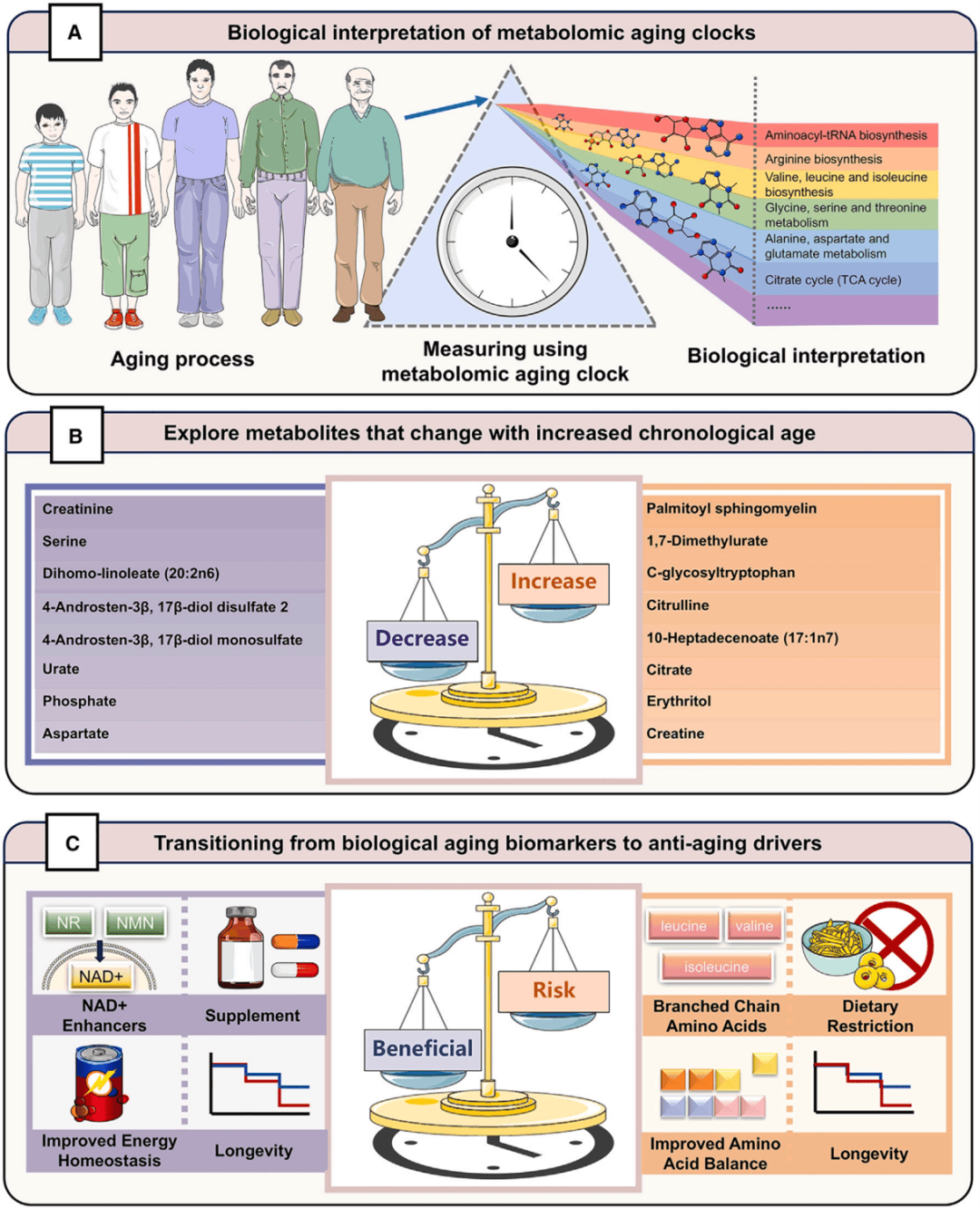
图4连接代谢组学衰老时钟与分子机制。 (A) 连接代谢组学衰老时钟的关键代谢特征与特定代谢物和代谢途径的过程说明。(B) 代谢物在人体内表现出与年龄相关的增加或减少。(C) 探索代谢物与衰老之间的因果关系是对衰老时钟进行生物学解释的关键一步。NAD+,烟酰胺腺嘌呤二核苷酸;NR,烟酰胺核苷;NMN,烟酰胺单核苷酸。
(图源:Huang et al., Cell Metabolism, 2024)
Part.04总结
本综述深入阐述了代谢组学衰老时钟的新兴领域,探索了与这些时钟相关的方法、建模复杂性和解释的细微差别,同时将它们与衰老的潜在分子机制联系起来。代谢组学作为测量生物衰老的关键工具,在衰老研究中提供了有前途的干预目标。尽管代谢组学衰老时钟取得了显著进展,但技术改进和模型增强仍有很大的空间。我们确定了未来探索和发展的三个关键领域:开展全面的纵向研究;结合来自不同生物标本和平台的数据来揭示衰老的普遍性和特异性;构建强大的框架,将代谢组学与其他组学数据整合到衰老时钟研究中。应对这些机遇和挑战对于充分利用这一快速发展领域的潜力至关重要。这些努力将为更好地理解健康老龄化铺平道路,最终为个人和社会的福祉做出贡献,并弥合老龄化和健康长寿方面的前沿研究与现实应用之间的差距。
Part.05拜谱小结
代谢组学是一个有趣且快速发展的研究领域,涉及体内小分子的全面分析,并提供最终的基因组与环境相互作用的结果。因此,利用代谢组学来表征生物衰老并构建衰老时钟具有巨大的潜力。拜谱生物作为国内领先的多组学公司,可提供完善成熟的代谢组学检测服务,包括基于 LC-MS和GC-MS的非靶向代谢组学、医学高通量靶向代谢组学(可定量检测1000余种医学常见代谢物)、医学高通量靶向脂质组学(可定量检测4000余种脂质分子)等,结合丰富的生信分析和机器学习技术,可为衰老时钟的构建、生物标志物的筛选等研究提供全面的服务。欢迎咨询。
参考文献:
Huang H, Chen Y, Xu W, et al. Decoding aging clocks: New insights from metabolomics. Cell Metab. Published online December 5, 2024. doi:10.1016/j.cmet.2024.11.007B1