

胶质母细胞瘤(GBM)是人类最致命的恶性肿瘤之一,癌症干细胞(CSC)表型的出现是肿瘤长久治疗的主要挑战。高脂饮食(HFD)会导致侵袭性疾病的发生,并伴随着肿瘤干细胞的富集和生存期的缩短。由于影响CSC人群的环境和生活方式因素尚不清楚,本研究试图评估饮食对CSC富集的影响。
2021年7月,美国克利夫兰诊所勒纳研究所的Daniel J Silver等在Journal of Clinical Investigation发表了题为“Severe consequences of a high-lipid diet include hydrogen sulfide dysfunction and enhanced aggression in glioblastoma”的文章。该研究通过非靶向脂质组学、基因组学和硫巯基化蛋白质组学分析发现饮食可通过限制代谢适应性来改变的H₂S信号,从而抑制GBM的生长。同时,H₂S的缺失会引发CSC富集和疾病加速,因此增加H₂S生物利用度可能会改善GBM患者的预后。

文章名称:Severe consequences of a high-lipid diet include hydrogen sulfide dysfunction and enhanced aggression in glioblastoma
期刊:Journal of Clinical Investigation
发表时间:2021年7月
影响因子:15.9
研究材料:小鼠
组学技术:非靶向脂质组学、硫巯基化蛋白质组学
一、研究思路
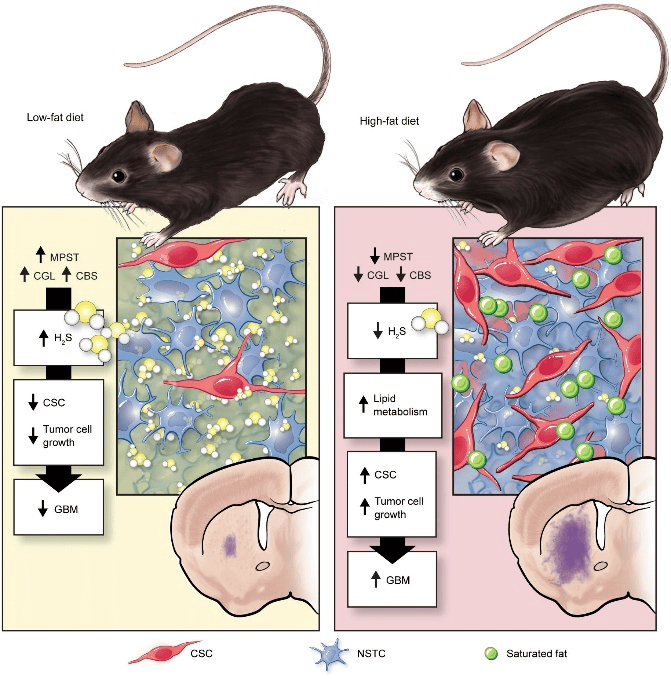
二、研究结果
1.HFD消耗对干细胞的影响
前期通过小鼠实验发现HFD消耗加速了胶质母细胞瘤的发生频率并可能导致脑内脂质富集,进而通过非靶向脂质组学分析小鼠中脂质变化(图1A),主要包括两种模式:一种是HFD喂养的携带肿瘤的小鼠中特异性富集的脂质,另一种是无论是否存在肿瘤,通常在HFD喂养的小鼠中富集的脂质(图1B-C)。同时,在过量脂质中生长的GBM细胞被诱导进入过度增殖状态并表现出增强的自我更新(图1D-G)。综上所述,本研究发现HFD消耗驱动干细胞表型富集。
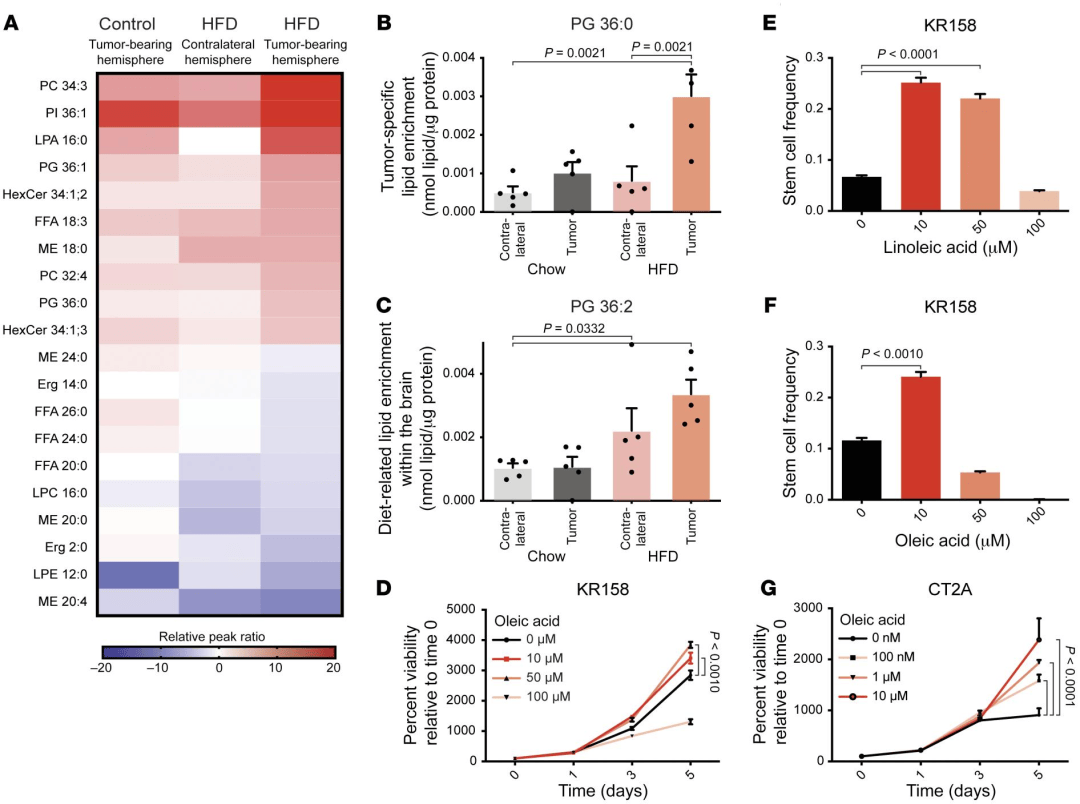 图1 HFD消耗对干细胞的影响
图1 HFD消耗对干细胞的影响
2.饮食对H₂S的影响
长期摄入HFD会抑制气体递质H₂S的产生,H₂S是半胱氨酸代谢的副产物,也是转硫代谢途径的一个特征(图2A)。实验表明HFD喂养的肿瘤小鼠的大脑中的H₂S合成减少了约50%(图2B)。通过基因组图谱的数据,确定了H₂S合成酶(CBS和MPST)的表达与神经胶质瘤相关(图2C-E)。研究表明H₂S是一种与GBM组织相关的重要因子。
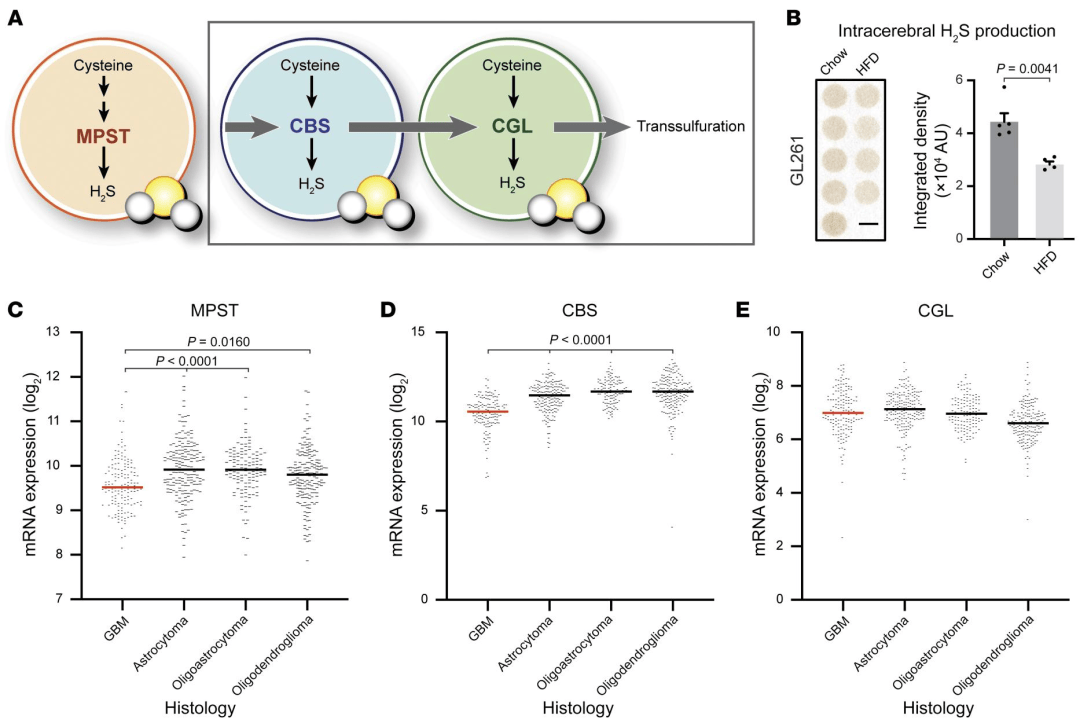 图2 饮食对H₂S的影响
图2 饮食对H₂S的影响
3.H₂S的抑制对细胞代谢的影响
为了探究H₂S的抑制在人类样本上可能起到的作用,本研究通过测定脑组织中H2S的含量发现人类的GBM组织产生大约50%的这种关键肿瘤抑制因子(图3A)。硫巯基化修饰蛋白质组分析发现GBM组织中S-硫巯基化蛋白的数量显著减少(图3B),并且KEGG通路分析将S-巯基化蛋白质景观分层为生化途径(图3C)。另外,研究发现H2S合成的长期抑制增加了组织的生物能(图3D-G)。这些结果表明S-硫巯基化作用的丧失增强了GBM组织的代谢和生物能,使肿瘤能够利用因HFD消耗而积累的饱和脂肪。
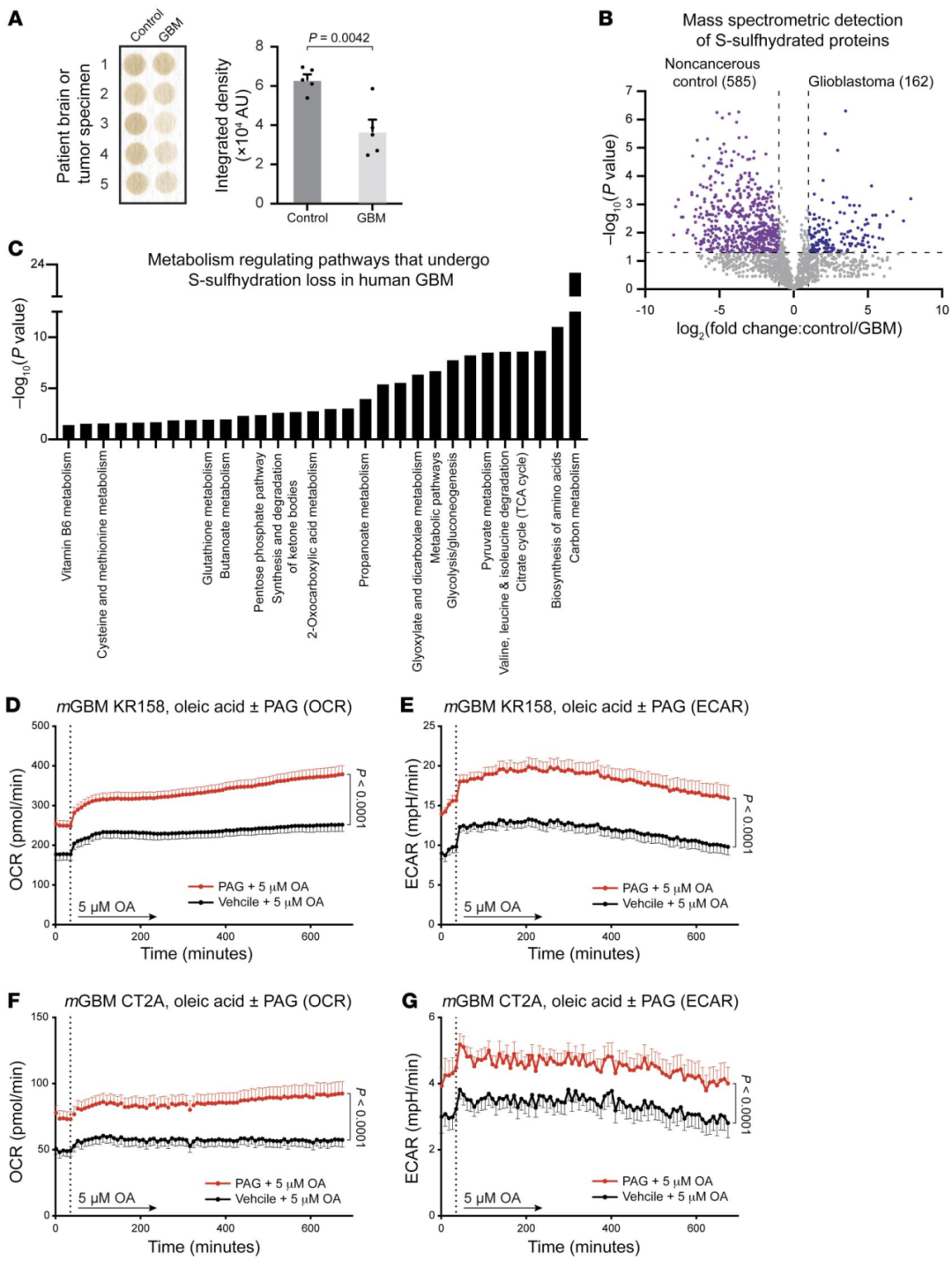 图3 H₂S抑制对细胞代谢的影响
图3 H₂S抑制对细胞代谢的影响
三、小结
本研究证明了喂食HFD会导致小鼠大脑营养状况的改变,由此导致的S-硫巯基化作用的丧失使肿瘤能够利用因HFD消耗而积累的饱和脂肪。同时,脑和肿瘤微环境的变化诱导了CSC的富集、化疗耐药性的增加和GBM进展的加快。
四、拜谱小结
H₂S是机体产生的重要调节信号分子。H₂S诱导的半胱氨酸S-硫巯基化是一种重要的翻译后修饰,通过多种信号通路参与细胞保护,H₂S引起这种修饰的机制研究很大程度上仍然缺乏。拜谱生物全面升级了半胱氨酸修饰蛋白质组学产品,现可提供硫巯基化修饰蛋白质组学等检测服务,欢迎大家咨询!
参考文献:Silver DJ, Roversi GA, Bithi N, et al. Severe consequences of a high-lipid diet include hydrogen sulfide dysfunction and enhanced aggression in glioblastoma. J Clin Invest. 2021;131(17):e138276. doi: 10.1172/JCI138276.