

帕金森病(PD)是一种复杂且日益流行的中枢神经系统(CNS)神经退行性疾病。它从运动前阶段(以非运动症状为特征,如快速眼动睡眠行为障碍)发展到运动失能阶段。临床上需要客观的早期/前期运动疾病阶段的生物标志物,以干预和减缓潜在的神经退行性过程。外周液体生物标志物侵入性较小、易于获得,可用于重复和长期监测,这对于即将进行的神经保护试验的人群的筛查是必要的。
2024年6月18日,英国伦敦大学学院儿童健康研究所和英国伦敦大奥蒙德街医院的Hällqvist Jenny等人在Nature Communications上在线发表了题为“Plasma proteomics identify biomarkers predicting Parkinson’s disease up to 7 years before symptom onset”,文章采用无偏倚的最先进的质谱法,通过比较PD患者于健康对照(HC)的血浆样本,发现PD患者血浆中存在早期炎症特征。此后,通过创建高通量和靶向蛋白质组学分析进入验证阶段,该分析应用于来自独立复制队列的样本,包括新发PD, HC和孤立的快速眼动睡眠行为障碍(iRBD)患者,机器学习模型通过分析八种血液生物标志物,准确识别所有帕金森患者,并在运动发病前7年对79%的运动前个体进行分类。这些生物标志物中有许多与症状严重程度相关。这种特殊的血检显示了早期阶段的分子事件,可以帮助识别有风险的参与者,进行旨在减缓/预防运动帕金森氏症的临床试验。

英文标题:Plasma proteomics identify biomarkers predicting Parkinson’s disease up to 7 years before symptom onset(Nature Communications,IF=14.70,2024)
中文标题:血浆蛋白质组学鉴定在症状出现前7年预测帕金森病的生物标志物
研究材料:健康及患者血浆样本
组学技术:非靶向蛋白组、MRM靶向蛋白组
主要研究结果
1. 蛋白质组学发现阶段(第0阶段)
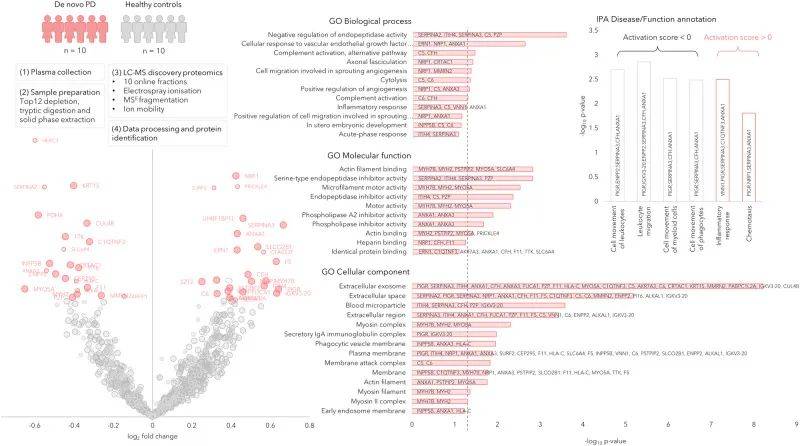
发现队列由10名随机选择的drug-naïve PD患者和10名匹配的HC患者组成。使用无标记质谱分析,对血浆进行了自下而上的蛋白质组学分析。该分析确定了1238个蛋白质,限制鉴定来自每个蛋白质至少一个肽和每个肽至少两个片段。在排除具有少于两个独特肽或识别分数低于设定阈值的蛋白质后,剩下895种不同的蛋白质。在这些蛋白质中,有47种是显著不同的(图1-2)。通路分析表明在几个炎症通路中富集。
 (图源:Hällqvist et al., Nature Communications, 2024)
(图源:Hällqvist et al., Nature Communications, 2024)
图1. 研究的整个工作流程。这项研究包括三个阶段。第0阶段包括通过非靶向质谱法发现蛋白质组学,以鉴定假定的生物标志物,随后是第1阶段,从发现阶段的目标转移到靶向质谱MRM方法,并应用于新的更大的样本队列,最后是第2阶段,改进靶向MRM方法,分析更多的样本,以评估靶向蛋白质组的临床可行性
 (图源:Hällqvist et al., Nature Communications, 2024)
(图源:Hällqvist et al., Nature Communications, 2024)
图2. 新发PD(n = 10)和健康对照(n = 10)的血浆样品中的发现阶段,由火山图表示,显示PD和对照之间的蛋白质表达差异(阶段0)。显示了重要蛋白质的 GO 注释,虚线表示 p = 0.05。显示了 IPA 的疾病和功能注释,分为具有正或负激活评分的注释
2.选择目标蛋白质组学分析的蛋白质
接下来,基于发现阶段确定的潜在生物标志物开发了一种经过验证的高通量和多重质谱靶向蛋白质组学检测方法。该测定中还包括其它蛋白质,其中一些蛋白质已在先前的PD,阿尔茨海默病(AD)和衰老的发现研究中被发现。此外,还纳入了文献中鉴定的几种已知的促炎和抗炎蛋白,这些蛋白先前已发展成为内部靶向蛋白质组神经炎症组。使用这种方法,我们创建了一个靶向蛋白质组学面板。这项靶向蛋白质组学和多重分析包括121种蛋白质,旨在验证生物标志物并探测在发现阶段被确定为受干扰的途径(图3)。
 (图源:Hällqvist et al., Nature Communications, 2024)
(图源:Hällqvist et al., Nature Communications, 2024)
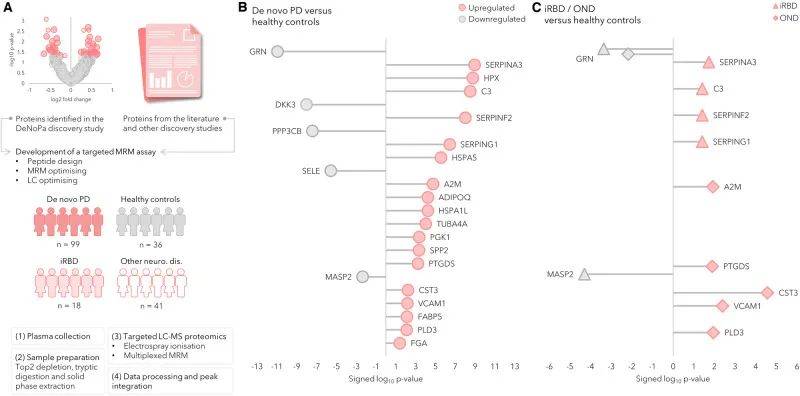
图3. 新发帕金森病(PD)受试者、健康对照(HC)以及其他神经系统疾病 (OND) 和孤立性 REM 睡眠行为障碍(iRBD)的验证队列的工作流程和目标蛋白质组学分析结果概述
3.目标蛋白质组学验证阶段(第1阶段)
对于靶向蛋白质组学分析,使用独立于蛋白质组学发现步骤的血浆样本,来自99名最近诊断为新发PD的个体(48名男性,50%,平均年龄67岁)和36名健康对照(HC;男性20人,57%,平均年龄64岁)。这是主要队列。又增加了进一步的样本进行验证,包括41名患有其他神经系统疾病(OND)的患者(29名男性,71%,平均年龄70岁)和18名vPSG确诊的iRBD患者(10名男性,56%,平均年龄67岁)。
4. 鉴定新生帕金森病患者和健康对照者之间显著差异表达的生物标志物-靶向蛋白质组学验证阶段(第1阶段)
开发了针对121种蛋白质的靶向蛋白质组学分析,其中32种在血浆中一致且可靠地检测到。在这32个标志物中,有23个被证实在PD和HC之间有显著差异表达。在iRBD患者和HC之间以及OND和HC之间的比较中发现了6种差异表达蛋白(图3)。新生PD和iRBD组均表现出丝氨酸蛋白酶抑制剂SERPINA3、SERPINF2和SERPING1以及中心补体蛋白C3的上调表达。与HC相比,颗粒蛋白前体蛋白在所有三组患者(PD, iRBD和OND)中均下调。OND组和PD组的PTGDS、CST3、VCAM1和PLD3蛋白表达相同且上调。图4用Box-scatter图显示了显著不同的蛋白质。
 (图源:Hällqvist et al., Nature Communications, 2024)
(图源:Hällqvist et al., Nature Communications, 2024)
图4. 对照组和不同疾病组之间的蛋白质显著不同:新发PD(DNP)、iRBD 和 OND(II 期)。数据显示为Box-scatter,叠加着各个测量值的散点图
5. 差异表达蛋白的生物学意义——靶向蛋白质组学验证阶段(第1阶段)
使用通路分析(Ingenuity pathway analysis [IPA], Qiagen)评估了差异表达蛋白的参与及其对生物过程的影响。确定了三个主要的途径簇,包括(i) 丝氨酸蛋白酶抑制剂或丝氨酸蛋白酶以及补体和凝血成分的表达,(ii) 内质网 (ER) 应激/热休克相关蛋白和 (iii) VCAM1、SELE 和 PPP3CB 的表达。最高的富集分数包括急性期反应信号通路、凝血系统、补体系统、LXR/RXR 激活、FXR/RXR 激活和糖皮质激素受体信号传导,这些都是参与炎症反应的途径。
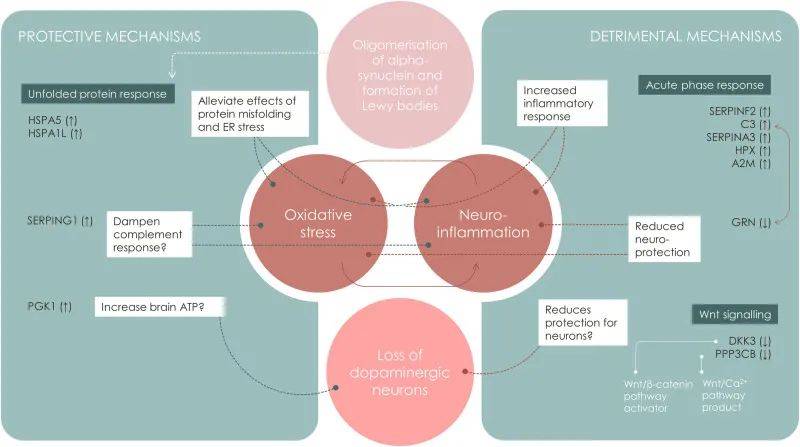
炎症相关通路(包括补体系统和急性期反应)表现出最高的显著性水平,其次是调节蛋白质折叠、内质网应激和热休克蛋白的途径。蛋白质和通路的网络表示显示由炎症/凝血/脂质代谢(FXR/RXR 和 LXR/RXR)、热休克蛋白/蛋白质错误折叠以及与 Wnt 信号传导和细胞外基质蛋白相关的更多异质性通路簇组成的簇。根据本研究中观察到的蛋白质表达,推测发生的潜在有害和保护机制,导致神经元路易体内含物中α-突触核蛋白的寡聚化和积累,并最终导致多巴胺能神经元细胞丢失(图5)。
 (图源:Hällqvist et al., Nature Communications, 2024)
(图源:Hällqvist et al., Nature Communications, 2024)
图5 提示差异表达蛋白参与神经元突触核蛋白疾病
6.使用蛋白质生物标志物的多重蛋白质组合预测新发帕金森病——靶向蛋白质组学验证阶段(第1阶段)
接下来,应用机器学习,使用验证阶段的PD和HC样本构建判别OPLS-DA模型。样本聚类为两个截然不同且分离良好的类别,对模型的评估表明其非常显著。对类分离影响最大的蛋白质是GRN、DKK3、C3、SERPINA3、HPX、SERPINF2、CAPN2、SERPING1和SELE。
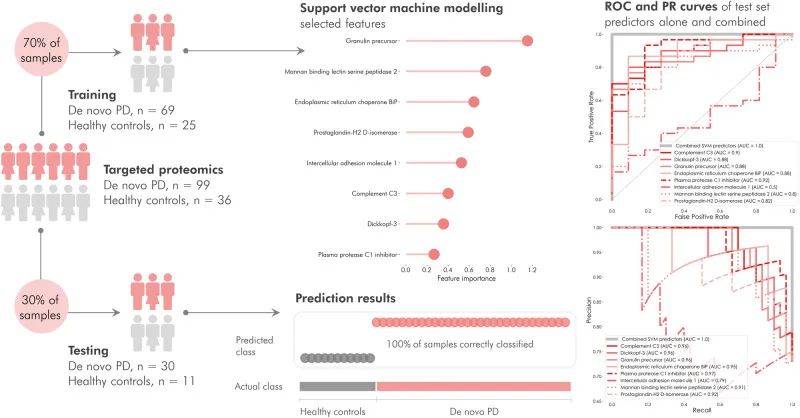
随后,我们探讨了观察到的蛋白质表达是否可用于构建能够预测个体是属于PD组还是HC组的回归模型。确定了一组以100%准确率区分PD和HC的蛋白质,然后构建了线性支持向量分类模型并应用递归特征消除来查明最具歧视性的变量。数据分为两部分:一部分用于模型训练,其中70%用于模型训练,另一部分包含30%用于测试。各部分保持PD和对照样品的比例。模型中包含的特征数量由特征排序确定,并在训练数据集中交叉验证递归特征消除。特征选择产生了一个具有八个预测因子的模型:GRN、MASP2、HSPA5、PTGDS、ICAM1、C3、DKK3 和 SERPING1。在模型中预测训练数据,并导致所有样本被分类到正确的类别中。我们进一步构建了受试者工作特征(ROC)和精确回忆(PR)曲线,以说明每种蛋白质区分PD和HC的能力,并将其与组合多重蛋白质组合的能力进行比较。组合面板在ROC和PR曲线上均实现了1.0的AUC。ROC曲线中单个预测因子的AUC范围为0.53至0.92,PR曲线中的AUC范围为0.79至0.96(图6)。通过对数据进行6次拆分和 40 次重复的重复交叉验证来进一步评估整个数据集。由此产生的分类指标的精确度、召回率、F1分数和平衡准确率得分的平均值和标准差分别为 0.87±0.09、0.87±0.08、0.86 ±0.09 和 0.82±0.12,从而表明了一个高度稳健的分类模型。
 (图源:Hällqvist et al., Nature Communications, 2024)
(图源:Hällqvist et al., Nature Communications, 2024)
图6 PD和对照受试者的线性支持向量分类(第一阶段)。测试集中单个和组合蛋白质的受试者工作特征(ROC)和精确召回率(PR)曲线表明,单个蛋白质的 ROC 曲线下面积 (AUC) 值为 0.53–0.92,PR 值为 0.79–0.96,而组合预测因子的AUC= 1.0
7.开发快速和精细的 LC-MS/MS 方法并评估独立和纵向iRBD队列(独立复制队列 - 第2阶段)
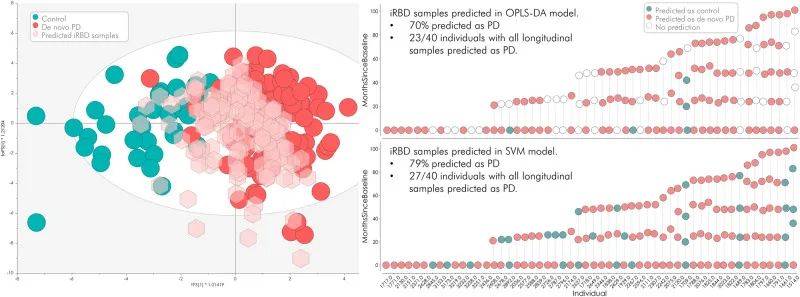
为了评估针对高危受试者的初始预测模型的结果,开发并改进了的靶向和多重蛋白质组学测试,以仅定量那些从初始靶向蛋白质组学测定中易于可靠检测到的蛋白质(n = 32)。接下来,分析了来自54名iRBD患者的独立队列的另外146个纵向样本。将第二阶段所有可用的纵向 iRBD 样本(n = 146)应用于第一阶段构建的两个机器学习模型(OPLS-DA 和支持向量机)(PD 与 HC)。OPLS-DA模型基于所有32种检测到的蛋白质,将70%的iRBD样品鉴定为PD,而基于8种蛋白质的 SVM 模型将 79% 的样品鉴定为 PD。如上所述,在分析时,纵向 iRBD 验证队列中的 54 名受试者中有 16 名患有 PD/DLB。最早的正确分类是表型转化前7.3年,最晚的分类是诊断前 0.9 年(平均 3.5 年± 2.4 年)。
 (图源:Hällqvist et al., Nature Communications, 2024)
(图源:Hällqvist et al., Nature Communications, 2024)
图7 一组新获得的前驱孤立性快速眼动睡眠行为障碍(iRBD)样本(II 期)的预测结果。在OPLS-DA模型中预测了来自诊断为iRBD的个体的146份新血清样本,其中几份具有纵向随访样本。70%的样本被预测为帕金森病(PD),40 人中有23人的所有纵向样本被预测为PD。在更精细的支持向量机(SVM)模型中,146 个新样本中有79%被预测为PD,40个个体中有27个始终将其所有纵向样本预测为PD
8. 差异表达的蛋白质生物标志物与靶向蛋白质组学验证阶段患者临床数据之间的相关性
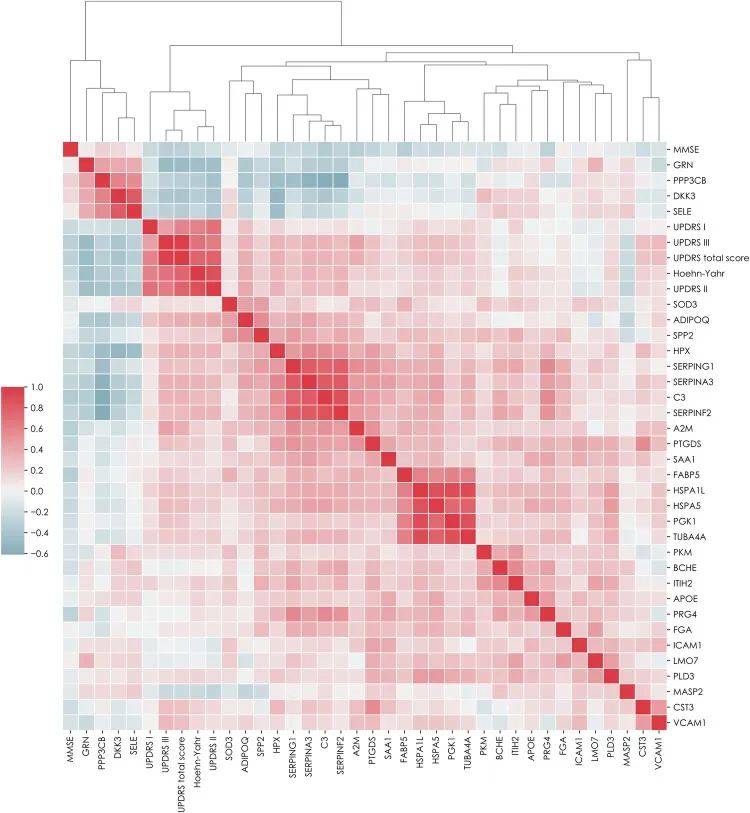
接下来评估PD和HC(从第1阶段)中的蛋白质表达与临床评分的关系,发现 GRN、DKK3、PPP3CB 和 SELE 与 H&Y 和 UPDRS 第 II 部分、III 部分和总分呈负相关,可能表明更严重的临床(尤其是运动)损伤与 Wnt 信号通路(DKK3 和 PPP3CB)中标志物的低表达之间存在联系。较高的胱抑素C血浆水平与UPDRS第III部分(运动性能)和 UPDRS 总分中的较高数字相关。PTGDS血浆水平也与MMSE呈负相关。中枢补体级联蛋白 C3 与 MMSE 呈负相关,与 H&Y、UPDRS 第 III 部分和总分呈正相关。UPR调节蛋白BiP(HSPA5)与MMSE呈负相关,与H&Y和UPDRS第II、III部分和总分呈正相关。ERAD相关蛋白HSPAIL和脂联素与H&Y、UPDRS第II、III部分和总分呈正相关。SERPINs(SERPINA3、SERPINF2和SERPING1)和血红素(HPX)与MMSE呈负相关,与H&Y和UPDRS第II、III部分和总分呈正相关。一般来说,MMSE评分与H&Y阶段和UPDRS评分呈负相关(图8)。
 (图源:Hällqvist et al., Nature Communications, 2024)
(图源:Hällqvist et al., Nature Communications, 2024)
图8 通过靶向质谱法测量的蛋白质的相关性和聚类热图以及对照组和帕金森病受试者的临床评分(第1阶段)。使用 Spearman 程序进行关联,并将聚类方法设置为平均值。MMSE简易精神状态检查,UPDRS统一帕金森病评定量表
小结
帕金森病已成为世界上增长最快的神经退行性疾病,目前影响着全球近1000万人。因此,迫切需要疾病改善和预防战略。这种策略的发展受到两个局限性的阻碍:我们对帕金森病分子病理生理学中最早事件的理解存在重大差距,并且我们缺乏可靠和客观的生物标志物和易于获得的生物体液中的测试。因此,我们需要能够更早地识别PD的生物标志物,最好是在个体出现严重的神经元损失和致残性运动和/或认知疾病之前的重要时间。这些生物标志物将推进基于人群的筛查,以确定有风险的个体以及哪些人可以被纳入即将到来的预防试验。
拜谱小结
将多组学分析转移到具有临床意义的结果,直接影响未来的药物试验计划和生物标志物验证。血液检测组可以在未来进一步验证后帮助识别有患PD/DLB风险的受试者,并为即将到来的预防试验对他们进行分层。血清和血浆样本具有很高的相关性,相反,血浆/血清和脑脊液配对样本的分析仅与这些外周和中央隔室中的标志物浓度呈弱相关,因此有必要对不同的样本类型进行生物标志物的筛查并找到最佳特异性的标志物。拜谱生物作为一家国内领先的多组学服务公司,可提供成熟完善的蛋白质组学、代谢组学、转录组与基因组等多组学技术服务,助力高分文章的发表。针对血液样本,拜谱生物推出了医学大队列血液多组学多维解决方案,可提供超高深度血液蛋白质组、糖蛋白修饰组、血液标志物精准靶向检测、血液代谢组等多组学技术服务,欢迎大家咨询!
参考文献:
Hällqvist J, Bartl M, Dakna M, Schade S, Garagnani P, Bacalini MG, Pirazzini C, Bhatia K, Schreglmann S, Xylaki M, Weber S, Ernst M, Muntean ML, Sixel-Döring F, Franceschi C, Doykov I, Śpiewak J, Vinette H, Trenkwalder C, Heywood WE, Mills K, Mollenhauer B. Plasma proteomics identify biomarkers predicting Parkinson's disease up to 7 years before symptom onset. Nat Commun. 2024 Jun 18; 15(1): 4759. doi: 10.1038/s41467-024-48961-3.