

单细胞技术以“细胞级分辨率”和“多模态联合分析”的优势,日益成为生命科学领域的核心工具。近一个月来中国学者在Cell、Nature、Science顶级期刊连续发表多项单细胞多组学突破性研究——从胚胎发育的表观密码到癌症免疫的微观战场,不断突破人类对生命认知的边界。拜谱生物也在积极探索更多维度的组学技术突破,致力于搭建单细胞&空间多组学技术平台,为系统生物学研究赋能。
PART.1
单细胞表观遗传新突破—scNanoATAC-seq2

2025年3月28日,北大汤富酬课题组/清华纪家葵课题组合作,首次报道了scNanoATAC-seq2技术。这项技术实现了对单细胞起始量的样本进行分析,揭示了小鼠着床发育前的染色质可及性图谱。
小编解读:ScATAC-seq虽已被广泛应用,但珍稀样本因样本量少难以满足实验需求。ScNanoATAC-seq解决了在单细胞起始量下研究染色质可及性的难题,能够精准捕捉重复元件的染色质状态,解决了重复序列、等位基因检测、低检出度基因检测等问题。推动单细胞功能基因组研究,为遗传和发育异常等相关疾病的诊断和治疗提供可靠方法。
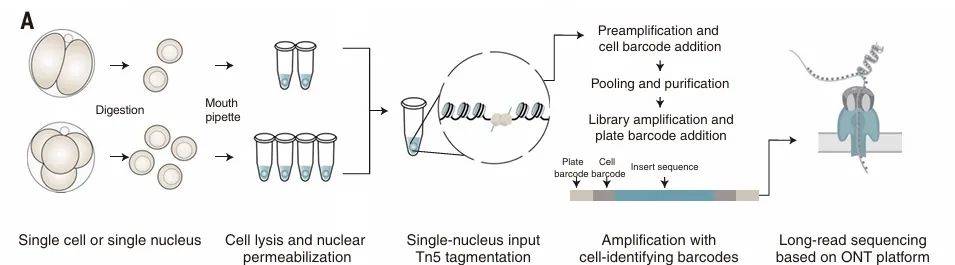 图1.scNanoATAC-seq2对小鼠着床前胚胎发育十个关键阶段进行分析
图1.scNanoATAC-seq2对小鼠着床前胚胎发育十个关键阶段进行分析
PART.2
单细胞组蛋白修饰新方法—靶染色质索引和标记(TACIT)

2025年2月26日,北京大学何爱彬团队在《Nature》上发布单细胞组蛋白修饰检测新技术TACIT(Target Chromatin Indexing and Tagmentation)和CoTACIT(Combined assay of Target Chromatin Indexed and Tagmented),成功构建小鼠胚胎着床前连续时间多维组蛋白修饰图谱。
小编解读:单细胞组蛋白修饰检测技术受限于起始样本量和分辨率,难以广泛应用。TACIT与CoTACIT将单细胞有效reads数提升近 50 倍(中位数达49万+),实现单细胞组蛋白修饰全景分析。突破传统技术样本量限制,仅需20个细胞即可实现全基因组覆盖,信噪比显著优于现有方案。研究通过整合scRNA-seq与多组学数据,结合ChromHMM框架揭示胚胎发育早期染色质动态重编程规律,首创时间分辨表观谱系树。这项兼具单细胞精度与全景分析能力的技术,推动了再生医学应用转化。
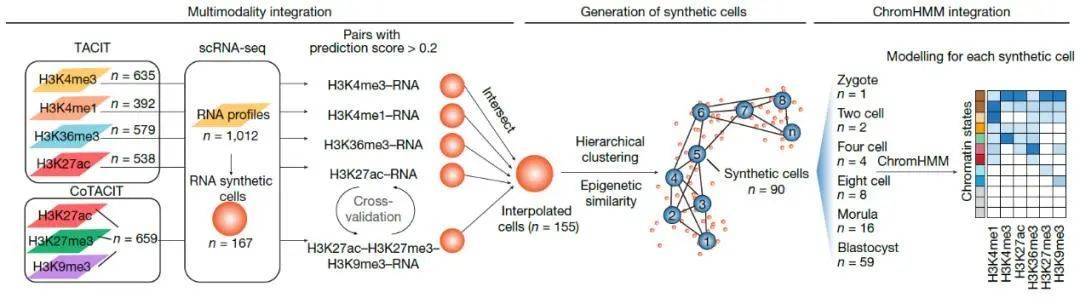 图2. 多模态整合分析流程图
图2. 多模态整合分析流程图
PART.3
单细胞的精准医疗探索—免疫亚型指导复发预测

2025年3月26日,北京大学张泽民院士课题组与合作团队在《Cell》发表研究,通过scRNA/TCR-seq解析非小细胞肺癌新辅助治疗后免疫微环境异质性,为临床实践提供指导。
小编解读:作为肿瘤与生信领域的领军人物,张泽民院士团队将非小细胞肺癌术后复发风险预测提升至单细胞精度,建立五型免疫分型模型。并利用scTCR-seq揭示non-MPR患者克隆扩增差异,识别耐药机制,推动肿瘤免疫研究向临床转化。该成果标志着张泽民教授从"泛癌图谱到治疗图谱"科研理念的实践突破,为精准分型治疗提供新范式。
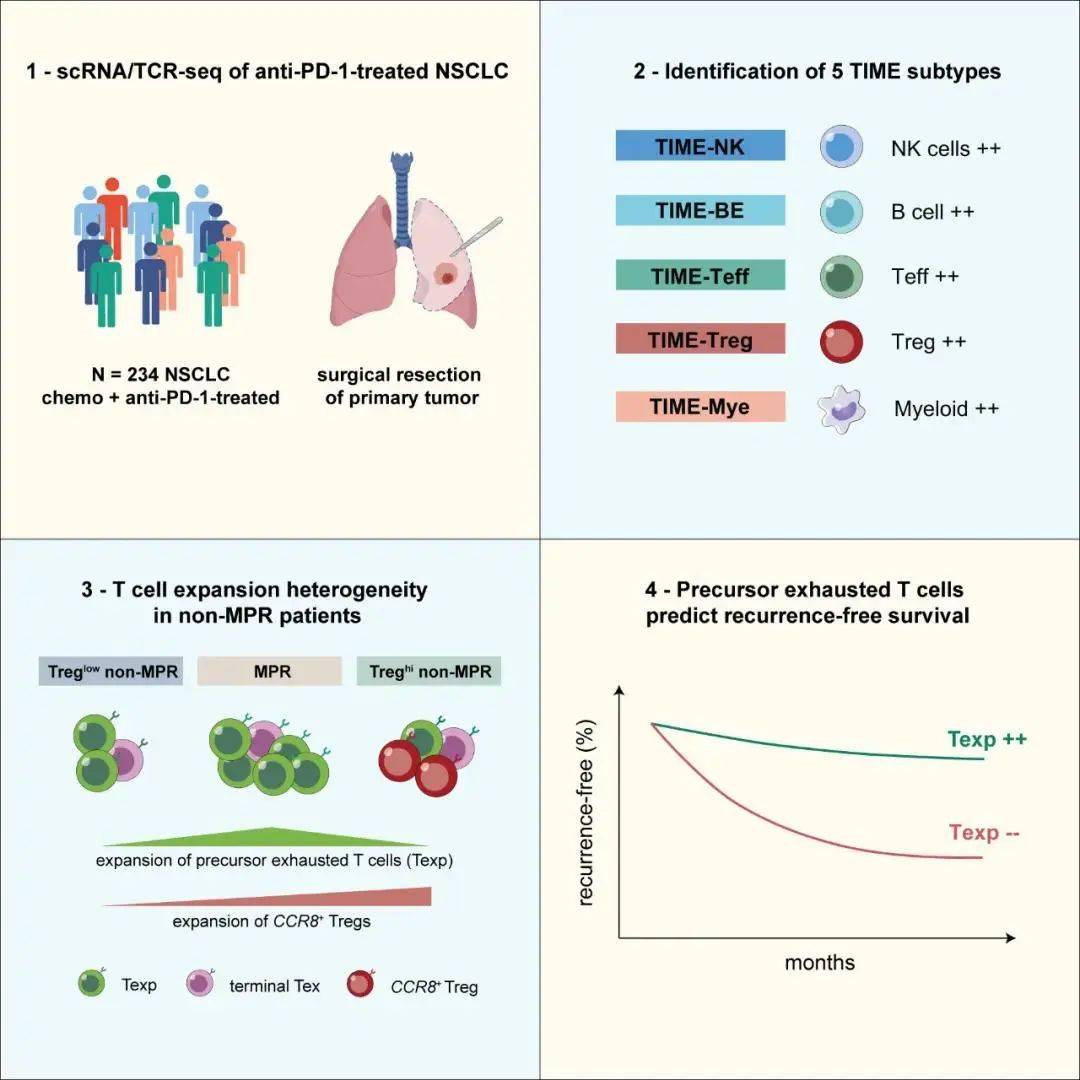 图3 研究方案及主要发现
图3 研究方案及主要发现
PART.4
拜谱小结
单细胞技术,凭借其不断迭代的技术更新, 从基因、转录快速拓展至表观、蛋白及代谢多维解析,重塑生命科学边界,贯穿胚胎发育、肿瘤治疗等全领域,加速基础研究向临床转化。拜谱生物基于前沿技术迭代与质谱平台,推出覆盖时空全组学的全方位解决方案,可提供 单细胞&空间多模态、多组学 服务,为科研与临床提供更精准的“细胞宇宙导航图”。
参考文献原文链接:
[1]https://www.science.org/doi/10.1126/science.adp4319
[2]https://www.nature.com/articles/s41586-025-08656-1#Sec48
[3]https://doi.org/10.1016/j.cell.2025.03.018