

前言
N-氯牛磺酸(Tau-Cl)是一种内源性代谢物,主要在病原体入侵时由巨噬细胞和中性粒细胞产生。Tau-Cl已知具有抗菌和抗病毒作用,但其在抗病毒先天免疫反应中的具体作用尚不清楚。
2025年1月,山东大学赵伟团队在Redox Biology(IF=10.7)上发表了题为“Endogenous metabolite N-chlorotaurine attenuates antiviral responses by facilitating IRF3 oxidation”的研究性论文。该研究不仅揭示了Tau-Cl在抗病毒免疫反应中的新作用,还为理解病毒感染过程中宿主微环境的调控机制提供了新的视角。通过调控Tau-Cl的产生,可能为治疗病毒感染和自身免疫疾病提供新的治疗靶点。拜谱生物为该研究成果提供了蛋白质修饰质谱检测服务。

中文标题:内源性代谢物N-氯牛磺酸通过促进IRF3氧化作用减弱抗病毒反应
期刊:Redox Biology
影响因子:10.7 (2025.01)
客户单位:山东大学
研究材料:人源beads
拜谱提供技术:蛋白质修饰质谱检测服务
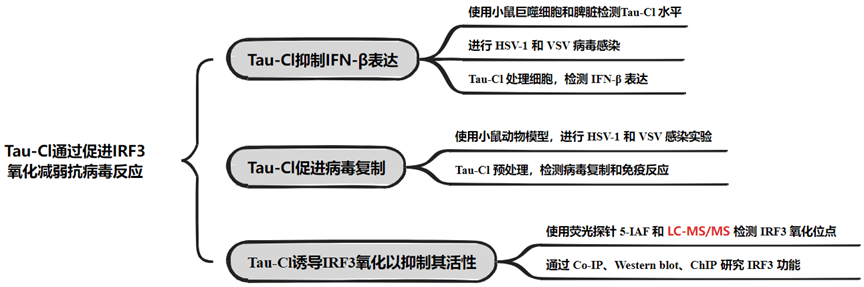
技术路线:
PART.01
研究结果
Tau-Cl抑制IFN-β表达
研究发现,病毒感染会上调细胞内Tau-Cl的水平。Tau-Cl通过促进IRF3的氧化修饰(Cys222和Cys371),抑制IRF3的磷酸化和核转位,从而阻断IRF3和IFN-β启动子区域的结合,最终抑制I型干扰素的产生。
Tau-Cl促进病毒复制
Tau-Cl不仅抑制了I型干扰素的产生,还促进了病毒在体内和体外的复制。实验表明,Tau-Cl处理的小鼠在病毒感染后表现出更严重的免疫细胞浸润和更高的病毒载量。
Tau-Cl诱导IRF3氧化以抑制其活性
作者通过前期的其他实验推测Tau-Cl可能靶向IRF3。Tau-Cl通过氧化半胱氨酸残基来影响蛋白质功能。然后,作者研究了Tau-Cl是否可以介导IRF3氧化。作者使用了荧光探针5-碘乙酰氨基荧光素(5-IAF),它与还原型半胱氨酸残基的巯基共价结。在Tau-Cl处理后,IRF3不再被5-IAF标记,表明它们的半胱氨酸残基被氧化(图1A)。为了进一步确定IRF3的潜在氧化位点,作者进行了LC-MS/ MS分析。残基Cys222和Cys371在物种之间是保守的,被确定为IRF3的潜在Tau-Cl诱导氧化位点(图1B)。因此,Tau-Cl抑制了TBK1和IRF3之间的相互作用,以及TBK1诱导的IRF3磷酸化(图1C-E)。IRF3的二聚化和核转位对其转录活性至关重要。作者发现Tau-Cl抑制病毒感染诱导的IRF3二聚化和核易位(图1F和G)。ChIP检测表明,Tau-Cl还阻断了IRF3与IFN-β启动子区域的结合(nt-200至-41)。总的来说,这些数据表明Tau-Cl诱导IRF3氧化以抑制其活性。
 图1|Tau-Cl抑制IRF3激活
图1|Tau-Cl抑制IRF3激活
(图源:Yang Y., et al., Redox Biol., 2025)
PART.02
文章小结
Tau-Cl促进了IRF3在Cys222和Cys371处的氧化,这是一种控制I型干扰素转录的关键转录因子。Tau-Cl抑制IRF3的磷酸化和核转位,并阻断IRF3与IFN-β启动子区的结合。因此,作者确定Tau-Cl是IRF3驱动的抗病毒先天反应的内源性抑制因子,并通过影响宿主微环境揭示了病毒的免疫逃逸机制。
 图2|Tau-Cl在IFN-β产生中的作用示意图
图2|Tau-Cl在IFN-β产生中的作用示意图
(图源:Yang Y., et al., Redox Biol., 2025)
PART.03
拜谱小结
该研究通过靶向IRF3确定Tau-Cl是抗病毒先天免疫的内源性抑制因子,并建议氧化是IRF3的一种新型PTM。考虑到IRF3在控制病毒感染和多种自身免疫性疾病发展中的重要作用,控制Tau-Cl的产生可以作为治疗由IRF3活性异常引起的疾病的一种有前途的治疗策略。其中拜谱生物提供了蛋白质修饰质谱检测服务。拜谱生物已建立了完善成熟的转录组学、蛋白组学、翻译后修饰组、代谢组学以及多组学联合产品技术服务体系,助力发表高分文献,欢迎致电咨询!
参考文献:
Yang Y, Wang C, Sun W, Fu Y, Wu X, Zhao C, Song H, Zhao W, Qin Y. Endogenous metabolite N-chlorotaurine attenuates antiviral responses by facilitating IRF3 oxidation. Redox Biol. 2025 Mar;80:103492. doi: 10.1016/j.redox.2025.103492