


蛋白质翻译后修饰(PTM)是通过添加或去除官能团对蛋白质功能产生影响的过程。糖基化是最常见的PTM之一,也是一种极其复杂且最为丰富的蛋白质翻译后修饰类型,对于生物体中各种功能活动的开展至关重要,且与蛋白质的溶解性、稳定性和活性密切相关。然而,糖基化残基的底层组成和结构尚未确定。全面了解糖基化的内部结构和差异表达,并采用先进的检测技术以推动相关疾病研究的进程势在必行。
2024年8月,山东大学和山东第一医科大学附属省立医院等单位在Signal Transduction and Targeted Therapy (IF=40.8)上联合发表了题为“Glycosylation: mechanisms, biological functions and clinical implications”的综述文章。作者首先简要总结了糖基化的机制及其生物学功能,并讨论了糖基化对人类疾病的影响。然后阐述了糖基化作为疾病诊断和预后生物标志物的潜在价值,概述了糖基化检测方法,并简要讨论了每种方法的优点和局限性。此外,本文还讨论了与糖基化相关的靶向治疗,以及在临床开发中遇到的挑战。

01、糖基化的分类与机制
蛋白质糖基化是指将以糖苷形式存在的寡糖用共价键的形式结合到蛋白质的某些氨基酸残基上的过程。根据氨基酸类型和聚糖的连接方式,常见的蛋白糖基化修饰类型可分为O-糖基化、N-糖基化、C-糖基化和GPI锚定(图1)。其中N-糖基化和O-糖基化是最常见的类型,与疾病发病机制和进展密切相关。
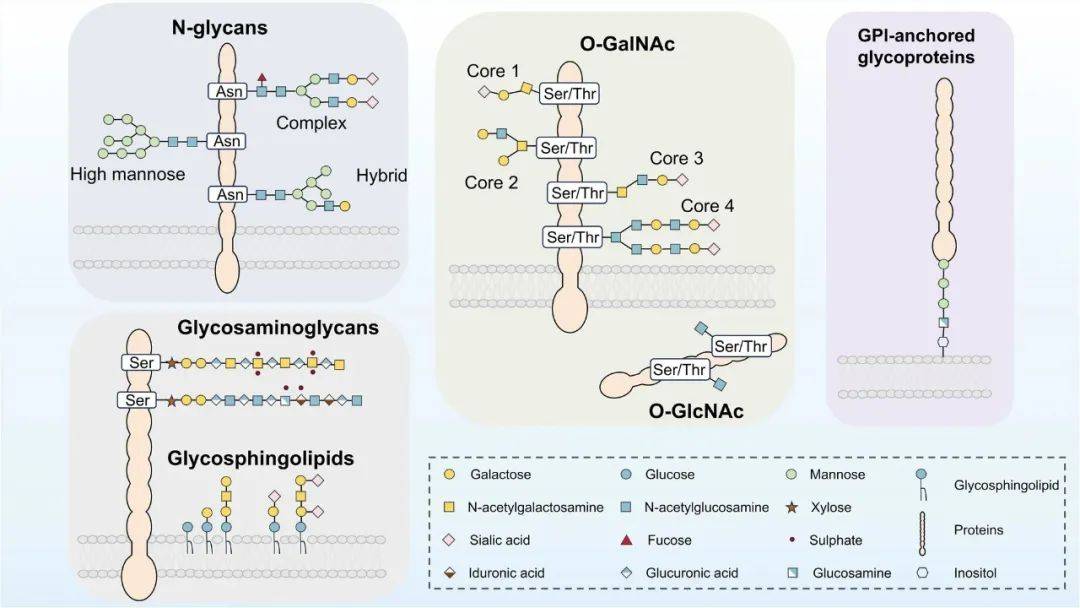 图1 蛋白质糖基化修饰主要类型图
图1 蛋白质糖基化修饰主要类型图
(图源:Mengyuan He, et al., Signal Transduct Target Ther., 2024)
02、糖基化的生物学功能
糖基化具有多种生物学功能,可以影响蛋白质折叠、稳定性、免疫逃逸和信号转导等方面(图2)。
(1)蛋白质折叠和稳定性的调节:糖基化影响蛋白质的正确折叠和稳定性。N-糖基化在内质网中指导糖蛋白与伴侣蛋白相互作用,确保正确折叠。O-糖基化有助于稳定蛋白质结构域并促进蛋白质分泌。
(2)相分离的调控:O-GlcNAc糖基化在细胞内的液-液相分离过程中起多重调控作用,有助于调节淀粉样蛋白聚集等过程,进而影响细胞内信号传递和结构维持。
(3)细胞粘附的调控:糖基化显著影响细胞与细胞、细胞与细胞外基质的相互作用。粘附分子如钙粘蛋白、整合素和选择素的糖基化模式与癌症中的肿瘤进展、免疫逃逸及转移密切相关。N-糖基化和O-糖基化调控了钙粘蛋白等关键粘附分子的功能,从而影响细胞间粘附强度及信号转导。
(4)免疫逃逸机制:糖基化在病原体和肿瘤细胞免疫逃逸中发挥重要作用。异常的糖基化模式,如肿瘤微环境中唾液酸的过度表达,能够与Siglec等受体相互作用,抑制免疫系统的识别和攻击。癌细胞通过产生异常糖链,干扰宿主的免疫监视,促进肿瘤细胞的免疫逃逸。
(5)信号转导通路的调控:糖基化通过调节关键的细胞信号转导通路(如Notch、JAK-STAT、TGF-β和Wnt/β-catenin)来影响细胞生长、分化和免疫反应。糖基化异常可导致信号通路失调,进而与多种疾病(如癌症、纤维化等)密切相关。
(6)代谢调控:蛋白质的糖基化与脂质代谢息息相关,尤其是通过影响脂蛋白受体的表达,调控低密度脂蛋白和高密度脂蛋白的代谢。在肿瘤细胞中,糖基化对谷氨酰胺代谢等关键代谢途径具有重要调控作用,从而影响肿瘤的生长和代谢重编程。
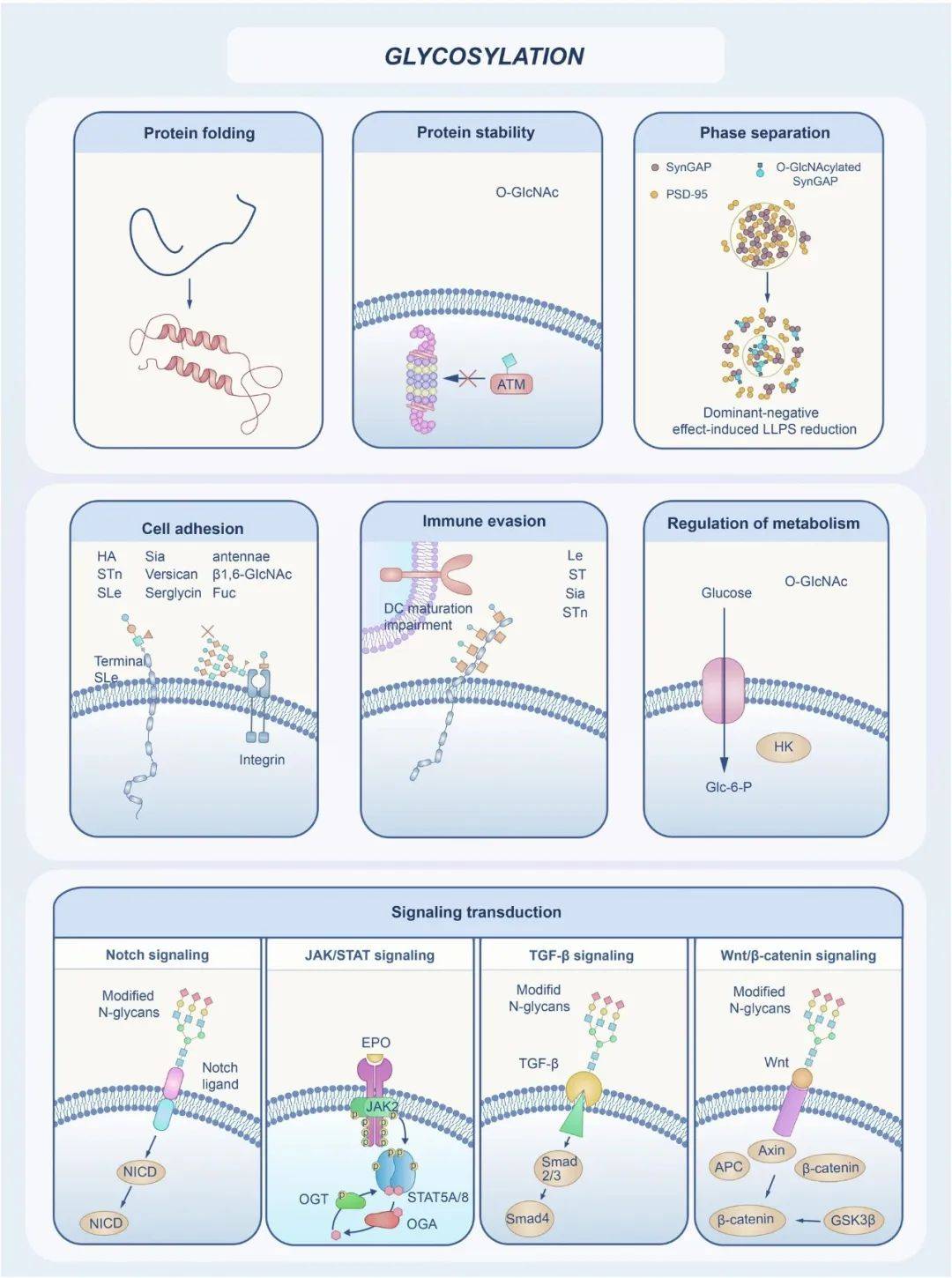 图2 糖基化的多种生物学功能
图2 糖基化的多种生物学功能
(图源:Mengyuan He, et al., Signal Transduct Target Ther., 2024)
03、人类疾病中的异常糖基化
蛋白质糖基化在生物体中广泛存在,涉及细胞免疫、蛋白质翻译调节和信号通路等各种过程。异常的糖基化与各种疾病的发生和发展有关(图3)。
(1)血液系统恶性肿瘤:糖基化在血液系统恶性肿瘤(如急性髓性白血病、急性淋巴细胞白血病、慢性淋巴细胞白血病等)的发生和发展中发挥重要作用。急性髓性白血病中的FLT3受体糖基化异常会促进白血病细胞的增殖和存活,而改变其糖基化可通过靶向疗法改善预后。在急性淋巴细胞白血病中,O-GlcNAc糖基化调控Myc蛋白的活性,促进白血病细胞的快速增殖。慢性淋巴细胞白血病中B细胞受体(BCR)的糖基化异常与抗原识别和信号传导功能的改变有关。
(2)淋巴瘤:在滤泡性淋巴瘤中,BCR可通过体细胞高频突变引入N-糖基化位点,高甘露糖类型的N-糖基化可持续激活BCR信号通路,促进肿瘤细胞增殖。弥漫性大B细胞淋巴瘤中,CD45的糖基化调控其与Galectin-3的相互作用,影响细胞的磷酸酶活性,并与化疗药物的敏感性相关。
(3)实体恶性肿瘤:异常糖基化是多种实体瘤的标志,特别是在肿瘤进展、免疫逃逸和转移过程中,糖基化模式的改变起到关键作用。已有研究包括,呼吸道肿瘤、胃肠道肿瘤、生殖系统癌症、乳腺癌、中枢神经系统肿瘤、肉瘤等。
(4)自身免疫性疾病:糖基化变化可以改变免疫球蛋白G(IgG)与Fcγ片段受体(FcγR)或C1q补体的结合亲和力,从而影响IgG在调节免疫细胞活动以实现促炎或抗炎反应中的作用。已有研究包括,类风湿性关节炎、系统性红斑狼疮、炎症性长肠病、自身免疫性肝病、重症肌无力、肾病。
(5)其他疾病:除了上述肿瘤和自身免疫性疾病中糖基化的改变外,这种PTM在心血管疾病、代谢性疾病、神经退行性疾病中的研究也越来越多。
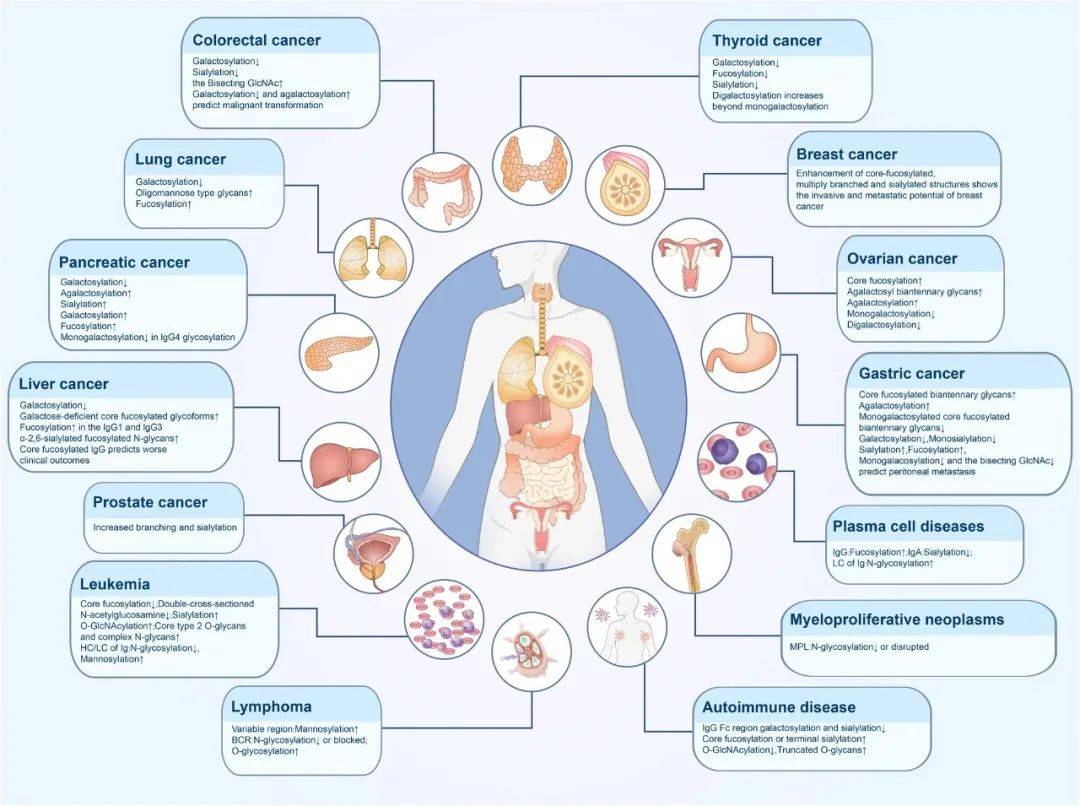 图3 人类疾病中的糖基化
图3 人类疾病中的糖基化
(图源:Mengyuan He, et al., Signal Transduct Target Ther., 2024)
04、糖基化在疾病中的诊断和预后价值
多种糖蛋白已被用作临床诊断和预测活性的肿瘤标志物,如肝癌中的甲胎蛋白(AFP)、前列腺癌中的前列腺特异性抗原(PSA),以及胰腺癌中的CA19-9等。在几种肿瘤中评估了糖基转移酶相关基因的诊断和预后价值,其中糖基转移酶相关基因和IgG的特征性糖基化也被评估为多种肿瘤的预后标志物,这也为个体化用药提供了良好的生物标志物。糖基化检测与现有诊断工具的结合,可以更好地管理疾病,促进疾病的准确诊断和治疗以及疗效监测。因此,探索糖基化蛋白作为人类疾病生物标志物的潜力非常重要。
05、靶向糖基化治疗疾病临床表现
基于聚糖的疗法是在癌症治疗中具有巨大潜力的方法,包括蛋白质糖基化抑制剂、糖基转移酶小分子抑制剂、糖基化修饰的 mAb、糖基化介导的靶向药物递送和疫苗设计等。糖基化相关靶向治疗和其他靶向治疗之间的选择取决于肿瘤的特定分子特征、患者的一般健康状况以及潜在的益处和风险。
06、糖基化检测方法
本文综述了液相色谱和质谱分析,基于凝集素技术,电泳,放射性标记等技术在糖基化检测中的应用。其中详细描述了液相色谱和质谱对糖基化位点和聚糖结构的分析。液相色谱(LC)是分离糖肽和游离寡糖中使用最广泛的技术。一项研究表明,三种亲水作用液相色谱 (HILIC)色谱柱在分离人IgG糖肽方面具有高性能,并且成功分离了IgG的A2G1F1异构体糖肽和异构体糖肽的结构潜力。质谱(MS)是一种电离样品中的分子并在磁场或电场中分离离子的方法,可高通量的检测糖基化位点和糖型,目前已成为糖类分析和糖蛋白质组学分析的有力工具。
07、未来展望
糖基化是一种极其复杂且最为丰富的蛋白质翻译后修饰类型,不仅极大地促进了蛋白质多样性的扩展,而且对蛋白质的功能产生了深远的影响。糖基化与蛋白质的溶解度、稳定性和活性密切相关。糖基化的异常或紊乱会导致人类疾病,并且被认为是癌症的标志。癌症的早期诊断、风险预测和治疗需要新的方法,蛋白质结合和糖基化模式检测相结合可能提供更好的诊断和预后性能,但如何在临床环境中准确检测糖基化位点和表达水平的变化已成为一个重大挑战。
08、拜谱小结
糖基化修饰是最常见但也是最复杂的翻译后修饰之一,广泛参与细胞黏附、识别、信号转导等重要过程,影响蛋白质的分泌、运输和稳态调控,可发生在细胞内50~70%的蛋白质上。但准确检测糖基化位点和表达水平的变化在生命科学领域还是亟待解决的问题。随着质谱技术的不断发展,针对O-糖基化、N-糖基化以及完整糖肽的分析能力已经实现质的飞跃。拜谱生物推出的完整糖肽产品可以有效检测蛋白质糖基化的位点和糖型结构,包括但不限于糖链组成、糖链长度、分支情况、糖基化位点等分析内容,该产品适用于癌症、免疫疾病、神经退行性疾病等领域的糖基化研究,助力科研人员深入挖掘糖基化在疾病发生与发展中的机制。同时,拜谱生物提供专业的技术支持和定制化服务,确保每一位客户都能获得高质量的实验结果和精准的分析数据。未来,拜谱生物将继续致力于糖基化领域的创新与突破,为推动生命科学研究和临床应用提供坚实保障。想了解更多关于完整糖肽产品的信息,欢迎咨询!
参考文献:
He M, Zhou X, Wang X. Glycosylation: mechanisms, biological functions and clinical implications. Signal Transduct Target Ther. 2024 Aug 5;9(1):194. doi: 10.1038/s41392-024-01886-1. PMID: 39098853; PMCID: PMC11298558