

近年来,中药的研究和应用越来越受到关注。随着现代科学技术的发展,如何利用现代技术手段发掘中药的新靶点成为研究的热点。在最新发表的两篇顶刊文章中,研究者利用蛋白质组学技术成功找到了中药的作用靶点,为中药的现代化研究提供了新的思路。
首先,我们来看一下这两篇文章。第一篇文章的是2024年9月11日发表在Nature上的A brain-to-gut signal controls intestinal fat absorption,由上海交通大学医学院附属瑞金医院王卫庆、王计秋团队领衔,他们通过光亲和化学方法发现葛根素作用于GABAA受体α1亚基,揭示了大脑通过DMV-迷走-空肠轴调控肠道脂肪吸收的机制,并证实葛根素具有减肥潜力。拜谱生物为此提供蛋白质组学的检测内容。

为了深入揭示大脑迷走神经背侧核(DMV)神经元如何抑制肠道脂肪吸收的分子机制,研究团队采用了以天然化合物葛根素为诱饵的活性蛋白质组学策略。通过精心设计的光反应性标签,合成了葛根素特异性探针,并利用这些探针通过光亲和化学反应成功富集和可视化潜在的靶蛋白。经过光亲和反应后,利用液相色谱和串联质谱(LC-MS /MS)技术对这些靶蛋白进行了精确鉴定,并从中筛选出GABAA受体α1亚基(GABRA1)作为葛根素的关键作用靶标。为了进一步验证葛根素与GABRA1蛋白之间的相互作用,进行了WB实验,并成功确认了两者之间的联系。此外,利用冷冻电镜(cryo-EM)技术解析了GABAA受体与葛根素的复合物结构,并明确了葛根素结合的具体位置和作用方式。这些发现表明,葛根素作为一种天然化合物,通过靶向GABAA受体α1亚基,能够抑制DMV神经元活性,进而减少肠道脂肪的吸收,为葛根素在肥胖和代谢性疾病治疗中的应用提供了科学依据。
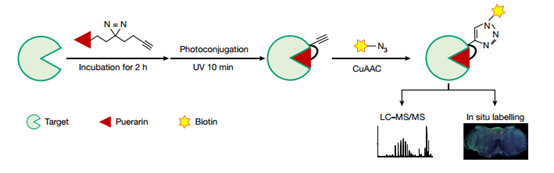 图1 光亲和反应示意图(图源:Lyu, et al., Nature, 2024)
图1 光亲和反应示意图(图源:Lyu, et al., Nature, 2024)
第二篇文章是2024年6月发表在Science上的Artemisinins ameliorate polycystic ovarian syndrome by mediating LONP1-CYP11A1 interaction,由复旦大学汤其群教授团队主导,揭示了青蒿素通过增强 LONP1-CYP11A1 之间的相互作用来抑制卵巢雄激素合成,从而改善多囊卵巢综合征的症状。

这项研究采用了基于质谱的相对定量蛋白质组学分析,发现CYP11A1蛋白在青蒿素处理下显著下调,这一发现与青蒿素抑制雄激素合成的观察结果相吻合。为了深入探究青蒿素诱导CYP11A1不稳定的机制,研究团队采用了免疫沉淀联用质谱(IP-MS)技术,鉴定了青蒿素处理下CYP11A1的相互作用伙伴。进一步的共免疫沉淀(CO-IP)实验表明,青蒿素能显著增强LONP1与CYP11A1之间的相互作用。更为关键的是,通过生物素与青蒿素偶联(bio-ATS)的下拉实验,研究证实了青蒿素的直接靶点是LONP1而非CYP11A1。这一发现通过分子对接实验得到了进一步证实,为青蒿素的作用机制提供了坚实的科学依据。这一研究不仅阐明了青蒿素在治疗疟疾中的分子机制,也为青蒿素在抗雄激素相关疾病中的应用提供了新的思路。青蒿素作为一种来自中药的天然化合物,其现代药理学研究正不断拓展,为传统中药的现代化应用开辟了新的道路。
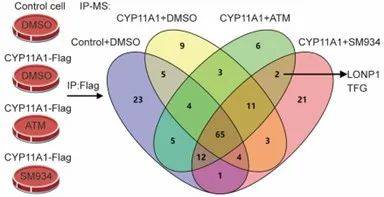 图2 采用IP-MS方法鉴定CYP11A1的青蒿素应答相互作用蛋白
图2 采用IP-MS方法鉴定CYP11A1的青蒿素应答相互作用蛋白
(图源:Liu, et al., Science, 2024)
技术总结
生物活性化合物在细胞筛选和体内激发活性的分子机制研究中,靶标鉴定已发展出一系列方法。其中,基于质谱的蛋白质组学技术以其独特优势,在直接分析小分子与蛋白质组的相互作用方面发挥着关键作用。具体而言,化学蛋白质组学技术能够通过生化或生物物理程序检测化合物与蛋白质的直接相互作用。这些方法通常依赖于从细胞提取物或活细胞系统中富集药物靶点,这些靶点是通过从所研究的生物活性化合物中提取的化学探针来实现的。
拜谱小结
自古以来,中药就在我国人民的健康中扮演着不可或缺的角色。从《黄帝内经》到现代医学研究,中药的疗效和作用机制一直是人们关注的焦点。然而,中药复杂多样的成分和作用方式,使得其作用机制的研究充满了挑战。随着现代科学技术的进步,特别是生物技术的飞速发展,我们有了更多、更先进的工具来探索中药的奥秘。
化学蛋白质组学技术,特别是限制性酶解-质谱分析(LiP-MS),正成为揭示中药作用机制的一把“金钥匙”。LiP-MS技术不仅能够帮助我们深入理解中药的药效机制,还能够为中药的现代化和新型药物开发提供强有力的支持。LiP-MS技术之所以备受青睐,得益于其诸多显著优点:
高通量 :LiP-MS能够同时分析多个样本,非常适合大规模的蛋白质组学研究,大大提高了研究效率。
无需同位素标记:相较于其他蛋白质组学技术,LiP-MS不需要使用昂贵的同位素标记,显著降低了实验成本。
提供结构信息:通过分析酶解产生的肽段,LiP-MS能够推断蛋白质的折叠状态和结构域信息,为理解蛋白质的功能提供重要线索。
适用于多种蛋白质:无论是可溶性的还是膜结合的蛋白质,LiP-MS都能进行分析,展现了其广泛的应用范围。
减少样品处理步骤:与传统的蛋白质分析技术相比,LiP-MS通常需要较少的样品前处理步骤,简化了实验流程。
LiP-MS主要用于检测蛋白丰度和结构变化,并识别不同条件下结构特异性蛋白水解指纹图谱的新型技术,可用于原位检测蛋白功能变化,通过将蛋白质动态结构数据与功能相联系,有助于推动结构生物学和系统生物学的进一步发展。基于此,拜谱生物推出的LiP-MS产品,在蛋白处于天然构象的条件下,用广谱蛋白酶对其进行酶切,并通过DIA扫描模式,结合高端的质谱仪实现LiP酶切肽段和靶蛋白的高质量检出,进而解析蛋白构象变化,可同时获取蛋白质丰度和蛋白构象变化两个维度的信息,为药物靶标发现、药物作用机制等研究提供了重要的手段。欢迎大家咨询!
参考文献:
1) Lyu Q, Xue W, Liu R, Ma Q, Kasaragod VB, Sun S, Li Q, Chen Y, Yuan M, Yang Y, Zhang B, Nie A, Jia S, Shen C, Gao P, Rong W, Yu C, Bi Y, Zhang C, Nan F, Ning G, Rao Z, Yang X, Wang J, Wang W. A brain-to-gut signal controls intestinal fat absorption. Nature. 2024 Sep 11. doi: 10.1038/s41586-024-07929-5.
2) Liu Y, Jiang JJ, Du SY, Mu LS, Fan JJ, Hu JC, Ye Y, Ding M, Zhou WY, Yu QH, Xia YF, Xu HY, Shi YJ, Qian SW, Tang Y, Li W, Dang YJ, Dong X, Li XY, Xu CJ, Tang QQ. Artemisinins ameliorate polycystic ovarian syndrome by mediating LONP1-CYP11A1 interaction. Science. 2024 Jun 14;384(6701):eadk5382. doi: 10.1126/science.adk5382.
3) Meissner F, Geddes-McAlister J, Mann M, Bantscheff M. The emerging role of mass spectrometry-based proteomics in drug discovery. Nat Rev Drug Discov. 2022 Sep;21(9):637-654. doi: 10.1038/s41573-022-00409-3.