

S-亚硝基化在NO细胞信号的传递中起关键作用,这是一种与磷酸化相似的蛋白翻译后修饰,广泛参与细胞功能调控。S-亚硝基化的失调与多种疾病紧密相关,包括阿尔茨海默症、癌症、肌肉萎缩症、心力衰竭和糖尿病等。与酶驱动的磷酸化修饰不同的是,S-亚硝基化修饰的基本催化机制尚不明确。2023年12月5日,美国凯斯西储大学医学系Jonathan S. Stamler团队在Cell上在线发表了题为“An enzyme that selectively S-nitrosylates proteins to regulate insulin signaling”,文章确定了一种使用SNO-CoA作为辅助因子对多种蛋白质进行S-亚硝基化的酶SCAN,其底物包括胰岛素受体(INSR)和胰岛素受体底物1 (IRS1)。SCAN活性在生理上调节胰岛素信号,其异常活性可导致糖尿病的发生。

英文标题:An enzyme that selectively S-nitrosylates proteins to regulate insulin signaling(Cell,IF=66.85,2023)
中文标题:一种特异性催化S-亚硝基化蛋白质以调节胰岛素信号的酶
研究材料:HEK293细胞
组学技术:S-亚硝基化修饰组
主要研究结果
01.SCAN介导高脂饮食(HFD)中INSRβ/IRS1的S-亚硝基化和胰岛素抵抗
为了确定SCAN在哺乳动物中的生理作用,作者使用了全身SCAN基因敲除的小鼠模型。由于SCAN含有一个未知功能的胰岛素受体(INSR)相互作用结构域,作者进一步研究了SCAN/SNO-CoA在胰岛素信号传导中的作用。在HFD的条件下,SCAN基因敲除小鼠体重增加较慢,其对胰岛素的敏感性较高,这说明SCAN在HFD小鼠中促进了胰岛素抵抗。进一步研究发现,HFD饲养的小鼠中,SCAN敲除小鼠表现出较低水平的S-亚硝基化INSRβ和IRS1,并且胰岛素效应子AKT和AS160的磷酸化水平较高。这表明SCAN介导的S-亚硝基化抑制INSRβ/IRS1依赖的胰岛素信号传导在很大程度上是通过抑制INSRβ的酪氨酸激酶活性(图1)。
 图1. SCAN介导高脂饮食中INSRβ/IRS1的S-亚硝基化和胰岛素抵抗 (图源:Zhou et al., Cell
图1. SCAN介导高脂饮食中INSRβ/IRS1的S-亚硝基化和胰岛素抵抗 (图源:Zhou et al., Cell
02.胰岛素诱导INSRβ/IRS1的S-亚硝基化抑制信号转导
进一步在大鼠成肌细胞L6细胞系的研究发现,胰岛素对L6-WT的细胞中INSRβ/IRS1的S-亚硝基化有促进作用,而且这种作用是动态变化的,在去除胰岛素60-120 min到达高峰,随后逐渐消退,反观在SCNA敲除的细胞中没有这种现象。通过对L6细胞和健康小鼠的研究,作者发现SCNA的缺失导致胰岛素刺激下的IRS1、AKT和AS160的磷酸化延长,这表明激动剂刺激的INSRβ/IRS1的S-亚硝基化是关闭胰岛素信号通路的负反馈回路的一部分。小鼠的胰岛素耐受实验证实,由SCAN介导的胰岛素诱导的S -亚硝基化可以关闭骨骼肌中的胰岛素信号,从而减缓葡萄糖摄取以防止低血糖(图2)。
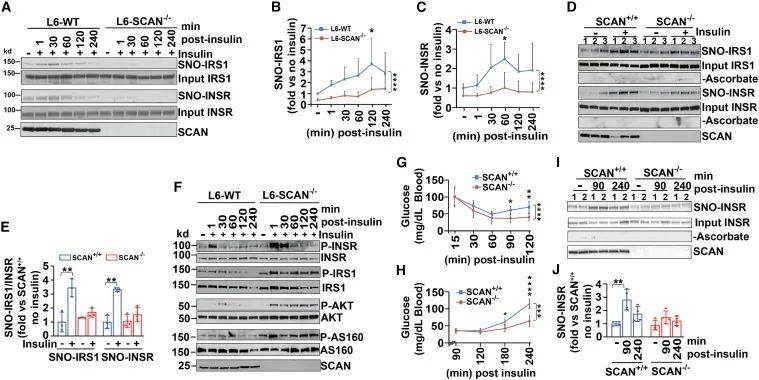 图2 胰岛素诱导INSRβ/IRS1的S-亚硝基化抑制信号转导(图源:Zhou et al., Cell, 2023)
图2 胰岛素诱导INSRβ/IRS1的S-亚硝基化抑制信号转导(图源:Zhou et al., Cell, 2023)
03.胰岛素刺激的INSRβ/IRS1的S-亚硝基化与NOS活性相关
在胰岛素刺激下,eNOS和nNOS的活性都显著增加,这表明SCAN介导的胰岛素刺激的INSRβ/IRS1的S-亚硝基化可能是利用eNOS和nNOS产生的NO。在L6细胞中,NOS抑制剂L-NMMA不仅阻断了胰岛素刺激的INSRβ/IRS1的S-亚硝基化,还阻断了SCAN本身的S-亚硝基化。因此,eNOS和nNOS可能是生理条件下SCAN活性的SNO来源(图3)。
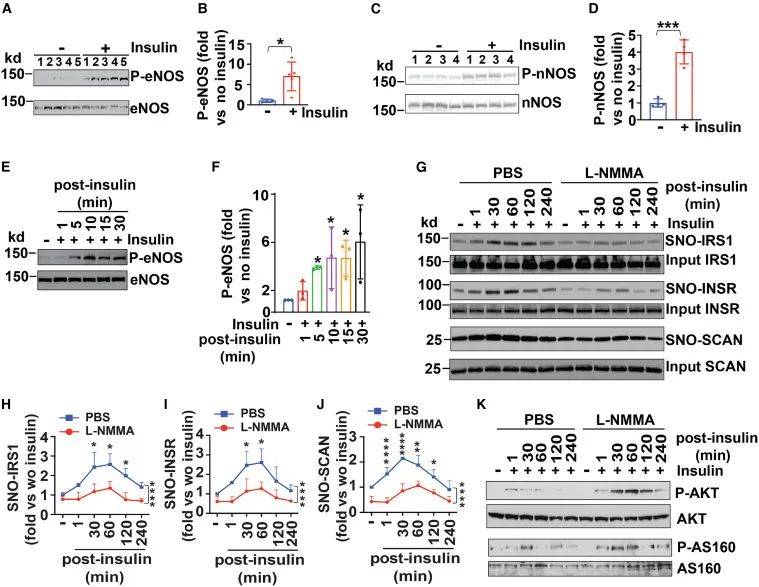 图3 eNOS和nNOS可能是生理条件下SCAN活性的SNO来源 (图源:Zhou et al., Cell, 2023
图3 eNOS和nNOS可能是生理条件下SCAN活性的SNO来源 (图源:Zhou et al., Cell, 2023
04.INSRβ的S-亚硝基化与人脂肪组织和骨骼肌中的BMI和SCAN表达相关
为了确定SCAN对INSRβ的S -亚硝基化是否与人类肥胖相关的胰岛素抵抗有关,作者量化了来自不同体重指数(BMI)患者的14个人类骨骼肌样本和26个人类脂肪库样本中SCAN的表达和SNO-INSRβ的量,发现在BMI较高的患者骨骼肌、内脏及皮下脂肪样本中表达上调。人体组织中SNO-INSRβ与BMI和SCAN存在显著的线性关系,表明SCAN介导的INSRβ的S-亚硝基化是人类胰岛素抵抗的首要因素(图4)。
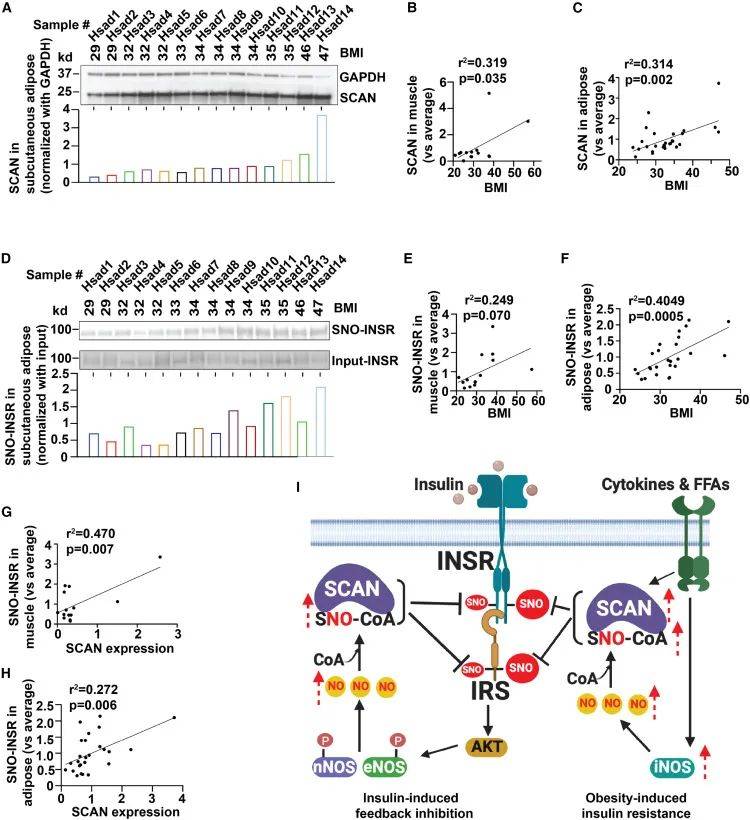 图4 基于S-亚硝基的胰岛素信号传导抑制和胰岛素抵抗(图源:Zhou et al., Cell, 2023)
图4 基于S-亚硝基的胰岛素信号传导抑制和胰岛素抵抗(图源:Zhou et al., Cell, 2023)
拜谱小结
本研究通过SCAN表达、BMI和SNO-INSRβ之间的多重线性相关(结合动物数据)表明,肥胖患者中SCAN的高表达通过INSRβ的亚硝基化导致胰岛素抵抗。据预测,整个蛋白组中70%蛋白发生S-亚硝基化,目前已鉴定超过10,000万种SNO蛋白,这也是信号传导的主要机制。本研究发现SNO会导致胰岛素抵抗,这也是其它疾病的既定特征,包括心力衰竭、阿尔茨海默病、肌肉萎缩症、恶性高热和肝癌等,因此可作为多种疾病的有潜力的治疗靶点。拜谱生物全面升级了半胱氨酸修饰蛋白质组学产品,现可提供棕榈酰化、亚硝基化、谷胱甘肽化、次磺酸化、硫巯基化、Total 氧化还原、游离巯基蛋白质组学检测服务,欢迎大家咨询!
参考文献:
Zhou HL, Grimmett ZW, Venetos NM, Stomberski CT, Qian Z, McLaughlin PJ, Bansal PK, Zhang R, Reynolds JD, Premont RT, Stamler JS. An enzyme that selectively S-nitrosylates proteins to regulate insulin signaling. Cell. 2023: S0092-8674(23)01226-6. doi: 10.1016/j.cell.2023.11.009.